填空题 适中0.65 引用1 组卷177
依题意回答下列问题。
(1)标准状况下,0.3mol C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2摩尔燃烧焓的热化学方程式:_______ 。
(2)用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
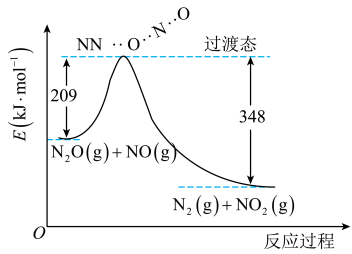
写出气态肼和N2O4反应的热化学方程式:_______ 。
(1)标准状况下,0.3mol C2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7 kJ热量,请写出表示C2H2摩尔燃烧焓的热化学方程式:
(2)用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1

写出气态肼和N2O4反应的热化学方程式:
23-24高二上·福建龙岩·阶段练习
类题推荐
(Ⅰ)请回答下列问题:
(1)在101kPa时,一定量的CO在1.00mol O2中完全燃烧,生成2.00mol CO2,放出566.0kJ热量,CO的燃烧热为ΔH=_______ ,表示CO燃烧热的热化学方程式_______ 。
(Ⅱ)试分别从能量变化和化学键变化角度研究反应2H2(g)+O2(g)=2H2O(l)的焓变。
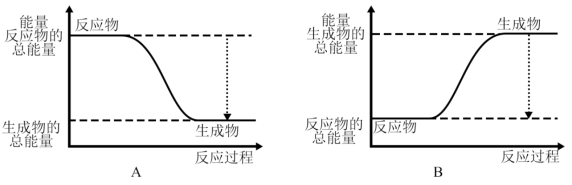
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是_______ 。
(3)从断键和成键的角度分析上述反应中能量的变化。已知化学键的键能:
由此计算2mol H2在氧气中完全燃烧生成气态水放出的热量_______ 。
(Ⅲ)依据盖斯定律回答下列问题:
已知火箭发射时可用肼(N2H4)作燃料,二氧化氮作氧化剂,这两者反应生成氮气和水蒸气。
且N2(g)+2O2(g)=2NO2(g);ΔH1=+67.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH2=-534kJ/mol ②
(4)写出肼与NO2反应的热应化学方程式_______ 。
(1)在101kPa时,一定量的CO在1.00mol O2中完全燃烧,生成2.00mol CO2,放出566.0kJ热量,CO的燃烧热为ΔH=
(Ⅱ)试分别从能量变化和化学键变化角度研究反应2H2(g)+O2(g)=2H2O(l)的焓变。
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是

(3)从断键和成键的角度分析上述反应中能量的变化。已知化学键的键能:
| 化学键 | H-H | O=O | H-O |
| 键能/kJ·mol-1 | 436 | 496 | 463 |
(Ⅲ)依据盖斯定律回答下列问题:
已知火箭发射时可用肼(N2H4)作燃料,二氧化氮作氧化剂,这两者反应生成氮气和水蒸气。
且N2(g)+2O2(g)=2NO2(g);ΔH1=+67.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH2=-534kJ/mol ②
(4)写出肼与NO2反应的热应化学方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


