解答题-原理综合题 适中0.65 引用1 组卷329
氮及其化合物在工农业生产、生活中有着重要作用。合成氨工业中: ,其化学平衡常数K与温度t的关系如表:
,其化学平衡常数K与温度t的关系如表:
完成下列填空:
(1)试比较K1、K2的大小,K1___________ K2(填写“>”、“=”或“<”)。
(2)400℃时,反应 的化学平衡常数的值为
的化学平衡常数的值为___________ 。当测得NH3和N2、H2的物质的量浓度分别为3mol/L和2molL、1mol/L时,则该反应v(N2)(正)___________ v(N2)(逆)(填写“>”、“=”或“<”)。
(3)某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。根据图像判断下列说法错误的是___________
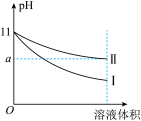
a.a值一定大于9
b.II为氨水稀释时溶液的pH变化曲线
c.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
d.完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V(NaOH)<V(氨水)
(4)甲醇是一种可再生能源,具有广泛的开发和应用前景。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.

II.

III.

回答下列问题:
①
___________ 
②若体系中只发生反应I,请写出反应I的化学平衡常数表达式,K=___________ ;保持恒温恒容,将反应I的平衡体系中各物质浓度均增大为原来的2倍,则化学平衡___________ (填“正向逆向”或“逆向”或“不”)移动,平衡常数K___________ (填“变大”“变小”或“不变”)。
③常温下,某一元弱酸HA的部分组分平衡浓度如下,
平衡浓度 V (a+b)1/2
计算出一元弱酸HA电离平衡常数Ka=___________ (用含a、b、V的代数式表示计算结果)
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
(1)试比较K1、K2的大小,K1
(2)400℃时,反应
(3)某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。根据图像判断下列说法错误的是

a.a值一定大于9
b.II为氨水稀释时溶液的pH变化曲线
c.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
d.完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V(NaOH)<V(氨水)
(4)甲醇是一种可再生能源,具有广泛的开发和应用前景。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.
II.
III.
回答下列问题:
①
②若体系中只发生反应I,请写出反应I的化学平衡常数表达式,K=
③常温下,某一元弱酸HA的部分组分平衡浓度如下,
HA⇌A-+H+
平衡浓度 V (a+b)1/2
计算出一元弱酸HA电离平衡常数Ka=
22-23高二上·福建·期中
类题推荐
氮及其化合物在工农业生产、生活中有着重要作用。合成氨工业中:
 ,其化学平衡常数K与温度t的关系如表:
,其化学平衡常数K与温度t的关系如表:
完成下列填空:
(1)试比较 、
、 的大小,
的大小,
_______  (填写“>”、“=”或“<”)。
(填写“>”、“=”或“<”)。
(2)400℃时,反应 的化学平衡常数的值为
的化学平衡常数的值为_______ 。当测得 和
和 、
、 的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则该反应
的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则该反应
_______  (填写“>”、“=”或“<”)。
(填写“>”、“=”或“<”)。
(3)在密闭恒容的容器中,下列能作为合成氨反应达到平衡的依据的是_______ 。
a. b.混合气体的密度保持不变
b.混合气体的密度保持不变
c.容器内压强保持不变 d. 、
、 、
、 的浓度之比为1:3:2
的浓度之比为1:3:2
(4)甲醇是一种可再生能源,具有广泛的开发和应用前景。以 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:④

_______  。
。
②若体系中只发生反应Ⅰ,请写出反应Ⅰ的化学平衡常数表达式:K=_______ ;保持恒温恒容,将反应Ⅰ的平衡体系中各物质浓度均增大为原来的2倍,则化学平衡_______ (填“正向”“逆向”或“不”)移动,平衡常数K_______ (填“变大”“变小”或“不变”)。
③一定条件下,向体积为VL的恒容密闭容器中通入1mol 和3mol
和3mol 同时发生Ⅰ、Ⅱ、Ⅲ反应,达到平衡时,容器中
同时发生Ⅰ、Ⅱ、Ⅲ反应,达到平衡时,容器中 为amol,CO为bmol,此时
为amol,CO为bmol,此时 的浓度为
的浓度为_______  (用含a、b、V的代数式表示)
(用含a、b、V的代数式表示)
| t/℃ | 200 | 300 | 400 |
| K | 0.5 |
(1)试比较
(2)400℃时,反应
(3)在密闭恒容的容器中,下列能作为合成氨反应达到平衡的依据的是
a.
c.容器内压强保持不变 d.
(4)甲醇是一种可再生能源,具有广泛的开发和应用前景。以
Ⅰ.
Ⅱ.
Ⅲ.
回答下列问题:④
②若体系中只发生反应Ⅰ,请写出反应Ⅰ的化学平衡常数表达式:K=
③一定条件下,向体积为VL的恒容密闭容器中通入1mol
氮及其化合物在工农业生产、生活中有着重要作用。合成氨工业中: N2+ 3H2⇌2NH3 ΔH<0,其化学平衡常数K与温度t的关系如表:
完成下列填空:
(1)试比较K1、K2的大小,K1_______ K2(填写“>”、“=”或“<”)
(2)400℃时,反应2NH3⇌N2+3H2的化学平衡常数的值为_______ 。当测得NH3和N2、H2的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则该反应v(N2)(正)_______ v(N2)(逆)(填写“>”、“=”或“<”)
(3)在密闭恒容的容器中,下列能作为合成氨反应达到平衡的依据的是_______ 。
a.v(N2)(正)=3v(H2)(逆)
b.混合气体的密度保持不变
c.容器内压强保持不变
d.N2、H2、NH3的浓度之比为1:3:2
(4)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。写出该反应的化学平衡常数表达式:K=_______ ;保持恒温恒容,将反应的平衡体系中各物质浓度均增大为原来的2倍,则化学平衡_______ (填“正向”逆向”或“不”)移动,平衡常数K_______ (填“变大”变小”或“不变”)。
| t/℃ | 200 | 300 | 400 | |
| K | K1 | K2 | 0.5 |
(1)试比较K1、K2的大小,K1
(2)400℃时,反应2NH3⇌N2+3H2的化学平衡常数的值为
(3)在密闭恒容的容器中,下列能作为合成氨反应达到平衡的依据的是
a.v(N2)(正)=3v(H2)(逆)
b.混合气体的密度保持不变
c.容器内压强保持不变
d.N2、H2、NH3的浓度之比为1:3:2
(4)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。写出该反应的化学平衡常数表达式:K=
高中化学涉及的平衡理论主要包括化学平衡、电离平衡、水解平衡和沉淀溶解平衡等,它们在工农业生产中都有广泛的应用,请回答下列问题:
(1)氮及其化合物在工农业生产、生活中有着重要作用。合成氨工业中:N2(g)+3H2(g) 2NH3(g) ΔH<0,其化学平衡常数K与温度t的关系如表:
2NH3(g) ΔH<0,其化学平衡常数K与温度t的关系如表:
完成下列填空:
①试比较K1、K2的大小,K1_______ K2(填写“>”、“=”或“<”)。
②将1molN2和1molH2投到一个温度恒定、体积恒定的容器中进行上述反应,一段时间后可判断该可逆反应达到化学平衡状态的标志是_______ (填字母)。
A.v正(NH3)=2v速(N2) B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变 D.N2的体积分数不再改变
(2)磷是重要的元素,能形成多种含氧酸和含氧酸盐。亚磷酸(H3PO3)的结构如图: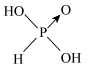 ,亚磷酸可由PCl3水解而成,H3PO3溶液存在电离平衡:H3PO3
,亚磷酸可由PCl3水解而成,H3PO3溶液存在电离平衡:H3PO3 H++H2PO
H++H2PO ,H2PO
,H2PO
 H++HPO
H++HPO ,回答下列问题:
,回答下列问题:
①Na2HPO3属于_______ (填“正盐”或“酸式盐”)。
②已知25C时,1molL的H3PO3溶液的电离度为α,H3PO3的一级电离平衡常数Ka1=_______ (用含α的计算式表示,H3PO3第二步电离忽略不计,忽略水的电离)。
③常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示 的是曲线
的是曲线_______ (填“I”或“Ⅱ”),亚磷酸(H3PO3)的Ka2=_______ 。
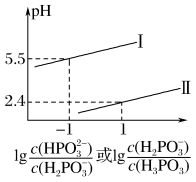
④请结合相关平衡常数说明0.1mol·L-1NaH2PO3的酸碱性:_______ ,常温下,0.1 mol·L-1Na2HPO3的水解平衡常数Kh1=_______ 。
(1)氮及其化合物在工农业生产、生活中有着重要作用。合成氨工业中:N2(g)+3H2(g)
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
完成下列填空:
①试比较K1、K2的大小,K1
②将1molN2和1molH2投到一个温度恒定、体积恒定的容器中进行上述反应,一段时间后可判断该可逆反应达到化学平衡状态的标志是
A.v正(NH3)=2v速(N2) B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变 D.N2的体积分数不再改变
(2)磷是重要的元素,能形成多种含氧酸和含氧酸盐。亚磷酸(H3PO3)的结构如图:
 ,亚磷酸可由PCl3水解而成,H3PO3溶液存在电离平衡:H3PO3
,亚磷酸可由PCl3水解而成,H3PO3溶液存在电离平衡:H3PO3①Na2HPO3属于
②已知25C时,1molL的H3PO3溶液的电离度为α,H3PO3的一级电离平衡常数Ka1=
③常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示

④请结合相关平衡常数说明0.1mol·L-1NaH2PO3的酸碱性:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


