解答题-原理综合题 较难0.4 引用2 组卷222
Fe、Co、Cu等金属在回收利用 和污水处理等多个领域都具有应用价值。回答下列问题:
和污水处理等多个领域都具有应用价值。回答下列问题:
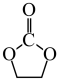
(1) 在金属催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
在金属催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
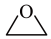 (g)+CO2(g)+3H2(g)⇌HOCH2CH2OH(g)+CH3OH(g)
(g)+CO2(g)+3H2(g)⇌HOCH2CH2OH(g)+CH3OH(g) 


获取乙二醇的反应历程可分为如下2步:
I.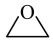

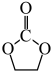 (g)
(g) 
II.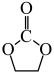 加氢生成乙二醇与甲醇。
加氢生成乙二醇与甲醇。
①步骤II的热化学方程式是:_______ 。
②研究反应温度对EC加氢的影响(反应时间均为 ),实验数据见下表:
),实验数据见下表:
由上表可知,温度越高,EC的转化率越高,原因是_______ 。温度升高到220℃时,乙二醇的产率反而降低,原因是_______ 。
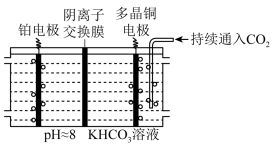
(2)多晶 是目前唯一被实验证实能高效催化
是目前唯一被实验证实能高效催化 还原为烃类(如
还原为烃类(如 )的金属。如图所示,电解装置中分别以多晶
)的金属。如图所示,电解装置中分别以多晶 和
和 为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后
为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后 浓度基本保持不变,温度控制在10℃左右,生成
浓度基本保持不变,温度控制在10℃左右,生成 的电极反应式为
的电极反应式为_______ 。
(3) 与
与 反应如果用
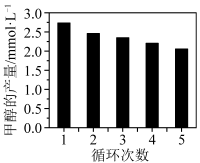
反应如果用 作为催化剂,可以得到含有少量甲酸的甲醇。为研究催化剂的催化效率,将
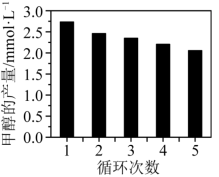
作为催化剂,可以得到含有少量甲酸的甲醇。为研究催化剂的催化效率,将 催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇产量如图所示,试推测甲醇产量变化的原因:
催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇产量如图所示,试推测甲醇产量变化的原因:_______ 。(Co的性质与 相似)
相似)
(4)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图所示。
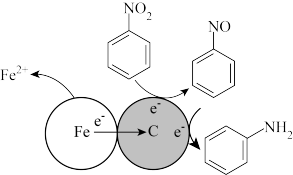
该物质转化示意图可以描述为_______ 。
(1)
 (g)+CO2(g)+3H2(g)⇌HOCH2CH2OH(g)+CH3OH(g)
(g)+CO2(g)+3H2(g)⇌HOCH2CH2OH(g)+CH3OH(g) 获取乙二醇的反应历程可分为如下2步:
I.

 (g)
(g) II.
 加氢生成乙二醇与甲醇。
加氢生成乙二醇与甲醇。①步骤II的热化学方程式是:
②研究反应温度对EC加氢的影响(反应时间均为
| 反应温度/℃ | 乙二醇的产率/% | |
| 160 | 23.8 | 23.2 |
| 180 | 62.1 | 60.9 |
| 200 | 99.9 | 94.7 |
| 220 | 99.9 | 92.4 |
(2)多晶

(3)

(4)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图所示。

该物质转化示意图可以描述为
23-24高三上·江苏镇江·阶段练习
类题推荐
CO2的利用是国际社会普遍关注的问题。
(1)CO2的电子式是______ 。
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。______ 。
②研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
由上表可知,温度越高,EC的转化率越高,原因是______ 。温度升高到220 ℃时,乙二醇的产率反而降低,原因是______ 。
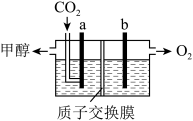
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源的______ 极(填“正”或“负”),生成甲醇的电极反应式是______ 。______ (填序号)。
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
(1)CO2的电子式是
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
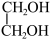 (g)+H2(g)
(g)+H2(g)C2H5OH(g)+H2(g)
H=-94.8kJ·mol-1
Ⅰ. (g)+CO2(g)
(g)+CO2(g)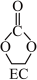 (g)
(g) H=-60.3kJ·mol-1
 (g)+CO2(g)+3H2(g)
(g)+CO2(g)+3H2(g) (g)+CH3OH(g)
(g)+CH3OH(g) H=-131.9kJ·mol-1
②研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
| 反应温度/ ℃ | EC转化率/ % | 产率/ % | |
| 乙二醇 | 甲醇 | ||
| 160 | 23.8 | 23.2 | 12.9 |
| 180 | 62.1 | 60.9 | 31.5 |
| 200 | 99.9 | 94.7 | 62.3 |
| 220 | 99.9 | 92.4 | 46.1 |
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源的
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
CO2的利用是国际社会普遍关注的问题。
(1)CO2的电子式是___________ 。
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
 (g)+CO2(g)+3H2(g)→
(g)+CO2(g)+3H2(g)→ (g)+CH3OH(g) ∆H=-131.9kJ∙mol-1
(g)+CH3OH(g) ∆H=-131.9kJ∙mol-1
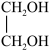 (g)+H2(g)→C2H5OH(g)+H2O(g) ∆H=-94.8kJ∙mol-1
(g)+H2(g)→C2H5OH(g)+H2O(g) ∆H=-94.8kJ∙mol-1
获取乙二醇的反应历程可分为如下2步:
I.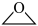 (g)+CO2(g)→
(g)+CO2(g)→ (g) ∆H=-60.3kJ∙mol-1
(g) ∆H=-60.3kJ∙mol-1
II.EC加氢生成乙二醇与甲醇
①步骤II的热化学方程式是___________ 。
②研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
由上表可知,温度越高,EC的转化率越高,原因是___________ 。温度升高到220℃时,乙二醇的产率反而降低,原因是___________ 。
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源___________ 极(填“正”或“负”),生成甲醇的电极反应式是___________ 。

(4)CO2较稳定、能量低。为实现CO2的化学利用,下列研究方向合理的是___________
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
(1)CO2的电子式是
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
 (g)+CO2(g)+3H2(g)→
(g)+CO2(g)+3H2(g)→ (g)+CH3OH(g) ∆H=-131.9kJ∙mol-1
(g)+CH3OH(g) ∆H=-131.9kJ∙mol-1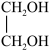 (g)+H2(g)→C2H5OH(g)+H2O(g) ∆H=-94.8kJ∙mol-1
(g)+H2(g)→C2H5OH(g)+H2O(g) ∆H=-94.8kJ∙mol-1获取乙二醇的反应历程可分为如下2步:
I.
 (g)+CO2(g)→
(g)+CO2(g)→ (g) ∆H=-60.3kJ∙mol-1
(g) ∆H=-60.3kJ∙mol-1II.EC加氢生成乙二醇与甲醇
①步骤II的热化学方程式是
②研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
| 反应温度/℃ | EC转化率/% | 产率/% | |
| 乙二醇 | 甲醇 | ||
| 160 | 23.8 | 23.2 | 12.9 |
| 180 | 62.1 | 60.9 | 31.5 |
| 200 | 99.9 | 94.7 | 62.3 |
| 220 | 99.9 | 92.4 | 46.1 |
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源

(4)CO2较稳定、能量低。为实现CO2的化学利用,下列研究方向合理的是
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
空气中 含量的控制和
含量的控制和 资源化利用具有重要意义。
资源化利用具有重要意义。
Ⅰ. 在金属催化剂作用下可转化为乙二醇和甲醇;若反应温度过高,乙二醇会深度加氢生成乙醇。
在金属催化剂作用下可转化为乙二醇和甲醇;若反应温度过高,乙二醇会深度加氢生成乙醇。

获取乙二醇的反应历程分为如下2步:
_______ 。
(2)研究反应温度对步骤2加氢反应的影响(反应时间均为4h),实验数据见下表:
 ”电池将
”电池将 变废为宝。我国科研人员研制出的可充电“Na-
变废为宝。我国科研人员研制出的可充电“Na- ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为
”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为 。
。
放电时该电池“吸入” ,生成
,生成 和C全部沉积在电极表面。其工作原理如图所示:
和C全部沉积在电极表面。其工作原理如图所示:_______ (填“钠箔”或“MWCNT”)。
(4)放电时,正极的电极反应式为_______ 。 -四甘醇二甲醚作电解液的优点是
-四甘醇二甲醚作电解液的优点是_______ (写出两点)。
Ⅲ. 与
与 反应如果用Co/C作为催化剂,可以得到含有少量甲酸的甲醇。
反应如果用Co/C作为催化剂,可以得到含有少量甲酸的甲醇。
(5)在相同条件下,将Co/C催化剂循环使用,随着循环使用次数增加,甲醇产量如图所示,试推测甲醇产量变化的原因:_______ (Co的性质与Fe相似)。
Ⅰ.
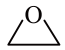
获取乙二醇的反应历程分为如下2步:
步骤1 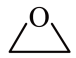
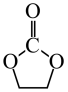
步骤2 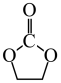
(2)研究反应温度对步骤2加氢反应的影响(反应时间均为4h),实验数据见下表:
反应温度/℃ |
| 乙二醇的产率/% |
160 | 23.8 | 23.2 |
180 | 62.1 | 60.9 |
200 | 99.9 | 94.7 |
220 | 99.9 | 92.4 |
由上表可知,温度越高,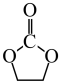 的转化率越高,原因是
的转化率越高,原因是
放电时该电池“吸入”
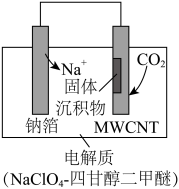
(4)放电时,正极的电极反应式为
Ⅲ.
(5)在相同条件下,将Co/C催化剂循环使用,随着循环使用次数增加,甲醇产量如图所示,试推测甲醇产量变化的原因:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 的转化率/%
的转化率/%

