单选题 适中0.65 引用1 组卷166
焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。利用烟道气中的SO2生产Na2S2O5的工艺为:
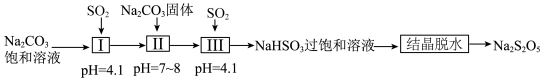
下列对I、II、III中主要发生反应的离子方程式判断错误的是

| 弱电解质 | 电离常数 |
| H2CO3 | Ka1=4.5×10-7,Ka2=4.7×10-11 |
| H2SO3 | Ka1=1.4×10-2,Ka2=6.0×10-8 |
| A.I中 |
| B.II中 |
| C.III中 |
| D.III中 |
22-23高二下·河北沧州·阶段练习
类题推荐
已知部分弱酸的电离平衡常数如下表所示:
下列实验的反应原理用离子方程式表示不正确的是
| 弱酸 | 次氯酸 | 碳酸 | 亚硫酸 | 苯酚 |
| 电离平衡常数Ka(25℃) | 2.98×10-8 | Ka1=4.3×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 | 1.28×10-10 |
下列实验的反应原理用离子方程式表示不正确的是
| A.少量的SO2通入Na2CO3溶液中:SO2+H2O+2 |
B.用碳酸氢钠溶液检验水杨酸中的羧基: + +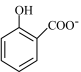 +H2O+CO2↑ +H2O+CO2↑ |
| C.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-==CaSO3↓+2HClO |
D.少量的SO2通入苯酚钠溶液中:SO2+H2O+2  →2 →2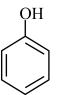 + SO32- + SO32- |
已知部分弱酸的电离平衡常数如表所示:
下列离子方程式正确的是
| 弱酸 | CH3COOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka=1.80×10-5 | Ka=2.95×10-8 | Ka1=4.30×10-7 Ka2=5.60×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
| A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-= |
| B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
| C.少量SO2通入Na2CO3溶液中:SO2+H2O+2 |
| D.相同浓度的NaHCO3溶液与NaHSO3溶液等体积混合:H++ |
下列离子方程式书写正确的是
| A.氢氧化钙溶液与碳酸氢镁溶液反应: |
| B.[Ag(NH3)2]OH与足量盐酸反应:[Ag(NH3)2]++OH-+3H++C1-=AgCl↓+2 |
| C.用铁作电极电解氯化钠溶液:2Cl-+2H2O |
| D.向Na2S溶液中通入少量SO2:S2-+SO2+H2O= |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


