解答题-原理综合题 适中0.65 引用1 组卷37
化学反应过程伴随有热量的变化。
(1)下列反应中属于放热反应的有___________ 。
①燃烧木炭取暖 ②C与H2O(g)反应制取水煤气 ③煅烧石灰石(主要成分是CaCO3)制生石灰 ④氯化铵晶体和Ba(OH)2·8H2O混合搅拌 ⑤食物因氧化而腐败 ⑥盐酸与NaOH溶液反应 ⑦镁与稀硫酸溶液反应
(2)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
①已知2CH4(g)=C2H4(g)+2H2(g),其中1mol C2H4中存在1mol C=C和4mol C-H键,已知每生成1 mol H2反应吸收83.5 kJ热量,则a=___________ 。
②已知5SO2(g)+2 (aq)+2H2O(l)=2Mn2+(aq)+5
(aq)+2H2O(l)=2Mn2+(aq)+5 (aq)+4H+(aq),每1 mol SO2参加反应放出热量m kJ,那么当放出的热量为n kJ时,该反应转移的电子数为
(aq)+4H+(aq),每1 mol SO2参加反应放出热量m kJ,那么当放出的热量为n kJ时,该反应转移的电子数为___________ 。(用含m、n的代数式表示,NA为阿伏加德罗常数的值。)
(3)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:

①该反应为___________ (填“吸热”或“放热”)反应。
②若要使该反应的反应速率增大,下列措施可行的是___________ (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度 D.使用催化剂
(4)若将上述反应设计成原电池,则化学反应速率会___________ (填“变大”或“变小”)
铜为原电池某一极材料,则铜为:___________ (填“正”或“负”)极,该极上发生的电极反应为:___________ 。
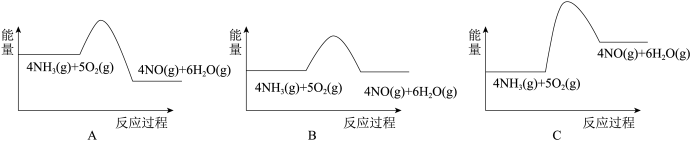
(5)关于氨气的催化氧化反应,先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达700 ℃以上。下列图示中,能够正确表示该反应过程中能量变化的是___________ (填序号),说明断键吸收的能量___________ (填“大于”“小于”或“等于”)成键放出的能量。
(1)下列反应中属于放热反应的有
①燃烧木炭取暖 ②C与H2O(g)反应制取水煤气 ③煅烧石灰石(主要成分是CaCO3)制生石灰 ④氯化铵晶体和Ba(OH)2·8H2O混合搅拌 ⑤食物因氧化而腐败 ⑥盐酸与NaOH溶液反应 ⑦镁与稀硫酸溶液反应
(2)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
②已知5SO2(g)+2
(3)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:

①该反应为
②若要使该反应的反应速率增大,下列措施可行的是
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度 D.使用催化剂
(4)若将上述反应设计成原电池,则化学反应速率会
铜为原电池某一极材料,则铜为:
(5)关于氨气的催化氧化反应,先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达700 ℃以上。下列图示中,能够正确表示该反应过程中能量变化的是

22-23高一下·黑龙江佳木斯·期末
类题推荐
化学反应过程伴随有热量的变化。
(1)下列反应中属于吸热反应的有_______ 。
①燃烧木炭取暖 ②C与H2O(g)反应制取水煤气 ③煅烧石灰石(主要成分是CaCO3)制生石灰④氯化铵晶体和Ba(OH)2·8H2O混合搅拌 ⑤食物因氧化而腐败
(2)一定条件下,由稳定单质反应生成1 mol化合物的反应热叫该化合物的生成热(ΔH)。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。
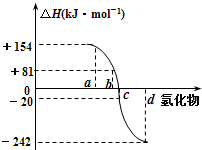
①非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系为______ 。
②硫化氢发生分解反应的热化学方程式为_____________ 。
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
①已知2CH4(g) = C2H4(g) + 2H2(g) ΔH= +167 kJ/mol,则a=____ 。
②已知5C2H4(g)+12MnO (aq)+36H+(aq)=12Mn2+ (aq)+10CO2(g)+28H2O(l) ΔH= —m kJ·mol-1,当放出的热量为n kJ时,该反应转移的电子数为
(aq)+36H+(aq)=12Mn2+ (aq)+10CO2(g)+28H2O(l) ΔH= —m kJ·mol-1,当放出的热量为n kJ时,该反应转移的电子数为________ 。(用含m、n的代数式表示)
③ 制备合成气反应历程分两步,步骤 Ⅰ:CH4(g) C(ads) +2H2(g);步骤Ⅱ:C(ads) + CO2(g)
C(ads) +2H2(g);步骤Ⅱ:C(ads) + CO2(g) 2CO(g)。上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
2CO(g)。上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
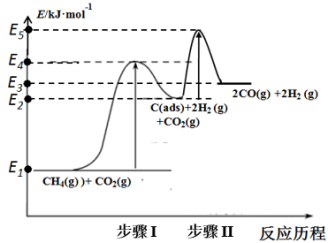
E4 – E1表示步骤①正反应的__________ ,决定制备合成气反应速率的是_________ (填“步骤 Ⅰ”或“步骤Ⅱ”);该反应可在___________ (填“高温”或“低温”)下自发进行。
(1)下列反应中属于吸热反应的有
①燃烧木炭取暖 ②C与H2O(g)反应制取水煤气 ③煅烧石灰石(主要成分是CaCO3)制生石灰④氯化铵晶体和Ba(OH)2·8H2O混合搅拌 ⑤食物因氧化而腐败
(2)一定条件下,由稳定单质反应生成1 mol化合物的反应热叫该化合物的生成热(ΔH)。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。

①非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系为
②硫化氢发生分解反应的热化学方程式为
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
①已知2CH4(g) = C2H4(g) + 2H2(g) ΔH= +167 kJ/mol,则a=
②已知5C2H4(g)+12MnO
③ 制备合成气反应历程分两步,步骤 Ⅰ:CH4(g)

E4 – E1表示步骤①正反应的
化学反应过程伴随有热量的变化。
(1)下列过程中属于放热反应的有___________ 。
①燃烧木炭取暖②C与H2O(g)反应制取水煤气③煅烧石灰石(主要成分是CaCO3)制生石灰④氯化铵晶体和Ba(OH)2·8H2O混合搅拌⑤金属腐蚀⑥浓硫酸稀释
(2)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热(ΔH)。图为VIA族元素(O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。
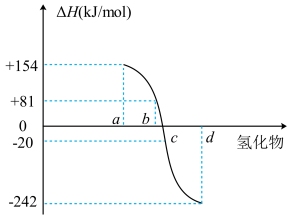
①非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系为___________ 。
②硫化氢发生分解反应的热化学方程式为___________ 。
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
①已知2CH4(g)=CH2=CH2(g)+2H2(g) ΔH=+167kJ/mol,则a=___________ 。
②已知5C2H4(g)+12MnO (aq)+36H+(aq)=12Mn2+(aq)+10CO2(g)+28H2O(l) ΔH=-mkJ·mol-1,当放出的热量为nkJ时,该反应转移的电子数为
(aq)+36H+(aq)=12Mn2+(aq)+10CO2(g)+28H2O(l) ΔH=-mkJ·mol-1,当放出的热量为nkJ时,该反应转移的电子数为___________ 。(用含m、n的代数式表示)
③制备合成气反应历程分两步(步骤I、步骤II),反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
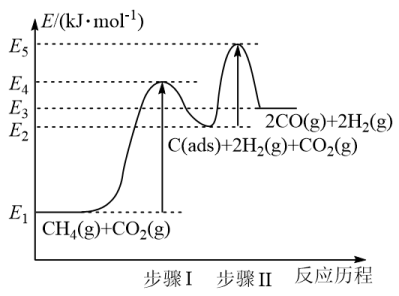
步骤I反应的焓变ΔH1为___________ kJ/mol(选用E1~E5的关系式表示)
④反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的焓变为ΔH2,与步骤Ⅰ反应的焓变ΔH1相比,ΔH1___________ ΔH2(填“>”或“<”)
(1)下列过程中属于放热反应的有
①燃烧木炭取暖②C与H2O(g)反应制取水煤气③煅烧石灰石(主要成分是CaCO3)制生石灰④氯化铵晶体和Ba(OH)2·8H2O混合搅拌⑤金属腐蚀⑥浓硫酸稀释
(2)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热(ΔH)。图为VIA族元素(O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。

①非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系为
②硫化氢发生分解反应的热化学方程式为
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
②已知5C2H4(g)+12MnO
③制备合成气反应历程分两步(步骤I、步骤II),反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:

步骤I反应的焓变ΔH1为
④反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的焓变为ΔH2,与步骤Ⅰ反应的焓变ΔH1相比,ΔH1
某同学利用如图装置模拟工业生产制备了少量硝酸,请结合所学知识完成下列问题。
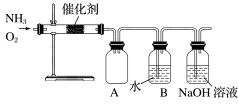
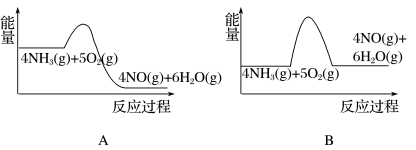
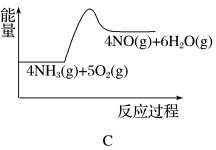
(1)实验时先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到 700℃以上。下列图示中,能够正确表示该反应过程能量变化的是_____ (填字母)。
(2)高温时,2NO2(g)⇌ 2NO(g)+O2(g),因此氨气与氧气反应难以生成 NO2 。根据下列数据计算,当 4molNO2 分解时,反应会________________ (填“吸收”或 “放出”)_____________________ kJ 能量。
NO2(g)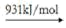 N(g)+2O(g)
N(g)+2O(g)
NO(g)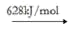 N(g)+O(g)
N(g)+O(g)
O2(g)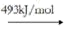 2O(g)
2O(g)
(3)在 2L 的恒温密闭容器中,通入等物质的量的 NO 和 O2 气体,n(NO)随时间的变化如下表:
①反应开始至第 1s 时,NO 的平均反应速率为_____ 。
②在第 5s 时,O2的转化率为_____ 。
③容器中混合气体压强与反应开始时的压强比值为_____ 。
④下列能说明反应已达平衡的是_____ 。
a.单位时间内,每生成一定物质的量浓度的 NO,同时有相同物质的量浓度的O2生成
b.气体混合物物质的量不再改变
c.气体混合物平均相对分子质量不再改变
d.容器内温度不再发生变化
e.密闭容器内气体颜色不再改变
f.混合气的密度不再改变

(1)实验时先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到 700℃以上。下列图示中,能够正确表示该反应过程能量变化的是


(2)高温时,2NO2(g)⇌ 2NO(g)+O2(g),因此氨气与氧气反应难以生成 NO2 。根据下列数据计算,当 4molNO2 分解时,反应会
NO2(g)
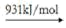 N(g)+2O(g)
N(g)+2O(g)NO(g)
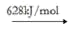 N(g)+O(g)
N(g)+O(g)O2(g)
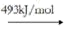 2O(g)
2O(g)(3)在 2L 的恒温密闭容器中,通入等物质的量的 NO 和 O2 气体,n(NO)随时间的变化如下表:
| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0 014 | 0.010 | 0.007 | 0.006 | 0.006 |
①反应开始至第 1s 时,NO 的平均反应速率为
②在第 5s 时,O2的转化率为
③容器中混合气体压强与反应开始时的压强比值为
④下列能说明反应已达平衡的是
a.单位时间内,每生成一定物质的量浓度的 NO,同时有相同物质的量浓度的O2生成
b.气体混合物物质的量不再改变
c.气体混合物平均相对分子质量不再改变
d.容器内温度不再发生变化
e.密闭容器内气体颜色不再改变
f.混合气的密度不再改变
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


