解答题-原理综合题 适中0.65 引用1 组卷131
碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)查阅资料得知,反应 在含有少量
在含有少量 的溶液中分两步进行:第I步反应为
的溶液中分两步进行:第I步反应为 (慢反应),第II步为快反应。增大
(慢反应),第II步为快反应。增大 的浓度
的浓度___________ (填“能”或“不能”)明显增大总反应的平均速率,理由为______________________________ 。
(2)用催化剂 催化
催化 加氢合成乙烯的反应,所得产物含
加氢合成乙烯的反应,所得产物含 、
、 、
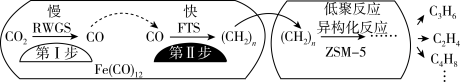
、 等副产物,反应过程如图。
等副产物,反应过程如图。
催化剂中添加 、K、
、K、 助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得
助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得 转化率和各产物的物质的量分数如表。
转化率和各产物的物质的量分数如表。
欲提高单位时间内乙烯的产量,在 中添加
中添加__________ 助剂效果最好;加入助剂能提高单位时间内乙烯产量的根本原因是__________ 。
a.明显降低了该体系中所有反应的活化能
b.降低了生成乙烯反应的焓变值使反应趋势增大
c.降低了 转化率
转化率
d.明显降低了生成乙烯反应的活化能,对其他反应几乎无影响
(3)在一密闭容器中,起始时向该容器中充入 和
和 且
且 2:1,发生反应:
2:1,发生反应:
 。0.11
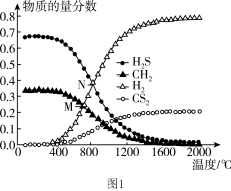
。0.11 时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高
时,温度变化对平衡时产物的物质的量分数的影响如图1所示:为提高 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是__________ (列举一条)。
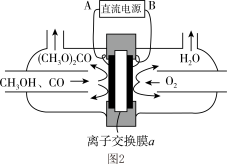
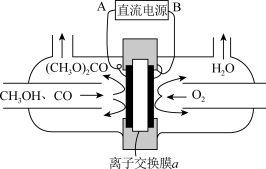
(4)合成碳酸二甲酯的工作原理如图2所示。阳极的电极反应式为__________ ,离子交换膜a为__________ (填“阳膜”、“阴膜”)。
(1)查阅资料得知,反应
(2)用催化剂

催化剂中添加
助剂 |
| 各产物在所有产物中的占比(%) | ||
其他 | ||||
42.5 | 35.9 | 39.6 | 24.5 | |
K | 27.2 | 75.6 | 22.8 | 1.6 |
9.8 | 80.7 | 12.5 | 6.8 | |
a.明显降低了该体系中所有反应的活化能
b.降低了生成乙烯反应的焓变值使反应趋势增大
c.降低了
d.明显降低了生成乙烯反应的活化能,对其他反应几乎无影响
(3)在一密闭容器中,起始时向该容器中充入

(4)合成碳酸二甲酯的工作原理如图2所示。阳极的电极反应式为

22-23高二上·福建宁德·阶段练习
类题推荐
碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+ Cl2(g)=CH2ClCHClCH3(g) ΔH1=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2= CHCH2Cl(g)+HCl(g) ΔH2 = -100 kJ·mol-1
又已知在相同条件下,CH2=CHCH2Cl(g)+ HCl(g)=CH2ClCHClCH3(g) ΔH3的逆反应的活化能Ea(逆)为165 kJ·mol-1,则正反应的活化能Ea (正)为______ kJ·mol-1
(2)查阅资料得知:反应CH3CHO(aq)=CH4(g)+CO(g)在含少量I2的溶液中分两步进行:
第I步反应为:CH3CHO(aq)+I2(aq)→CH3(l)+HI(aq)+CO(g) (慢反应)
第II步为快反应,增大I2的浓度能明显增大总反应的平均速率,理由为______ 。
(3)用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。

在其他条件相同时,催化剂中添加不同Na、K、Cu助剂(助剂也起催化作用)经过相同时间后测得CO2转化率和各产物的物质的量分数如表。
由以上信息可知:在催化剂中添加不同的助剂可改变反应的______ 性,欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加 ______ 助剂效果最好。
(4)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应:CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。0.11 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:

为提高H2S的平衡转化率,除改变温度外,还可采取的措施是______ (列举一条)。N点对应温度下,该反应的Kp=______ (MPa)2(Kp为以分压表示的平衡常数)
(5)合成碳酸二甲酯的工作原理如图所示。阳极的电极反应式为______ 。

(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+ Cl2(g)=CH2ClCHClCH3(g) ΔH1=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2= CHCH2Cl(g)+HCl(g) ΔH2 = -100 kJ·mol-1
又已知在相同条件下,CH2=CHCH2Cl(g)+ HCl(g)=CH2ClCHClCH3(g) ΔH3的逆反应的活化能Ea(逆)为165 kJ·mol-1,则正反应的活化能Ea (正)为
(2)查阅资料得知:反应CH3CHO(aq)=CH4(g)+CO(g)在含少量I2的溶液中分两步进行:
第I步反应为:CH3CHO(aq)+I2(aq)→CH3(l)+HI(aq)+CO(g) (慢反应)
第II步为快反应,增大I2的浓度能明显增大总反应的平均速率,理由为
(3)用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。

在其他条件相同时,催化剂中添加不同Na、K、Cu助剂(助剂也起催化作用)经过相同时间后测得CO2转化率和各产物的物质的量分数如表。
| 助剂 | CO2转化率(%) | 各产物在所有产物中的占比(%) | ||
| C2H4 | C3H6 | 其他 | ||
| Na | 42.5 | 35.9 | 39.6 | 24.5 |
| K | 27.2 | 75.6 | 22.8 | 1.6 |
| Cu | 9.8 | 80.7 | 12.5 | 6.8 |
由以上信息可知:在催化剂中添加不同的助剂可改变反应的
(4)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应:CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。0.11 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:

为提高H2S的平衡转化率,除改变温度外,还可采取的措施是
(5)合成碳酸二甲酯的工作原理如图所示。阳极的电极反应式为

碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+Cl2(g)=CH2ClCHClCH3(g) ΔH1=-133kJ∙mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2=CHCH2Cl(g)+HCl(g) ΔH2=-100kJ∙mol-1
又已知在相同条件下,CH2=CHCH2Cl(g)+ HCl(g)=CH2ClCHClCH3(g) ΔH3的逆反应的活化能Ea(逆)为165kJ∙mol-1,则正反应的活化能Ea (正)为_______ kJ∙mol-1。
(2)查阅资料得知:反应CH3CHO(aq)=CH4(g)+CO(g)在含少量I2的溶液中分两步进行:
第I步反应为:CH3CHO(aq)+I2(aq)→CH3(l)+HI(aq)+CO(g) (慢反应)
第II步为快反应,增大I2的浓度能明显增大总反应的平均速率,理由为_______ 。
(3)用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物。在其他条件相同时,催化剂中添加不同Na、K、Cu助剂(助剂也起催化作用)经过相同时间后测得CO2转化率和各产物的物质的量分数如表。
由信息可知:在催化剂中添加不同的助剂可改变反应的_______ 性,欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加_______ 助剂效果最好。
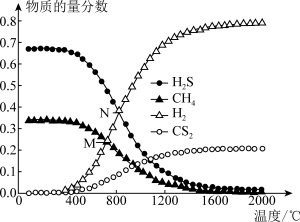
(4)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S)∶n(CH4)=2∶1,发生反应:CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示,N点对应温度下,该反应的Kp=_______ (MPa)2。
(5)合成碳酸二甲酯的工作原理如图所示,阳极的电极反应式为_______ 。
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+Cl2(g)=CH2ClCHClCH3(g) ΔH1=-133kJ∙mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2=CHCH2Cl(g)+HCl(g) ΔH2=-100kJ∙mol-1
又已知在相同条件下,CH2=CHCH2Cl(g)+ HCl(g)=CH2ClCHClCH3(g) ΔH3的逆反应的活化能Ea(逆)为165kJ∙mol-1,则正反应的活化能Ea (正)为
(2)查阅资料得知:反应CH3CHO(aq)=CH4(g)+CO(g)在含少量I2的溶液中分两步进行:
第I步反应为:CH3CHO(aq)+I2(aq)→CH3(l)+HI(aq)+CO(g) (慢反应)
第II步为快反应,增大I2的浓度能明显增大总反应的平均速率,理由为
(3)用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物。在其他条件相同时,催化剂中添加不同Na、K、Cu助剂(助剂也起催化作用)经过相同时间后测得CO2转化率和各产物的物质的量分数如表。
| 助剂 | CO2转化率(%) | 各产物在所有产物中的占比(%) | ||
| C2H4 | C3H6 | 其他 | ||
| Na | 42.5 | 35.9 | 39.6 | 24.5 |
| K | 27.2 | 75.6 | 22.8 | 1.6 |
| Cu | 9.8 | 80.7 | 12.5 | 6.8 |
(4)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S)∶n(CH4)=2∶1,发生反应:CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示,N点对应温度下,该反应的Kp=

(5)合成碳酸二甲酯的工作原理如图所示,阳极的电极反应式为

碳的化合物在工业上应用广泛,下面有几种碳的化合物的应用:
(1)正戊烷异构化为异戊烷是油品升级的一项重要技术。正戊烷和异戊烷的部分性质如表:
由表中数据可知,稳定性:正戊烷_______ 异戊烷(填“>”或“=”或“<”)。
(2)用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物。催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表:
欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加_______ 助剂效果最好;从活化能对反应影响的角度说明加入该助剂能提高单位时间内乙烯产量的根本原因是_______ 。
(3)在密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应:CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如图甲所示:
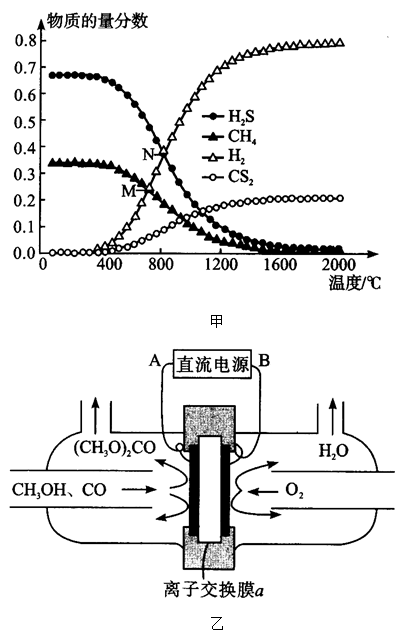
为提高H2S的平衡转化率,除改变温度外,还可采取的措施是____ (列举一条)。N点对应温度下,该反应的Kp=___ (MPa)2(Kp为以分压表示的平衡常数)。
(4)合成碳酸二甲酯的工作原理如图乙所示。阳极的电极反应式为__ ,离子交换膜a为___ (填“阳膜”、“阴膜”)。
(1)正戊烷异构化为异戊烷是油品升级的一项重要技术。正戊烷和异戊烷的部分性质如表:
| 名称 | 结构简式 | 熔点/℃ | 沸点/℃ | 燃烧热/kJ∙mol-1 |
| 正戊烷 | CH3CH2CH2CH2CH3 | -130 | 36 | 3506.1 |
| 异戊烷 | (CH3)2CHCH2CH3 | -159.4 | 27.8 | 3504.1 |
(2)用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物。催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表:
| 助剂 | CO2转化率(%) | 各产物在所有产物中的占比(%) | ||
| C2H4 | C3H6 | 其他 | ||
| Na | 42.5 | 35.9 | 39.6 | 24.5 |
| K | 27.2 | 75.6 | 22.8 | 1.6 |
| Cu | 9.8 | 80.7 | 12.5 | 6.8 |
(3)在密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应:CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如图甲所示:

为提高H2S的平衡转化率,除改变温度外,还可采取的措施是
(4)合成碳酸二甲酯的工作原理如图乙所示。阳极的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


