解答题-实验探究题 适中0.65 引用2 组卷401
完成下列问题
(1)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:


根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1molC2H2(g)反应热化学方程式:___________ 。
(2)工业上利用CO和H2在催化剂作用下合成甲醇: ,已知反应中有关物质的化学键键能数据如下表所示:
,已知反应中有关物质的化学键键能数据如下表所示:
则
___________ 
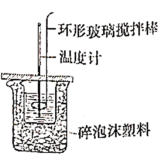
(3)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。

a.用量筒量取50mL0.50mol/L盐酸倒入如图装置的小烧杯中,测出盐酸温度。
b.用另一量筒量取50mL0.55mol/LNaOH溶液,并用另一温度计测出其温度。
c.将NaOH溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。
①实验中,倒入NaOH溶液的正确操作是___________ 。
A.一次性快速倒入 B.分3次倒入 C.边搅拌边慢慢倒入
②若将各含1mol溶质的NaOH稀溶液、Ca(OH)2稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为Q1、Q2、Q3,则Q1、Q2、Q3的关系为___________ 。
③若通过测定计算出产生的热量为1.39kJ,则中和热
___________ 。
(1)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1molC2H2(g)反应热化学方程式:
(2)工业上利用CO和H2在催化剂作用下合成甲醇:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
(3)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。

a.用量筒量取50mL0.50mol/L盐酸倒入如图装置的小烧杯中,测出盐酸温度。
b.用另一量筒量取50mL0.55mol/LNaOH溶液,并用另一温度计测出其温度。
c.将NaOH溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。
①实验中,倒入NaOH溶液的正确操作是
A.一次性快速倒入 B.分3次倒入 C.边搅拌边慢慢倒入
②若将各含1mol溶质的NaOH稀溶液、Ca(OH)2稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为Q1、Q2、Q3,则Q1、Q2、Q3的关系为
③若通过测定计算出产生的热量为1.39kJ,则中和热
21-22高二上·福建宁德·阶段练习
类题推荐
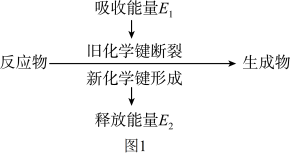
(1)如图 1 是化学反应中物质变化和能量变化的示意图。在锌与稀盐酸的反应中,E1_____ E2 (填“>”或“<”或“=”)
(2)工业上利用 CO 和 H2在催化剂作用下合成甲醇:CO(g)+2H2(g) CH3OH(g) ,已知反应中有关物质的化学键键能数据如下表所示:
CH3OH(g) ,已知反应中有关物质的化学键键能数据如下表所示:
则 CO(g)+2H2(g)  CH3OH(g) △H=
CH3OH(g) △H=_____ kJ•mol-1
(3)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。
a.用量筒量取 50 mL 0.50 mol·L-1盐酸倒入如图装置的小烧杯中,测出盐酸温度。 b.用另一量筒量取 50 mL 0.55 mol·L-1 NaOH 溶液,并用另一温度计测出其温度。 c.将 NaOH 溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。

①实验中,倒入 NaOH 溶液的正确操作是_____ 。
A.一次性快速倒入 B.分 3 次倒入 C.边搅拌边慢慢倒入
②若将各含 1mol 溶质的 NaOH 稀溶液、Ca(OH)2稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为 Q1、Q2、Q3,则 Q1、Q2、Q3的关系为_____ 。
③假设盐酸和氢氧化钠溶液的密度都是 1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。某学生实验后,处理数据,得到实验变化的温度为 3.20℃。该实验测得中和热ΔH =_____ (结果保留一位小数)。

(2)工业上利用 CO 和 H2在催化剂作用下合成甲醇:CO(g)+2H2(g)
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
(3)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。
a.用量筒量取 50 mL 0.50 mol·L-1盐酸倒入如图装置的小烧杯中,测出盐酸温度。 b.用另一量筒量取 50 mL 0.55 mol·L-1 NaOH 溶液,并用另一温度计测出其温度。 c.将 NaOH 溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。

①实验中,倒入 NaOH 溶液的正确操作是
A.一次性快速倒入 B.分 3 次倒入 C.边搅拌边慢慢倒入
②若将各含 1mol 溶质的 NaOH 稀溶液、Ca(OH)2稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为 Q1、Q2、Q3,则 Q1、Q2、Q3的关系为
③假设盐酸和氢氧化钠溶液的密度都是 1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。某学生实验后,处理数据,得到实验变化的温度为 3.20℃。该实验测得中和热ΔH =
I.(1)如图是化学反应中物质变化和能量变化的示意图。

在锌与稀盐酸的反应中,E1______ E2(填“>”或“<”或“=”)
(2)工业上利用 和
和 比在催化剂作用下合成甲醇:
比在催化剂作用下合成甲醇: ,已知反应中有关物质的化学键键能数据如下表所示:
,已知反应中有关物质的化学键键能数据如下表所示:
则 生成
生成
 放出
放出______  热量。
热量。
(3)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。
a.用量筒量取
 盐酸倒入如图装置的小烧杯中,测出盐酸温度。
盐酸倒入如图装置的小烧杯中,测出盐酸温度。
b.用另一量筒量取

 溶液,并用另一温度计测出其温度。
溶液,并用另一温度计测出其温度。
c.将 溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。
溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。
①实验中,倒入 溶液的正确操作是
溶液的正确操作是_______ 。
A.一次性快速倒入 B.分3次倒入 C.边搅拌边慢慢倒入
②若将各含 溶质的
溶质的 稀溶液、
稀溶液、 稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为Q1、Q2、Q3,则Q1、Q2、Q3的关系为
稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为Q1、Q2、Q3,则Q1、Q2、Q3的关系为______ 。
II.甲烷燃料电池。已知电池的总反应为 ,
,
①负极的电极反应式为_______ 。
②当消耗甲烷11.2L(标准状况下时),则导线中转移的电子的物质的量为______ mol。
在锌与稀盐酸的反应中,E1
(2)工业上利用
| 化学键 | |||||
| 436 | 343 | 1076 | 465 | 413 |
则
(3)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。

a.用量筒量取
b.用另一量筒量取
c.将
①实验中,倒入
A.一次性快速倒入 B.分3次倒入 C.边搅拌边慢慢倒入
②若将各含
II.甲烷燃料电池。已知电池的总反应为
①负极的电极反应式为
②当消耗甲烷11.2L(标准状况下时),则导线中转移的电子的物质的量为
利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.50 mol/L盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50mL 0.55 mol/L NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
(1)为什么所用NaOH溶液要稍过量_______ 。
(2)倒入NaOH溶液的正确操作是_______ (填序号)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是_______(填序号)。
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol/L的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为_______ 。
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生进行实验并通过实验数据计算,该实验测得中和热的数值为57.3 KJ/moL。写出中和热的热化学反应方程式:_______ 。
(6)大烧杯上如不盖硬纸板,求得的中和热ΔH_______ (填‘偏大’‘偏小’‘无影响’)

①用量筒量取50 mL 0.50 mol/L盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50mL 0.55 mol/L NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
(1)为什么所用NaOH溶液要稍过量
(2)倒入NaOH溶液的正确操作是
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是_______(填序号)。
| A.用温度计小心搅拌 |
| B.揭开硬纸片用玻璃棒搅拌 |
| C.轻轻地振荡烧杯 |
| D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动 |
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生进行实验并通过实验数据计算,该实验测得中和热的数值为57.3 KJ/moL。写出中和热的热化学反应方程式:
(6)大烧杯上如不盖硬纸板,求得的中和热ΔH
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


