填空题 适中0.65 引用1 组卷369
25 ℃时,部分物质的电离平衡常数如下表所示:
(1)NH3·H2O的电离方程式是_____________ ,25 ℃时,物质的量浓度为0.10 mol/L的氨水中,c(OH-)=___________ (列出算式即可)。
(2)25 ℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa________ (填“>”“<”或“=”)NaClO,请结合题目有关信息说明原因__________ 。
(3)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是_____ ,结合所给数据说明生成该产物的理由__________ 。
化学式 | CH3COOH | H2CO3 | HClO | NH3·H2O |
电离平 衡常数 | Ka=1.75×10-5 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 | Kb=1.8×10-5 |
(2)25 ℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa
(3)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是
23-24高二上·全国·课时练习
类题推荐
25℃时,部分物质的电离平衡常数如下表所示:
(1)NH3·H2O的电离方程式是___________ ,25℃时,物质的量浓度为0.10mol/L的氨水中,c(OH-)为___________ (列出算式即可)。
(2)下列方法中可以使0.10 mol/L醋酸溶液中 CH3COOH电离程度增大的是___________(填字母序号)。
(3)25℃时,pH与体积均相同的醋酸溶液A与盐酸B分别与足量镁条充分反应,下列说法不正确 的是 ___________ (填字母序号)。
a.开始反应时的速率:A < B
b.放出等量氢气所需要的时间A=B
c.生成氢气的总体积:A > B
(4)常温下, CH3COONa溶液呈___________ 性(填“酸”、“碱”、“中”),请用化学用语解释___________ 。该溶液中离子浓度由大到小的顺序是___________ 。
(5)25℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa___________ NaClO(填“>”、“<”或“=”),请结合题目有关信息说明原因_____ 。
(6)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是___________ ,结合所给数据说明生成该产物的理由___________ 。
| 化学式 | CH3COOH | H2CO3 | HClO | NH3·H2O |
| 电离平衡常数 | Ka=1.75×10-5 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 | Kb=1.8×10-5 |
(2)下列方法中可以使0.10 mol/L醋酸溶液中 CH3COOH电离程度增大的是___________(填字母序号)。
| A.加水稀释 | B.微热溶液 |
| C.滴加少量浓氢氧化钠 | D.加入少量醋酸钠晶体 |
a.开始反应时的速率:A < B
b.放出等量氢气所需要的时间A=B
c.生成氢气的总体积:A > B
(4)常温下, CH3COONa溶液呈
(5)25℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa
(6)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是
电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
(1)25℃时,pH=11的NaCN溶液中水电离出的c(OH-)____________ mol/L。
(2)25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为________ 。
(3)NH4Cl溶液呈______ 性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈_______ 性,0.1mol/LNH4HCO3溶液中物质的量浓度最大的离子是_________ (填化学式)。
(4)25℃时,等浓度的CH3COOH溶液和CH3COONa溶液等体积混合,混合溶液中各种离子浓度大小_________ 。
(5)向NaCN溶液中通入少量CO2,所发生反应的化学方程式______________ 。
| 化学式 | 电离平衡常数(25℃) |
| NH3·H2O | Kb=1.77×10-5 |
| HCN | Ka=4.93×10-10 |
| CH3COOH | Ka=1.76×10-5 |
| H2CO3 | Ka1=4.30×10-7,Ka2=5.61×10-11 |
(2)25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为
(3)NH4Cl溶液呈
(4)25℃时,等浓度的CH3COOH溶液和CH3COONa溶液等体积混合,混合溶液中各种离子浓度大小
(5)向NaCN溶液中通入少量CO2,所发生反应的化学方程式
25 ℃时,部分物质的电离平衡常数如表所示:
(1)25℃时,等浓度的Na2CO3溶液、CH3COONa溶液、Na2SO3溶液,3种溶液的pH由大到小的顺序为____________________________________________ 。
(2)工业上可用氨水除去尾气SO2。
①若氨水的浓度为2.0mol·L-1,溶液中的c(OH−)=________ mol·L−1。向该氨水中加入少量NH4Cl固体,溶液的pH__________ (填“升高”或“降低”);若加入少量明矾,溶液中NH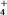 的浓度
的浓度____________ (填“增大”或“减小”)。
②将SO2通入氨水中,当c(OH−)降至1.0×10−7mol·L−1时,溶液中的 =
=_________________ 。
(3)若某溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
___________ c(NH3·H2O)(填“大于”、“小于”或“等于”,下同);混合前酸中c(H+)和碱中c(OH-)的关系为c(H+)____________ c(OH-)。
(4)根据表中所给的信息,向NaClO溶液中通入少量CO2气体,发生反应的离子方程式为____________________________________________________ 。
| 化学式 | CH3COOH | H2CO3 | HClO | NH3·H2O | H2SO3 |
| 电离平衡常数 | 1.8×10-5 | K1=4.2×10-7 K2=5.6×10-11 | 4.7×10-8 | 1.8×10-5 | Ka1=1.3×10−2 Ka2=6.2×10−8 |
(1)25℃时,等浓度的Na2CO3溶液、CH3COONa溶液、Na2SO3溶液,3种溶液的pH由大到小的顺序为
(2)工业上可用氨水除去尾气SO2。
①若氨水的浓度为2.0mol·L-1,溶液中的c(OH−)=
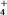 的浓度
的浓度②将SO2通入氨水中,当c(OH−)降至1.0×10−7mol·L−1时,溶液中的
(3)若某溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
(4)根据表中所给的信息,向NaClO溶液中通入少量CO2气体,发生反应的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


