解答题-实验探究题 适中0.65 引用2 组卷257
苯甲酸是一种化工原料,常用作制药和染料的中间体,也用于制取增塑剂和香料等。实验室合成苯甲酸的原理及有关数据及装置示意图如下:
反应过程: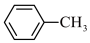

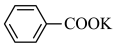

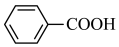
已知:(1)苯甲酸 100 ℃左右开始升华。
(2)反应试剂、产物的物理常数如下:
步骤Ⅰ:按图在 250 mL 仪器 a 中放入 2.7 mL 甲苯和 100 mL 水,控制温度为 100℃,搅拌溶液,在石棉网上加热至沸腾。从冷凝管上口分批加入 8.5 g 高锰酸钾(加完后用少量水冲洗冷凝管内壁),继续搅拌约 4~5h,反应完全后,停止加热。
步骤 II:在反应结束后混合物中加入一定量亚硫酸氢钠溶液,产生黑色沉淀,趁热过滤、热水洗涤沉淀,合并滤液与洗涤液,再将其放在冰水浴中冷却,然后用浓盐酸酸化至苯甲酸全部析出;将析出的苯甲酸减压过滤,再用少量冷水洗涤苯甲酸固体,挤压除去水分,将制得的苯甲酸固体放在沸水浴上干燥,得到粗产品。
(1)仪器 a 的名称___________________ 。
(2)步骤Ⅰ中反应完全的现象为___________________ 。
(3)步骤 II 在反应混合物中加入一定量亚硫酸氢钠溶液,亚硫酸氢钠溶液的作用是___________________ ;还可以用___________________ (填选项)代替亚硫酸氢钠溶液。
A . H2O2 B. NaHCO3 C. Na2C2O4
(4)步骤 II 中干燥苯甲酸晶体时,若温度过高,可能出现的结果是___________________ 。
(5)若将苯甲酸粗产品进一步提纯,可用___________________ 方法。
反应过程:

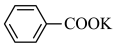

已知:(1)苯甲酸 100 ℃左右开始升华。
(2)反应试剂、产物的物理常数如下:
| 名称 | 性状 | 熔点 | 沸点/C | 密度/g·mL-1 | 溶解度/g(室温) | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体、易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 |
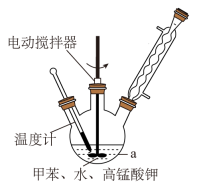
步骤Ⅰ:按图在 250 mL 仪器 a 中放入 2.7 mL 甲苯和 100 mL 水,控制温度为 100℃,搅拌溶液,在石棉网上加热至沸腾。从冷凝管上口分批加入 8.5 g 高锰酸钾(加完后用少量水冲洗冷凝管内壁),继续搅拌约 4~5h,反应完全后,停止加热。
步骤 II:在反应结束后混合物中加入一定量亚硫酸氢钠溶液,产生黑色沉淀,趁热过滤、热水洗涤沉淀,合并滤液与洗涤液,再将其放在冰水浴中冷却,然后用浓盐酸酸化至苯甲酸全部析出;将析出的苯甲酸减压过滤,再用少量冷水洗涤苯甲酸固体,挤压除去水分,将制得的苯甲酸固体放在沸水浴上干燥,得到粗产品。
(1)仪器 a 的名称
(2)步骤Ⅰ中反应完全的现象为
(3)步骤 II 在反应混合物中加入一定量亚硫酸氢钠溶液,亚硫酸氢钠溶液的作用是
A . H2O2 B. NaHCO3 C. Na2C2O4
(4)步骤 II 中干燥苯甲酸晶体时,若温度过高,可能出现的结果是
(5)若将苯甲酸粗产品进一步提纯,可用
22-23高二下·广西南宁·期末
类题推荐
苯甲酸是一种化工原料,常用作制药和染料的中间体等。实验室合成苯甲酸并利用苯甲酸制备苯甲酸乙酯的原理和有关数据及装置示意图如下:
b.分水器可以储存冷凝管冷凝的液体,当液面达到支管口时上层液体可回流到反应器中,通过下端活塞可以将密度较大的下层液体排放出去。
c.一些有机物的物理性质如表所示:
Ⅰ.用图1装置合成苯甲酸(加热及夹持装置已省略),实验步骤如下:
步骤②:在反应结束后向混合物中加入一定量 溶液,产生黑色沉淀,趁热过滤、热水洗涤沉淀,合并滤液与洗涤液,再将其放在冰水浴中冷却,然后用浓盐酸酸化至苯甲酸全部析出;将析出的苯甲酸经过滤、冷水洗涤后放在沸水浴上干燥,得到粗产品。
溶液,产生黑色沉淀,趁热过滤、热水洗涤沉淀,合并滤液与洗涤液,再将其放在冰水浴中冷却,然后用浓盐酸酸化至苯甲酸全部析出;将析出的苯甲酸经过滤、冷水洗涤后放在沸水浴上干燥,得到粗产品。
Ⅱ.用图2装置合成苯甲酸乙酯(加热及夹持装置已省略)实验步骤如下:
步骤④:控制温度在65~70℃加热回流2h,期间不时打开旋塞放出分水器中的下层液体;
步骤⑤:反应结束后,将三颈烧瓶内反应液依次用水、饱和 溶液、水洗涤。用分液漏斗分离出有机层与分水器中分离的有机层合并,水层经
溶液、水洗涤。用分液漏斗分离出有机层与分水器中分离的有机层合并,水层经 处理后用适量乙醚萃取分液,然后合并至有机层;
处理后用适量乙醚萃取分液,然后合并至有机层;
步骤⑥:向⑤中所得有机层中加入氯化钙固体,蒸馏,接收210~213℃的馏分,得到产品12.00mL。
回答下列问题:
(1)图2中冷凝管的出水口为___________ (填“a”或“b”);步骤③中碎瓷片的作用是___________ 。
(2)步骤②在反应混合物中加入一定量 溶液,
溶液, 溶液的作用是
溶液的作用是___________ ;还可以用___________ (填字母)代替 溶液。
溶液。
A. B.
B. C.
C.
(3)步骤②干燥苯甲酸晶体时,若温度过高,可能出现的结果是___________ 。
(4)步骤④“加热回流”时,装置宜采用的加热方法是___________ ,判断反应完成的实验现象为___________ 。
(5)使用分水器能提高酯的产率,原因是___________ (用平衡移动的原理解释)。
(6)本实验得到的苯甲酸乙酯的产率为___________ (结果保留3位有效数字)。
反应过程: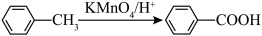

b.分水器可以储存冷凝管冷凝的液体,当液面达到支管口时上层液体可回流到反应器中,通过下端活塞可以将密度较大的下层液体排放出去。
c.一些有机物的物理性质如表所示:
| 名称 | 性状 | 沸点/℃ | 密度/ | 溶解性 |
| 甲苯 | 无色液体、易燃、易挥发 | 110.6 | 0.8669 | 不溶于水,与乙醇互溶 |
| 苯甲酸 | 无色晶体 | 249(100℃升华) | 1.27 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 |
| 苯甲酸乙酯 | 无色液体 | 212.6 | 1.05 | 微溶于热水,与乙醇、乙醚混溶 |
| 乙醇 | 无色液体 | 78.3 | 0.79 | 与水互溶 |
| 环己烷 | 无色液体 | 80.8 | 0.73 | 不溶于水 |
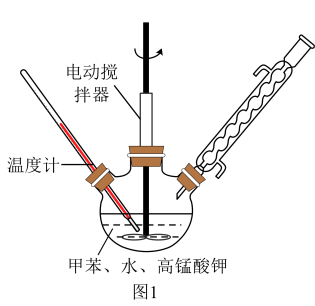
步骤②:在反应结束后向混合物中加入一定量
Ⅱ.用图2装置合成苯甲酸乙酯(加热及夹持装置已省略)实验步骤如下:
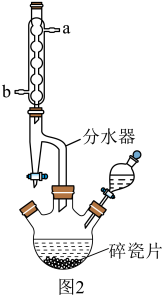
步骤④:控制温度在65~70℃加热回流2h,期间不时打开旋塞放出分水器中的下层液体;
步骤⑤:反应结束后,将三颈烧瓶内反应液依次用水、饱和
步骤⑥:向⑤中所得有机层中加入氯化钙固体,蒸馏,接收210~213℃的馏分,得到产品12.00mL。
回答下列问题:
(1)图2中冷凝管的出水口为
(2)步骤②在反应混合物中加入一定量
A.
(3)步骤②干燥苯甲酸晶体时,若温度过高,可能出现的结果是
(4)步骤④“加热回流”时,装置宜采用的加热方法是
(5)使用分水器能提高酯的产率,原因是
(6)本实验得到的苯甲酸乙酯的产率为
苯甲酸是一种重要的化工原料。实验室合成苯甲酸的原理、有关数据及装置示意图如下:

苯甲酸在水中的溶解度如右表:
草酸(H2C2O4)为易溶于水的固体
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
一、制备苯甲酸
在三颈瓶中加入2.7mL甲苯、100mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加入8.5g高锰酸钾,继续搅拌约4~5h,直到甲苯层几乎近于消失、回流液不再出现油珠,停止加热和搅拌,静置。
二、分离提纯
在反应混合物中加入一定量草酸充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,挤压去水分后放在沸水浴上干燥,得到粗产品。
三、测定纯度
称取mg产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶,滴加2~3滴酚酞,然后用标准浓度KOH溶液滴定。
请回答下列问题:
(1)装置a的名称是____________ ,其作用为______________________ 。
(2)甲苯被高锰酸钾氧化的原理为:
 ,
,
请完成并配平该化学方程式________________ 。
(3)分离提纯过程中加入的草酸是一种二元弱酸,反应过程中有酸式盐和无色气体生成。加入草酸的作用是_______ ,请用离子方程式表示反应原理_________________________ 。
(4)产品减压过滤时用冷水洗涤的原因是________________________ 。
(5)选用下列__________ 操作,可以将粗产品进一步提纯。(选填字母)
(6)测定纯度步骤中,滴定终点溶液的颜色变化是______________ 。若m=1.200g,滴定时用去0.1200mol· L-1标准KOH溶液20.00mL,则所得产品中苯甲酸的质量分数为_______________ 。

| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 密度 (g/mL) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 112.4 (100℃左右升华) | 248 | 1.2659 | 微溶 | 易溶 |
| 温度/℃ | 4 | 18 | 75 |
| 溶解度/g | 0.2 | 0.3 | 2.2 |
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
一、制备苯甲酸
在三颈瓶中加入2.7mL甲苯、100mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加入8.5g高锰酸钾,继续搅拌约4~5h,直到甲苯层几乎近于消失、回流液不再出现油珠,停止加热和搅拌,静置。
二、分离提纯
在反应混合物中加入一定量草酸充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,挤压去水分后放在沸水浴上干燥,得到粗产品。
三、测定纯度
称取mg产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶,滴加2~3滴酚酞,然后用标准浓度KOH溶液滴定。
请回答下列问题:
(1)装置a的名称是
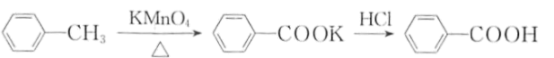
(2)甲苯被高锰酸钾氧化的原理为:
 ,
,请完成并配平该化学方程式
(3)分离提纯过程中加入的草酸是一种二元弱酸,反应过程中有酸式盐和无色气体生成。加入草酸的作用是
(4)产品减压过滤时用冷水洗涤的原因是
(5)选用下列
| A.溶于水后过滤 | B.溶于乙醇后蒸馏 | C.用甲苯萃取后分液 | D.升华 |
苯甲酸是一种重要的化工原料。实验室合成苯甲酸的原理、有关数据及装置示意图如下:

苯甲酸在水中的溶解度如表:
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
一、制备苯甲酸
在b中加入2.7mL甲苯、100mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加入8.5g高锰酸钾,继续搅拌约4~5h,直到甲苯层几乎近于消失、回流液不再出现油珠,停止加热和搅拌,静置。
二、分离提纯
在反应混合物中加入一定量草酸(H2C2O4)充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,挤压去水分后放在沸水浴上干燥,得到粗产品。
三、测定纯度
称取m g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶中,滴加2~3滴酚酞,然后用标准浓度的KOH溶液滴定。
请回答下列问题:
(1)装置b的名称是__________________ ,装置a的作用为_____________________________ 。
(2)分离提纯过程中加入的草酸是一种二元弱酸,反应过程中有酸式盐、无色气体和黑色固体生成。加入草酸的作用是_________________________ ,请用离子方程式表示反应的原理______________________________ 。
(3)产品减压过滤时用冷水洗涤的原因是__________________________________________ 。
(4)选用下列__________ 操作,可以将粗产品进一步提纯。(选填字母)
A.溶于水后过滤 B.溶于乙醇后蒸馏 C.用甲苯萃取后分液 D.升华
(5)测定纯度步骤中,判断滴定终点的标志是________________________________________________ 。若m=1.200g,滴定时用去0.1200mol· L-1标准KOH溶液18.00mL,则所得产品中苯甲酸的质量分数为__________ (保留四位有效数字)。

| 名词 | 性状 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 112.4(100℃左右升华) | 248 | 1.2659 | 微溶 | 易溶 |
| 温度/℃ | 4 | 18 | 75 |
| 溶解度/g | 0.2 | 0.3 | 2.2 |

一、制备苯甲酸
在b中加入2.7mL甲苯、100mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加入8.5g高锰酸钾,继续搅拌约4~5h,直到甲苯层几乎近于消失、回流液不再出现油珠,停止加热和搅拌,静置。
二、分离提纯
在反应混合物中加入一定量草酸(H2C2O4)充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,挤压去水分后放在沸水浴上干燥,得到粗产品。
三、测定纯度
称取m g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶中,滴加2~3滴酚酞,然后用标准浓度的KOH溶液滴定。
请回答下列问题:
(1)装置b的名称是
(2)分离提纯过程中加入的草酸是一种二元弱酸,反应过程中有酸式盐、无色气体和黑色固体生成。加入草酸的作用是
(3)产品减压过滤时用冷水洗涤的原因是
(4)选用下列
A.溶于水后过滤 B.溶于乙醇后蒸馏 C.用甲苯萃取后分液 D.升华
(5)测定纯度步骤中,判断滴定终点的标志是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


