解答题-原理综合题 适中0.65 引用1 组卷148
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1mol·L-1NH4Al(SO4)2溶液中的c( )
)___________ (填“等于”“大于”或“小于”)0.1mol·L-1NH4HSO4溶液中的c( )。
)。
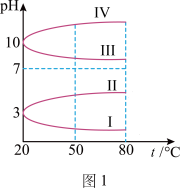
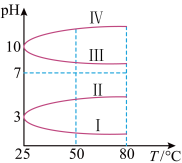
(2)浓度均为0.1mol·L-1的几种电解质溶液的pH随温度变化的曲线如图1所示:___________ ,导致pH随温度变化的原因是___________ 。
②25℃时,0.1mol·L-1NH4Al(SO4)2溶液中2c( )-c(
)-c( )-3c(Al3+)=
)-3c(Al3+)=___________ mol·L-1(填精确 数值表达式)
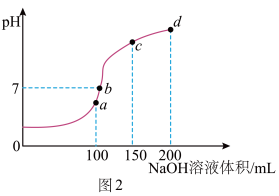
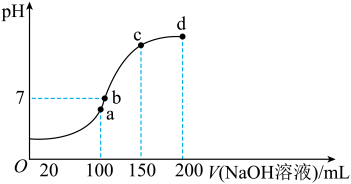
(3)室温时,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的关系如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是___________ 点;在b点,溶液中各离子浓度由大到小的排列顺序是___________ 。___________ 。(25℃时,Al(OH)3的Ksp=1×10-34)
(5)向AgNO3溶液中加入过量NaCl溶液,会有白色沉淀产生,接着加入NaI溶液,发现白色沉淀变为黄色,请用平衡移动原理来解释颜色变化与溶液中c(Cl-)升高的原因:___________ 。
(1)相同条件下,0.1mol·L-1NH4Al(SO4)2溶液中的c(
(2)浓度均为0.1mol·L-1的几种电解质溶液的pH随温度变化的曲线如图1所示:
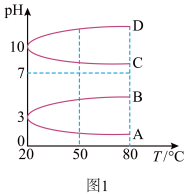
②25℃时,0.1mol·L-1NH4Al(SO4)2溶液中2c(
(3)室温时,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的关系如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
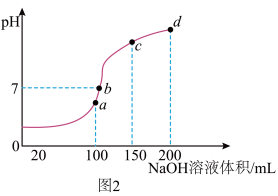
(5)向AgNO3溶液中加入过量NaCl溶液,会有白色沉淀产生,接着加入NaI溶液,发现白色沉淀变为黄色,请用平衡移动原理来解释颜色变化与溶液中c(Cl-)升高的原因:
22-23高二下·上海嘉定·期末
类题推荐
回答下列问题。
(1)下列物质的水溶液因水解而呈碱性的是___________。
(2)0.1mol•L﹣1的醋酸溶液中存在电离平衡:CH3COOH⇌CH3COO﹣+H+,要使溶液中 值增大,可以采取的措施是___________。
值增大,可以采取的措施是___________。
①加少量烧碱固体②升高温度③加少量冰醋酸④加水
(3)氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是___________。
(4)溶液的pH与水的电离密切相关,以下说法一定正确的是___________。
(5)室温下,在10mL浓度均为0.1mol•L﹣1的醋酸和盐酸混合液中,滴加0.1mol•L﹣1的NaOH溶液VmL,则下列关系正确的是___________。
(6)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
①相同条件下,0.1mol•L﹣1NH4Al(SO4)2溶液中的c( )
)___________ (填“等于”“大于”或“小于”)0.1mol•L﹣1NH4HSO4溶液中的c( )。
)。
②浓度均为0.1mol•L﹣1的几种电解质溶液的pH随温度变化的曲线如图1所示:
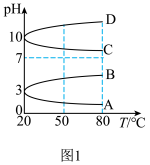
i.其中符合0.1mol•L﹣1NH4Al(SO4)2溶液的pH随温度变化的曲线是___________ ,导致pH随温度变化的原因是___________ 。
ii.20℃时,0.1mol•L﹣1NH4Al(SO4)2溶液中2c( )﹣c(
)﹣c( )﹣3c(A13+)=
)﹣3c(A13+)=___________ mol•L﹣1(填精确数值表达式)。
③室温时,向100mL0.1mol•L﹣1NH4HSO4溶液中滴加0.1mol•L﹣1NaOH溶液,溶液pH与NaOH溶液体积的关系如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是___________ 点;在b点,溶液中各离子浓度由大到小的排列顺序是___________ 。

④难溶电解质在水溶液中存在溶解平衡。25℃,某NH4Al(SO4)2溶液里c(A13+)=0.1mol•L﹣1,使Al3+开始沉淀的pH为___________ 。[25℃时,Al(OH)3的Ksp=1×10﹣34]
⑤向AgNO3溶液中加入过量NaCl溶液,会有白色沉淀产生,接着加入NaI溶液,发现白色沉淀变为黄色,请用平衡移动原理来解释颜色变化与溶液中c(Cl﹣)升高的原因:___________ 。
(1)下列物质的水溶液因水解而呈碱性的是___________。
| A.Na2S | B.NH3 | C.KOH | D.NH4Cl |
(2)0.1mol•L﹣1的醋酸溶液中存在电离平衡:CH3COOH⇌CH3COO﹣+H+,要使溶液中
①加少量烧碱固体②升高温度③加少量冰醋酸④加水
| A.②③ | B.②④ | C.①④ | D.①③ |
(3)氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是___________。
| A.1mol•L﹣1氢氰酸(HCN)溶液的pH约为3 |
| B.HCN易溶于水 |
| C.10mL1mol•L﹣1HCN恰好与10mL1mol•L﹣1NaOH溶液完全反应 |
| D.HCN溶液的导电性比强酸溶液的弱 |
(4)溶液的pH与水的电离密切相关,以下说法一定正确的是___________。
| A.90℃的纯水pH=7 |
| B.将醋酸滴入氢氧化钠溶液,促进了水的电离 |
| C.电解质溶液中都存在水的电离平衡 |
| D.室温下pH相同的盐酸和明矾溶液,水的电离程度相同 |
(5)室温下,在10mL浓度均为0.1mol•L﹣1的醋酸和盐酸混合液中,滴加0.1mol•L﹣1的NaOH溶液VmL,则下列关系正确的是___________。
| A.V=0时:c(H+)>c(Cl﹣)=c(CH3COOH) |
| B.V=10mL时:c(OH﹣)+c(CH3COO﹣)=c(H+) |
| C.V=20mL时:c(Na+)<c(CH3COO﹣)+c(Cl﹣) |
| D.加入NaOH溶液至pH=7时,V>20mL |
(6)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
①相同条件下,0.1mol•L﹣1NH4Al(SO4)2溶液中的c(
②浓度均为0.1mol•L﹣1的几种电解质溶液的pH随温度变化的曲线如图1所示:

i.其中符合0.1mol•L﹣1NH4Al(SO4)2溶液的pH随温度变化的曲线是
ii.20℃时,0.1mol•L﹣1NH4Al(SO4)2溶液中2c(
③室温时,向100mL0.1mol•L﹣1NH4HSO4溶液中滴加0.1mol•L﹣1NaOH溶液,溶液pH与NaOH溶液体积的关系如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是

④难溶电解质在水溶液中存在溶解平衡。25℃,某NH4Al(SO4)2溶液里c(A13+)=0.1mol•L﹣1,使Al3+开始沉淀的pH为
⑤向AgNO3溶液中加入过量NaCl溶液,会有白色沉淀产生,接着加入NaI溶液,发现白色沉淀变为黄色,请用平衡移动原理来解释颜色变化与溶液中c(Cl﹣)升高的原因:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网