解答题-实验探究题 适中0.65 引用1 组卷173
氯化铁(FeCl3)是一种棕色结晶,易升华,有强烈的吸水性。实验室制备无水氯化铁并探究氯化铁性质的相关实验如下。
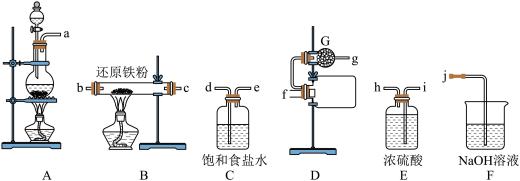
(1)装置A中发生反应的离子方程式是_______ 。
(2)实验装置接口的连接顺序是a→_______ →j, G中盛装的物质是_______ 。
(3)当观察到出现_______ 现象时,再点燃B处的酒精灯。
(4)若没有使用C装置,则可能导致的不良后果是_______ 。
Ⅱ.探究D中固态产物的相关性质
(5)取适量D中收集到的固态物质进行相关实验,完成下列实验,回答问题。

(1)装置A中发生反应的离子方程式是
(2)实验装置接口的连接顺序是a→
(3)当观察到出现
(4)若没有使用C装置,则可能导致的不良后果是
Ⅱ.探究D中固态产物的相关性质
(5)取适量D中收集到的固态物质进行相关实验,完成下列实验,回答问题。
| 序号 | 实验操作 | 实验现象 | 问题或结论 |
① | 取少量固态物质置于烧杯中,加入适量蒸馏水,搅拌,溶解 | 溶液浑浊,滴加某试剂,振荡,得到棕黄色澄清溶液 | 该试剂是 |
② | 取少量①中的澄清溶液于试管 中,滴加一滴 | 无明显现象 | 证明原固体中不含 FeCl2 |
③ | 将①中的澄清溶液滴入刚做完 银镜反应实验的试管中,振荡 | 管壁上的银镜溶解,溶液浑 浊 | 相关离子方程式是 |
20-21高三下·广东汕头·阶段练习
类题推荐
氯化铁(FeCl3)是一种黑棕色结晶,易升华,易溶于水并且有强烈的吸水性。实验室制备无水氯化铁并探究氯化铁的相关实验如下。
I.利用MnO2粉末、浓盐酸、还原铁粉制备无水氯化铁
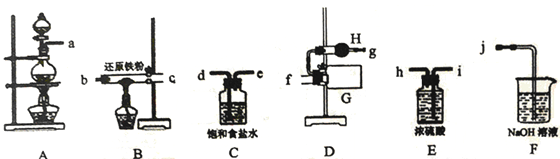
(1)写出装置A中发生的离子方程式_______ 。
(2)整套实验装置接口的连接顺序是_______ ,仪器H的名称是_______ 。
(3)当出现_______ 实验现象时,再点燃B处的酒精灯。
II.探究FeCl3的相关性质
(4)将G中所得固体进行相关实验,完成下列实验,回答问题。
Ⅲ.探究FeCl3与KSCN溶液的反应
(5)向试管中滴加5mL0.01mol/LKSCN溶液,再滴加5mL0.005mol/L FeCl3,溶液显红色,发生反应:Fe3+(aq)+3SCN-(aq)⇌Fe(SCN)3(aq)。将该红色溶液分成2份,分别装于A、B三支试管中,分别完成下列实验。
I.利用MnO2粉末、浓盐酸、还原铁粉制备无水氯化铁

(1)写出装置A中发生的离子方程式
(2)整套实验装置接口的连接顺序是
(3)当出现
II.探究FeCl3的相关性质
(4)将G中所得固体进行相关实验,完成下列实验,回答问题。
| 序号 | 实验操作 | 实验现象 | 问题或结论 |
| ① | 取少量G中固体置于烧杯中,加入适量蒸馏水,搅拌,溶解 | 溶液显浑浊,经过处理,得到澄清溶液。 | 该“处理”的操作是① |
| ② | 取少量①中的澄清溶液于试管中,滴加2滴② | 无明显现象 | 证明原固体中不含FeCl2, 原固体是FeCl3固体 |
| ③ | 将SO2气体通入BaCl2溶液中,再滴入①中的澄清溶液 | 开始无明显现象,后来有白色沉淀生成 | FeCl3表现出③ |
| ④ | 将①中的澄清溶液滴入刚刚做完银镜反应实验的试管中,振荡 | 银镜溶解,溶液显浑浊 | 相关离子方程式是④ |
(5)向试管中滴加5mL0.01mol/LKSCN溶液,再滴加5mL0.005mol/L FeCl3,溶液显红色,发生反应:Fe3+(aq)+3SCN-(aq)⇌Fe(SCN)3(aq)。将该红色溶液分成2份,分别装于A、B三支试管中,分别完成下列实验。
| 序号 | 实验操作 | 实验现象 | 给出合理的解释 |
| ① | 向A试管中滴加5滴1 mol/L KSCN溶液 | 红色溶液变为血红色 | |
| ② | 向B试管中加入lgKCl固体(足量,溶液体积变化忽略不计),振荡,静置 | 固体未完全溶解,红色溶液变浅(接近无色) |
ClO2是一种新型的环保饮用水消毒剂。为了收集ClO2并探究其性质,某课题小组拟选择下列部分装置进行实验(装置不可重复使用):
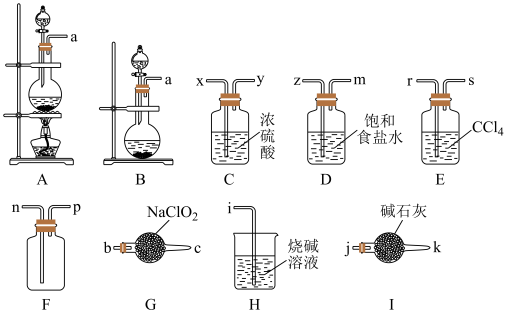
已知:①常温下,NaClO2固体与Cl2反应生成ClO2和NaCl;
②饱和食盐水可除去氯气中混有的氯化氢气体;
③Cl2易溶于有机溶剂,ClO2是一种易溶于水而难溶于有机溶剂的气体,氧化性比氯气强。
回答下列问题:
探究ClO2的制备实验:
(1)实验室中常用二氧化锰与浓盐酸制取氯气,故上述发生装置应选择_____ (填“A”或“B”),该反应的化学方程式为________ 。
(2)用上图装置制备二氧化氯:导管口连接顺序为:__________ ,a→___→__→___→___→___→___→___→___→n→p→j;本实验选择装置I而不选择装置H的原因是:___________ 。写出装置G中发生反应的化学方程式:___________ 。
(3)探究ClO2与少量Na2S的反应:
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的C1O2通入如图所示装置中充分反应,得到无色澄清溶液。
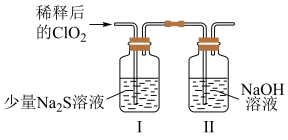
一段时间后,通过下列实验探究I中反应的产物(已知:二氧化硫或亚硫酸能使品红溶液褪色)。
③若C1O2中氯元素被还原为Cl-,则ClO2与少量Na2S反应的离子方程式为___________ 。

已知:①常温下,NaClO2固体与Cl2反应生成ClO2和NaCl;
②饱和食盐水可除去氯气中混有的氯化氢气体;
③Cl2易溶于有机溶剂,ClO2是一种易溶于水而难溶于有机溶剂的气体,氧化性比氯气强。
回答下列问题:
探究ClO2的制备实验:
(1)实验室中常用二氧化锰与浓盐酸制取氯气,故上述发生装置应选择
(2)用上图装置制备二氧化氯:导管口连接顺序为:
(3)探究ClO2与少量Na2S的反应:
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的C1O2通入如图所示装置中充分反应,得到无色澄清溶液。

一段时间后,通过下列实验探究I中反应的产物(已知:二氧化硫或亚硫酸能使品红溶液褪色)。
| 操作步骤 | 实验现象 | 结论 |
| 取少量I中反应后的溶液放入试管甲中,滴加品红溶液和盐酸 | 品红溶液始终不褪色 | ①无 |
| 另取少量I中反应后的溶液放入试管乙中,加入Ba(OH)2溶液振荡 | ② | 有 |
二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为10℃,可用于饮用水净化。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
I .ClO2的制备
已知:在强酸性溶液中用SO2还原NaClO3能制备ClO2
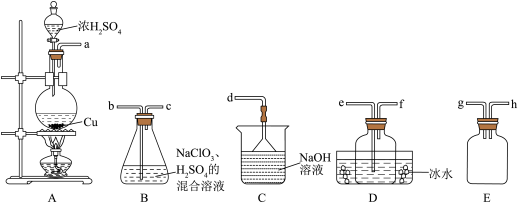
(1)反应过程中圆底烧瓶内会看到溶液中有一种白色固体析出,为了证明该物质常采用的实验操作及现象为:待实验完成、圆底烧瓶冷却后,____________________ 。
(2)装置B中反应的离子方程式为_________________________ 。
(3)欲制备并收集ClO2,选择上图中的装置,其连接顺序为a→_________ (按气流方向,用小写字母表示)
(4)装置D的作用_______________ 。
Ⅱ. ClO2与Na2S的反应
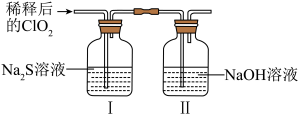
(5)将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通 入上图所示装置中充分反应,得到无色澄清溶液。—段时间后,通过下列实验探究I中反应的产物。
(6)C1O2与Na2S反应的离子方程式为_________ 。用于饮用水净化时,ClO2相对于Cl2的优点是______________ (任写一条)。
I .ClO2的制备
已知:在强酸性溶液中用SO2还原NaClO3能制备ClO2

(1)反应过程中圆底烧瓶内会看到溶液中有一种白色固体析出,为了证明该物质常采用的实验操作及现象为:待实验完成、圆底烧瓶冷却后,
(2)装置B中反应的离子方程式为
(3)欲制备并收集ClO2,选择上图中的装置,其连接顺序为a→
(4)装置D的作用
Ⅱ. ClO2与Na2S的反应

(5)将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通 入上图所示装置中充分反应,得到无色澄清溶液。—段时间后,通过下列实验探究I中反应的产物。
| 操作步骤 | 实验现象 | 结论 |
| 取少量Ⅰ中溶液于试管甲中,滴加品红溶液和盐酸。 | 品红始终不褪色 | ①无 |
| 另取少量Ⅰ中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ② | 有 |
| ③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管中, | 有白色沉淀生成 | 有Cl-生成 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


