解答题-实验探究题 适中0.65 引用1 组卷89
微量实验具有用量少,污染小,操作简单,现象明显等特点,硬质玻璃管可用于气体微量实验的场所。如图所示,将浓硫酸滴入培养皿后,会产生一种无色的气体。一段时间后,a、b、c、d四个棉球都褪为白色 。
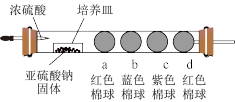
(1)a棉球变白后,微热该处一段时间,棉球又恢复红色,则a棉球上滴有的溶液为_______ 。
(2)b棉球上滴有的溶液为___________ 。发生反应的化学方程式为___________ 。
(3)c棉球上滴有酸性高锰酸钾溶液,它变为白色原因与___________ (填“a”、或“b”)棉球相同,说明无色气体具有___________ 性。
(4)d棉球上滴有NaOH溶液(混有酚酞),棉球变为白色说明无色气体溶于水显_______ 性。
(5)装置末端通入充满硫化氢溶液中,现象是___________ ,反应的化学反应方程式为___________ 。说明无色气体具有___________ 性。

(1)a棉球变白后,微热该处一段时间,棉球又恢复红色,则a棉球上滴有的溶液为
(2)b棉球上滴有的溶液为
(3)c棉球上滴有酸性高锰酸钾溶液,它变为白色原因与
(4)d棉球上滴有NaOH溶液(混有酚酞),棉球变为白色说明无色气体溶于水显
(5)装置末端通入充满硫化氢溶液中,现象是
22-23高一下·上海闵行·期末
类题推荐
为验证 SO2的相关性质,某化学兴趣小组利用硬质玻璃管设计了如图所示的微型实验装置(夹持仪器已省略),实验时将浓硫酸滴入装有 Na2SO3固体的培养皿中,观察实验现象,并回答下列问题。
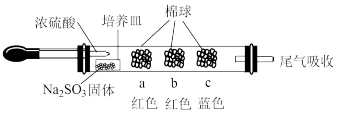
(1)浓硫酸与亚硫酸钠固体反应的化学方程式为___________ 。
(2)请填写表中空白:

(1)浓硫酸与亚硫酸钠固体反应的化学方程式为
(2)请填写表中空白:
| 棉球 | 棉球上蘸有的试剂 | 实验现象 | 解释或结论 |
| a | 棉球变白;棉球微热后变红 | 该气体具有漂白性 | |
| b | 含酚酞的NaOH 溶液 | 棉球变为白色 | 离子方程式: |
| c | I2与淀粉的混合溶液 | 棉球变为白色 | 化学方程式: |
完成下列问题。
I.
(1)硬质玻璃管是化学实验中经常使用的一种仪器,进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。

II.分析并回答下列问题:
利用Y型管与其它仪器组合可以进行许多实验(固定装置略)。分析并回答下列问题:

(2)实验目的:验证SO2有_______ 性。
(3)将胶头滴管中浓硫酸分别滴入Y型管的两个支管中,在支管交叉处发生的化学方程式是_______ ,实验现象为_______ ;
(4)硫化亚铁处加水的目的是_______ 。
I.
(1)硬质玻璃管是化学实验中经常使用的一种仪器,进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。

| 棉球 | 棉球上滴加试剂 | 实验现象 | 解释或结论 |
| a | 棉球变白,微热后又恢复红色 | 解释: 结论:该气体具有漂白性。 | |
| b | 含酚酞的NaOH溶液 | 棉球变为白色 | 结论:该气体水溶液具有 过程中可能发生反应化学方程式 |
| c | 棉球变为白色 | 化学方程式: 结论:该气体具有 |
II.分析并回答下列问题:
利用Y型管与其它仪器组合可以进行许多实验(固定装置略)。分析并回答下列问题:

(2)实验目的:验证SO2有
(3)将胶头滴管中浓硫酸分别滴入Y型管的两个支管中,在支管交叉处发生的化学方程式是
(4)硫化亚铁处加水的目的是
I、硬质玻璃管是化学实验中经常使用的一种仪器,分析下列实验并回答:
如图1所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c 三个棉球变化如下表(认为所产生的气体与棉球上的试剂均得到充分的反应)。则浓硫酸在该反应中表现的性质_________________ ;

II.通常情况下,向硫酸亚铁溶液中滴加氢氧化钠溶液时,生成的白色絮状沉淀会迅速变为_____ 色,最终变为____ 色写出上述白色絮状沉淀变化过程的化学方程式_______ ;
用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一: 用不含O2的蒸馏水配制的NaOH 溶液与硫酸亚铁反应制备。
(1)除去蒸馏水中溶解的O2常采用_________ 的方法。
(2)生成白色Fe(OH)2 沉淀的操作是用长滴管吸取不含O2的NaOH 溶液,插入FeSO4溶液液面下,再挤出NaOH 溶液。
方法二: 如右图装置中,用NaOH 溶液、铁屑、稀H2SO4等试剂制备。

(1)在试管I里加入的试剂是___________ 。
(2)为了制得白色Fe(OH)2沉淀,在试管I和II中加入试剂,打开止水夹,塞紧塞子后,检验试管II出口处排出的氢气的纯度。当排出的氢气纯净时,再________ (如何操作)。这样生成的Fe(OH)2沉淀能较长时间保持白色。原因是____________ 。
如图1所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c 三个棉球变化如下表(认为所产生的气体与棉球上的试剂均得到充分的反应)。则浓硫酸在该反应中表现的性质

| 棉球 | 棉球上滴加试剂 | 实验现象 | 解释或结论 |
| a | 棉球变白,微热后又恢复红色 | 该气体具有 | |
| b | 含酚酞的NaOH 溶液 | 棉球变为白色 | 离子方程式 |
| c | 棉球变为白色 | 化学方程式 |
用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一: 用不含O2的蒸馏水配制的NaOH 溶液与硫酸亚铁反应制备。
(1)除去蒸馏水中溶解的O2常采用
(2)生成白色Fe(OH)2 沉淀的操作是用长滴管吸取不含O2的NaOH 溶液,插入FeSO4溶液液面下,再挤出NaOH 溶液。
方法二: 如右图装置中,用NaOH 溶液、铁屑、稀H2SO4等试剂制备。

(1)在试管I里加入的试剂是
(2)为了制得白色Fe(OH)2沉淀,在试管I和II中加入试剂,打开止水夹,塞紧塞子后,检验试管II出口处排出的氢气的纯度。当排出的氢气纯净时,再
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


