解答题-实验探究题 适中0.65 引用4 组卷919
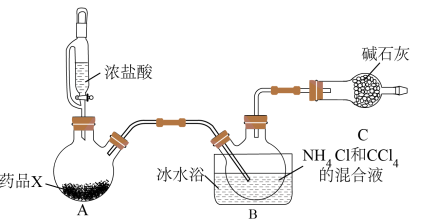
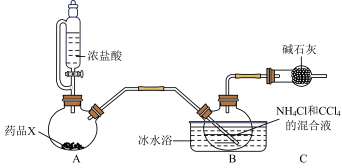
三氯化氮是一种黄色油状液体,可用于漂白和杀菌。已知: 熔点为-40℃,沸点为70℃,95℃以上易爆炸。在弱酸性溶液中稳定,在热水中易水解,遇碱则迅速反应。在实验室可用
熔点为-40℃,沸点为70℃,95℃以上易爆炸。在弱酸性溶液中稳定,在热水中易水解,遇碱则迅速反应。在实验室可用 和
和 溶液反应制取
溶液反应制取 ,所用仪器如图(忽略部分夹持装置):
,所用仪器如图(忽略部分夹持装置):

回答下列问题:
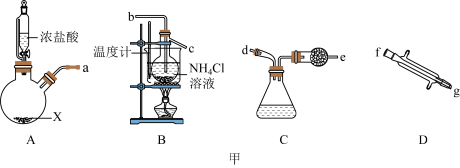
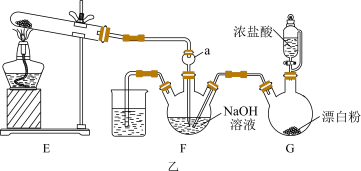
(1)根据气流方向,各仪器的连接顺序为a接_______ ,_______ 接_______ ,g接d;装置A中使用恒压滴液漏斗的优点是_______
(2)若用装置A制取氯气,则试剂X可选用_______ (填字母);D中仪器的名称为_______
A. B.
B. C.
C. D.
D.
(3)实验过程中,在B中蒸馏烧瓶中观察到的现象是_______ ,反应生成的 遇热水易水解,反应液有漂白性.写出
遇热水易水解,反应液有漂白性.写出 水解的化学方程式:
水解的化学方程式:_______
(4) 纯度测定:
纯度测定: 的制取是可逆反应,根据反应
的制取是可逆反应,根据反应 ,利用间接碘量法测定氯气的量即可测定
,利用间接碘量法测定氯气的量即可测定 的纯度
的纯度
实验步骤:ⅰ.准确称量C中的产物0.4g置于三颈烧瓶中,加入10mL足量浓盐酸,使用磁力搅拌器搅拌,并鼓入氮气
ⅱ.将混合气通入200mL KI溶液中,待试管中无色液体变成黄色,关闭氮气(溶液体积变化忽略不计)
KI溶液中,待试管中无色液体变成黄色,关闭氮气(溶液体积变化忽略不计)
ⅲ.量取20.00mL吸收液,加入淀粉指示剂,用 标准液进行滴定,滴定至终点时消耗
标准液进行滴定,滴定至终点时消耗 溶液18.00mL。
溶液18.00mL。
(已知:反应原理为 )
)
①确定滴定终点的现象为_______
② 的纯度为
的纯度为_______ (保留三位有效数字)

回答下列问题:
(1)根据气流方向,各仪器的连接顺序为a接
(2)若用装置A制取氯气,则试剂X可选用
A.
(3)实验过程中,在B中蒸馏烧瓶中观察到的现象是
(4)
实验步骤:ⅰ.准确称量C中的产物0.4g置于三颈烧瓶中,加入10mL足量浓盐酸,使用磁力搅拌器搅拌,并鼓入氮气
ⅱ.将混合气通入200mL
ⅲ.量取20.00mL吸收液,加入淀粉指示剂,用
(已知:反应原理为
①确定滴定终点的现象为
②
2023·河北衡水·三模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网