解答题-原理综合题 较难0.4 引用2 组卷368
减弱温室效应的方法之一是将 回收利用,科学家研究利用回收的
回收利用,科学家研究利用回收的 制取甲醛,反应的热化学方程式为
制取甲醛,反应的热化学方程式为
 。请回答下列问题:
。请回答下列问题:
(1)已知:①

②相关化学键的键能数据如表所示:
则

___________
(2)一定条件下,将 的混合气体充入恒温恒容的密闭容器中,发生反应
的混合气体充入恒温恒容的密闭容器中,发生反应 。
。
①下列说明反应已经达到平衡状态的是___________ (填选项字母)。
a.容器内气体密度保持不变 b. 的体积分数保持不变
的体积分数保持不变
c.该反应的平衡常数保持不变 d.混合气体的平均相对分子质量不变
②下列措施既能提高 的转化率又能加快反应速率的是
的转化率又能加快反应速率的是___________ (填选项字母)
a.升高温度 b.使用高效催化剂 c.缩小容器体积 d.扩大容器体积 e.及时将产物 分离出体系
分离出体系
(3)实验室在2L密闭容器中进行模拟上述合成 的实验。T℃时,将体积比为1:2的
的实验。T℃时,将体积比为1:2的 和
和 混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
①已知: 则反应开始
则反应开始 内,用
内,用 的压强变化表示该反应的平均反应速率为
的压强变化表示该反应的平均反应速率为___________  。
。
② 时,反应的平衡常数
时,反应的平衡常数 的代数式为
的代数式为
___________  不必化简。
不必化简。 为用各气体分压表示的平衡常数,分压=总压×物质的量分数)。
为用各气体分压表示的平衡常数,分压=总压×物质的量分数)。
③ 时,向体积为
时,向体积为 的恒容密闭容器中充入一定量的
的恒容密闭容器中充入一定量的 和
和 的混合气体,容器内气体压强为
的混合气体,容器内气体压强为 ,反应达到平衡时,
,反应达到平衡时, 的分压与起始的
的分压与起始的 关系如图所示:
关系如图所示:
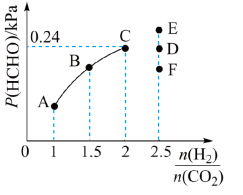
a.当 时,反应达到平衡后,若再向容器中加入
时,反应达到平衡后,若再向容器中加入 和
和 ,使二者分压均增大
,使二者分压均增大 ,则达到新平衡时,
,则达到新平衡时, 的转化率将
的转化率将___________ (填“增大”“减小”或“不变”)。
b.当 时,达到平衡状态后,
时,达到平衡状态后, 的分压可能是图象中的点
的分压可能是图象中的点___________ (填“D”“”E“或”F“),原因为___________ 。
(1)已知:①
②相关化学键的键能数据如表所示:
| 化学键 | |||
| 键能/ | 498 | 436 | 464 |
(2)一定条件下,将
①下列说明反应已经达到平衡状态的是
a.容器内气体密度保持不变 b.
c.该反应的平衡常数保持不变 d.混合气体的平均相对分子质量不变
②下列措施既能提高
a.升高温度 b.使用高效催化剂 c.缩小容器体积 d.扩大容器体积 e.及时将产物
(3)实验室在2L密闭容器中进行模拟上述合成
| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强/kPa | 1.08 | 0.96 | 0.88 | 0.82 | 0.80 | 0.80 | 0.80 |
②
③

a.当
b.当
2023·广东茂名·模拟预测
类题推荐
一定条件下,CH4与CO2反应可制备CH3COOH,反应的热化学方程式为 ,
, 。回答下列问题:
。回答下列问题:
(1)若上述反应在恒容密闭容器中进行,则下列情况能说明反应已经达到平衡状态的是___________(填字母,下同)。
(2)下列措施既能提高CH4的平衡转化率又能加快反应速率的是___________。
(3)T1℃时催化剂作用下,将体积比为1:1的CH4与CO2混合气体充入恒容密闭容器中反应生成CH3COOH(g),每隔一定时间测得容器内气体压强如表所示:
①已知: 。反应开始10 min内,用CH4的压强变化表示该反应的平均反应速率为
。反应开始10 min内,用CH4的压强变化表示该反应的平均反应速率为___________  。
。
② ℃时,反应的平衡常数Kp=
℃时,反应的平衡常数Kp=___________  (Kp为用各气体分压表示的平衡常数,分压
(Kp为用各气体分压表示的平衡常数,分压 总压
总压 物质的量分数)。
物质的量分数)。
(4)用Co作催化剂,可使反应 在较温和条件下进行,反应历程如图:
在较温和条件下进行,反应历程如图:
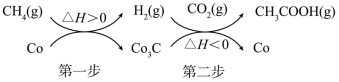
①第二步反应的化学方程式为___________ 。
②为增大CH3COOH的平衡产率:从温度角度考虑,第一步反应在高温下进行,第二步反应在___________ 进行;从H2浓度的角度考虑,第二步应采取的措施是___________ 。
(1)若上述反应在恒容密闭容器中进行,则下列情况能说明反应已经达到平衡状态的是___________(填字母,下同)。
| A.容器内气体密度保持不变 | B.CO2的体积分数保持不变 |
| C.该反应的平衡常数保持不变 | D.混合气体的平均相对分子质量不变 |
| A.升高温度 | B.使用高效催化剂 |
| C.加入CH4 | D.扩大容器体积 |
| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| 压强/kPa | 2 | 1.5 | 1.3 | 1.2 | 1.2 | 1.2 |
②
(4)用Co作催化剂,可使反应

①第二步反应的化学方程式为
②为增大CH3COOH的平衡产率:从温度角度考虑,第一步反应在高温下进行,第二步反应在
CO2、CO是化石燃料燃烧后的主要产物,回收并利用CO2、CO是科学家研究的重要课题。回答下列问题:
(1)CH4-CO2催化重整可以得到CO和H2:CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH
已知:C(s)+2H2(g)=CH4(g)ΔH1
C(s)+O2(g)=CO2(g)ΔH2
C(s)+ O2(g)=CO(g)ΔH3
O2(g)=CO(g)ΔH3
该催化重整反应的ΔH=_______ (用ΔH1、ΔH2和ΔH3表示)。
(2)利用回收的 制取甲醛的反应为CO2(g)+2H2(g)⇌HCHO(g)+H2O(g)
制取甲醛的反应为CO2(g)+2H2(g)⇌HCHO(g)+H2O(g) -6kJmol-1
-6kJmol-1
①一定条件下,将n(CO2):n(H2)=1:2的混合气体充入某恒温恒容的密闭容器中,下列描述能说明反应已达到平衡状态的是_______ (填标号)。
a.单位时间内,断裂1mol的H-H键的,同时生成1mol的H-O键
b. 的体积分数保持不变
的体积分数保持不变
c.混合气体的平均相对分子质量不变
d.气体的密度不变
②为提高上述反应中H2的平衡转化率,可以采取的措施有_______ 、_______ (任写两条)。
③实验室在2L恒容密闭容器中模拟上述合成HCHO的实验。 时将
时将 的
的 和
和 混合气体充入容器中,每隔一定时间测得容器内混合气体压强如表所示:
混合气体充入容器中,每隔一定时间测得容器内混合气体压强如表所示:
已知: 为用B物质的分压变化表示t时间内反应的平均反应速率。0-10min内该反应的平均反应速率vp(H2)为
为用B物质的分压变化表示t时间内反应的平均反应速率。0-10min内该反应的平均反应速率vp(H2)为_______  。10min时,CO2的转化率为
。10min时,CO2的转化率为_______ (保留小数点后一位)。
(3)CO与O2反应过程中存在:CO(g)+O2(g)⇌CO2(g)+O(g) -33.5kJmol-1
-33.5kJmol-1
①已知该反应的正反应速率 ,逆反应速率
,逆反应速率 ,k为速率常数。2500K时,
,k为速率常数。2500K时, ,
, ,则该温度下该反应的平衡常数K为
,则该温度下该反应的平衡常数K为_______ (保留小数点后一位小数)。
②2500K时,若某时刻该反应体系中各物质的浓度满足关系 ,则此时反应
,则此时反应_______ (填“正向”或“逆向”)进行。
(1)CH4-CO2催化重整可以得到CO和H2:CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH
已知:C(s)+2H2(g)=CH4(g)ΔH1
C(s)+O2(g)=CO2(g)ΔH2
C(s)+
该催化重整反应的ΔH=
(2)利用回收的
①一定条件下,将n(CO2):n(H2)=1:2的混合气体充入某恒温恒容的密闭容器中,下列描述能说明反应已达到平衡状态的是
a.单位时间内,断裂1mol的H-H键的,同时生成1mol的H-O键
b.
c.混合气体的平均相对分子质量不变
d.气体的密度不变
②为提高上述反应中H2的平衡转化率,可以采取的措施有
③实验室在2L恒容密闭容器中模拟上述合成HCHO的实验。
| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强/kPa | 1.08 | 0.96 | 0.88 | 0.82 | 0.80 | 0.80 | 0.80 |
已知:
(3)CO与O2反应过程中存在:CO(g)+O2(g)⇌CO2(g)+O(g)
①已知该反应的正反应速率
②2500K时,若某时刻该反应体系中各物质的浓度满足关系
研究碳及其化合物的资源化利用具有重要的意义。回答下列问题:
(1)已知下列热化学方程式:
反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH1=-164.9kJ/mol。
CH4(g)+2H2O(g) ΔH1=-164.9kJ/mol。
反应II:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.2kJ/mol
CO(g)+H2O(g) ΔH2=+41.2kJ/mol
则反应CH4(g)+H2O(g) CO(g)+3H2(g)的ΔH3=
CO(g)+3H2(g)的ΔH3=_______ kJ/mol。
(2)在T°C时,将1molCO2和3molH2加入容积不变的密闭容器中,发生反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g),实验测得CO2的体积分数φ(CO2)如表所示:
CH4(g)+2H2O(g),实验测得CO2的体积分数φ(CO2)如表所示:
①能判断反应CO2(g)+4H2(g) CH4(g)+2H2O(g)达到平衡的是
CH4(g)+2H2O(g)达到平衡的是_______ (填标号)。
A.CO2的消耗速率和CH4的生成速率相等
B.混合气体的密度不再发生变化
C.容器内气体压强不再发生变化
D.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO2的转化率为_______ %(结果保留三位有效数字)。
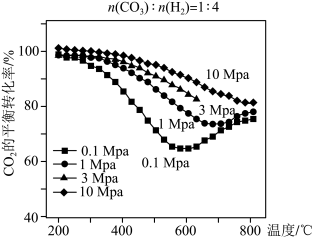
(3)将n(CO2):n(H2)=1:4的混合气体充入密闭容器中发生上述反应I、II,在不同温度和压强时,CO2的平衡转化率如图。0.1MPa时,CO2的转化率在600°C之后,随温度升高而增大的主要原因是_______ 。
(4)在T°C时,向容积为2L的恒容密闭容器中充入1molCO2和一定量的H2发生反应:CO2(g)+2H2(g) =HCHO(g)+H2O(g)。达到平衡时,HCHO的分压与起始
=HCHO(g)+H2O(g)。达到平衡时,HCHO的分压与起始 的关系如图所示:(分压=总压×物质的量分数)
的关系如图所示:(分压=总压×物质的量分数)

①起始时容器内气体的总压强为1.2pkPa,若5min时反应到达c点,v(H2)=_______ mol/(L·min)。
②b点时反应的平衡常数Kp=_______ (kPa)-1(以分压表示)。
③c点时,再加入CO2(g)和H2O(g),使二者分压均增大0.05pkPa,则H2的转化率_______ (填“增大”“不变”或减小”)。
(1)已知下列热化学方程式:
反应I:CO2(g)+4H2(g)
反应II:CO2(g)+H2(g)
则反应CH4(g)+H2O(g)
(2)在T°C时,将1molCO2和3molH2加入容积不变的密闭容器中,发生反应I:CO2(g)+4H2(g)
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| φ(CO2) | 0.25 | 0.23 | 0.214 | 0.202 | 0.200 | 0.200 |
A.CO2的消耗速率和CH4的生成速率相等
B.混合气体的密度不再发生变化
C.容器内气体压强不再发生变化
D.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO2的转化率为
(3)将n(CO2):n(H2)=1:4的混合气体充入密闭容器中发生上述反应I、II,在不同温度和压强时,CO2的平衡转化率如图。0.1MPa时,CO2的转化率在600°C之后,随温度升高而增大的主要原因是

(4)在T°C时,向容积为2L的恒容密闭容器中充入1molCO2和一定量的H2发生反应:CO2(g)+2H2(g)

①起始时容器内气体的总压强为1.2pkPa,若5min时反应到达c点,v(H2)=
②b点时反应的平衡常数Kp=
③c点时,再加入CO2(g)和H2O(g),使二者分压均增大0.05pkPa,则H2的转化率
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


