解答题-实验探究题 适中0.65 引用1 组卷207
50mL 0.50 盐酸与50mL 0.55
盐酸与50mL 0.55 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。回答下列问题:
NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。回答下列问题:

(1)写出该反应的热化学方程式_______ 。(中和反应的反应热 )
)
(2)若将装置中的玻璃搅拌器换成环形铜丝搅拌棒,实验数值结果与57.3 相比
相比_______ (填“偏大”或“偏小”),产生偏差的原因可能是_______ 。
(3)实验操作过程中,实验数据如下表:
上述实验中温度变化的平均值为_______ ℃,若近似认为0.50 稀盐酸与0.55
稀盐酸与0.55 NaOH溶液的密度均为1
NaOH溶液的密度均为1 ,反应所得溶液的比热容
,反应所得溶液的比热容 ,则中和热△H的数值为
,则中和热△H的数值为_______  (保留1位小数)。
(保留1位小数)。
(4)如果用0.50 的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将
的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将_______ (填“偏大”、“偏小”、“不变”),原因是_______ 。
(5)实验中改用60mL 0.5 盐酸跟50mL 0.55
盐酸跟50mL 0.55 NaOH溶液进行反应,调整反应物用量后所放出的热量与原实验
NaOH溶液进行反应,调整反应物用量后所放出的热量与原实验_______ (填“相等”或“不相等”,下同),所求中和反应反应热与原实验_______ ,简述理由:_______ 。

(1)写出该反应的热化学方程式
(2)若将装置中的玻璃搅拌器换成环形铜丝搅拌棒,实验数值结果与57.3
(3)实验操作过程中,实验数据如下表:
| 温度 实验次数 | 起始温度 | 终止温度 | ||
| HCl | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 29.4 |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 |
| 3 | 25.9 | 25.9 | 25.9 | 29.4 |
| 4 | 26.4 | 26.2 | 26.3 | 29.7 |
(4)如果用0.50
(5)实验中改用60mL 0.5
22-23高一下·河北张家口·阶段练习
类题推荐
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液在如图装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
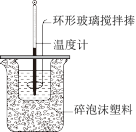
(1)环形玻璃搅拌棒的作用是___________ 。
(2)中和反应放出的热量会造成少量盐酸在反应中挥发,则测得的中和热的数值___________ (填“偏大”、“偏小”或“不变”)。
(3)该实验小组做了三次实验,每次取溶液各50mL,并将实验数据记录如下:
已知盐酸、NaOH溶液的密度与水相同,中和后生成的溶液的比热容 ,则该反应的中和热∆H=
,则该反应的中和热∆H=___________ 。
(4)根据上表中的数据,写出该反应的热化学方程式:___________ 。
(5)在中和热测定实验中,测量起始温度时需要两个温度计,如果只用一个温度计测量,则测得的中和热的数值___________ (填“偏大”、“偏小”或“不变”)。

(1)环形玻璃搅拌棒的作用是
(2)中和反应放出的热量会造成少量盐酸在反应中挥发,则测得的中和热的数值
(3)该实验小组做了三次实验,每次取溶液各50mL,并将实验数据记录如下:
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差(t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.8 | 6.8 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 32.0 | 6.9 |
(4)根据上表中的数据,写出该反应的热化学方程式:
(5)在中和热测定实验中,测量起始温度时需要两个温度计,如果只用一个温度计测量,则测得的中和热的数值
中和热的测定实验中取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL进行中和热的测定实验,装置图如下,回答下列问题:
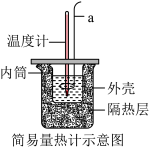
(1)仪器a的名称为环形玻璃搅拌棒,___________ 换成铜棒(填“能”或“不能”)。
(2)该实验共做了4组,第___________ 组数据比较异常,应该舍弃,采用剩下的了组数据进行计算。近似认为0.55mol/LNaOH溶液和0.50mol/L盐酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g ℃)。则中和热
℃)。则中和热 =
=___________ (取小数点后一位)。
(3)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是___________ 。(写一个原因即可)
(4)若改用60mL0.50 HCl和50mL0.55
HCl和50mL0.55 NaOH溶液进行反应与上述实验相比,所放出的热量
NaOH溶液进行反应与上述实验相比,所放出的热量___________ (填“相等”、“不相等”),用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和反应的反应热绝对值会___________ (填“偏大“偏小”或“无影响”)。

(1)仪器a的名称为环形玻璃搅拌棒,
(2)该实验共做了4组,第
| 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | ||
| HCl | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 |
| 4 | 26.4 | 26.3 | 26.3 | 29.8 |
(4)若改用60mL0.50
50mL 1.0mol•L-1盐酸跟 50mL 1.1mol•L-1氢氧化钠溶液在图 1 装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热。试回答下列问题:
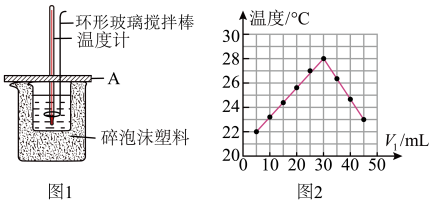
(1)写出该反应的中和热热化学方程式:___________ 。
(2)___________ (填“能”或“不能”)将环形玻璃搅拌棒改为环形铜棒,其原因是_____ 。
(3)如果改用 60mL 1.0mol•L-1盐酸跟 50mL 1.1mol•L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量_____ (“增加”、“减少”或“不变”),所求中和热数值_____ (“增加”、“减少”或“不变”)。
(4)某研究小组将装置完善后,把 V1 mL 1.0mol/L HCl 溶液和 V2 mL 未知浓度的 NaOH 溶液混合均匀后测量并记录溶液温度,实验结果如图 2 所示(实验中始终保持 V1+V2 = 50mL)。回答下列问题:研究小组做该实验时环境温度_________ (填“高于”、“低于”或“等于”)22℃。
(5)①请填写下表中的空白:
②近似认为 50mL 1.0mol•L-1盐酸跟 50mL 1.1mol•L-1氢氧化钠溶液的密度都是 1 g/cm3,中和后生成溶液的比热容 c=4.18 J/(g·℃)。则中和热Δ H=_________ ( 取小数点后一位)。

(1)写出该反应的中和热热化学方程式:
(2)
(3)如果改用 60mL 1.0mol•L-1盐酸跟 50mL 1.1mol•L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量
(4)某研究小组将装置完善后,把 V1 mL 1.0mol/L HCl 溶液和 V2 mL 未知浓度的 NaOH 溶液混合均匀后测量并记录溶液温度,实验结果如图 2 所示(实验中始终保持 V1+V2 = 50mL)。回答下列问题:研究小组做该实验时环境温度
(5)①请填写下表中的空白:
| 温度 实验次数 | 起始温度 t1℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 32.9 | |
| 2 | 27.0 | 27.4 | 27.2 | 37.0 | |
| 3 | 25.9 | 25.9 | 25.9 | 32.5 | |
| 4 | 26.4 | 26.2 | 26.3 | 33.3 | |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


