填空题 适中0.65 引用2 组卷142
化学反应方向的综合判据是判断反应能否白专进行的关键。由于反应的焓变、熵变随温度的变化较小,假设它们不随温度变化,根据下表数据。
(1)根据表中数据可知:反应①在______ 下(填“高温”、“低温”、“任何温度)正向能自发进行。
(2)有人提出采用适当的催化剂,用热分解法分解CO2,以减少CO2的排放,你认为是否可行?___________ (填“是”或“否”)。阐述判断的理由___________ 。
(3)利用综合判据,计算反应③能正向自发进行的温度范围___________ 。(写出过程)
| 化学反应 | AH/kJ·mol—1 | |
| ① | -98 | 57.2 |
| ② | 393.5 | -2.86 |
| ③ | -176 | -285 |
(2)有人提出采用适当的催化剂,用热分解法分解CO2,以减少CO2的排放,你认为是否可行?
(3)利用综合判据,计算反应③能正向自发进行的温度范围
22-23高二下·上海闵行·期末
类题推荐
工业上可采用丙烯氨氧化法制丙烯脂,回答下列问题:
I.丙烯的制备反应方程式为C3H8(g)=C3H6(g)+H2(g)。
已知:部分共价键的键能如下:
(1)制备丙烯反应的△H=__ 。该反应在__ (“高温”或“低温”)下有利于自发进行。
(2)提高丙烯产率可以选择__ (填序号)。
A.升温 B.减小压强 C.充入H2(恒容) D.加入催化剂
(3)已知:CO2(g)+H2(g)=CO(g)+H2O(g) ∆H=-41kJ·mol-1,工业上选择向反应体系中加入CO2,提高丙烷的转化率,从化学平衡原理角度说明原因:__ 。
II.利用丙烯制备丙烯腈,反应方程式如下:2C3H6(g)+2NH3(g)+3O2(g) 2CH2=CHCN(g)+6H2O(l) ∆H=-1294kJ·mol-1。
2CH2=CHCN(g)+6H2O(l) ∆H=-1294kJ·mol-1。
(4)主要的反应机理如下:
CH3-CH=CH2→[CH2 CH
CH CH2]+H 慢 ∆H>0
CH2]+H 慢 ∆H>0
[CH2 CH
CH CH2]+[NH]→CH2=CH-CN+3H 快
CH2]+[NH]→CH2=CH-CN+3H 快
如图能表示反应历程的是__ (填序号)。.
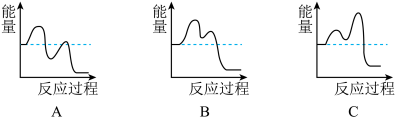
(5)一定温度下,IL恒容密闭容器中充人等物质的量的C3H6、NH3、O2制备丙烯腈,c(C3H6)与v正随时间变化的数据如下表:
①判断t4时刻反应是否已经达到平衡状态并说明理由:__ 。
②列式并计算制备丙烯腈反应的平衡常数K=__ (mol·L-1)-5。
③已知:正反应速率v正=kca(C3H6),根据表中数据,a=__ 。
I.丙烯的制备反应方程式为C3H8(g)=C3H6(g)+H2(g)。
已知:部分共价键的键能如下:
| 共价键 | C—H | C—C | C | H—H |
| 键能(kJ | 414 | 346 | 602 | 436 |
(2)提高丙烯产率可以选择
A.升温 B.减小压强 C.充入H2(恒容) D.加入催化剂
(3)已知:CO2(g)+H2(g)=CO(g)+H2O(g) ∆H=-41kJ·mol-1,工业上选择向反应体系中加入CO2,提高丙烷的转化率,从化学平衡原理角度说明原因:
II.利用丙烯制备丙烯腈,反应方程式如下:2C3H6(g)+2NH3(g)+3O2(g)
 2CH2=CHCN(g)+6H2O(l) ∆H=-1294kJ·mol-1。
2CH2=CHCN(g)+6H2O(l) ∆H=-1294kJ·mol-1。(4)主要的反应机理如下:
CH3-CH=CH2→[CH2
 CH
CH CH2]+H 慢 ∆H>0
CH2]+H 慢 ∆H>0[CH2
 CH
CH CH2]+[NH]→CH2=CH-CN+3H 快
CH2]+[NH]→CH2=CH-CN+3H 快如图能表示反应历程的是

(5)一定温度下,IL恒容密闭容器中充人等物质的量的C3H6、NH3、O2制备丙烯腈,c(C3H6)与v正随时间变化的数据如下表:
| 时间 | 0 | t1 | t2 | t3 | t4 | t5 |
| c(C3H6)/(mol | 1.00 | 0.70 | 0.55 | 0.45 | 0.40 | 0.40 |
| v正 | k | 0.70k | 0.55k | 0.45k | 0.40k | 0.4k |
②列式并计算制备丙烯腈反应的平衡常数K=
③已知:正反应速率v正=kca(C3H6),根据表中数据,a=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


