解答题-无机推断题 较易0.85 引用1 组卷49
完成下列问题。
Ⅰ.短周期元素D、E、X、Y、Z原子序数逐渐增大,它们的最简单氢化物分子空间结构依次是正四面体形、三角锥形、正四面体形、V形、直线形。回答下列问题:
(1)HZO分子的中心原子价层电子对数的计算式为___________ ,该分子的空间结构为___________ 。
(2)Y的价层电子排布式为_________ ,Y的最高价氧化物的VSEPR模型为________ 。
(3)D、E的最简单氢化物的分子空间结构分别是正四面体形与三角锥形,这是因为_______ 。
a.两种分子的中心原子的价层电子对数不同
b.D、E的非金属性不同
c.E的氢化物分子中有一个孤电子对,而D的氢化物分子中没有
Ⅱ.有A、B、C、D、E、F六种主族元素,有关信息如下:
①短周期元素C原子的价电子排布式为ns2np2,E的单质可在空气中燃烧;
②如图是元素周期表中主族元素的一部分:
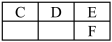
③A、B同周期,其电离能数据如下(单位:kJ·mol-1):
试回答下列问题:
(4)F原子的核外电子排布式为___________ 。
(5)C、D、E元素的电负性相对大小为___________ (用元素符号表示)。
(6)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是______ (填字母)。
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3∶2
Ⅰ.短周期元素D、E、X、Y、Z原子序数逐渐增大,它们的最简单氢化物分子空间结构依次是正四面体形、三角锥形、正四面体形、V形、直线形。回答下列问题:
(1)HZO分子的中心原子价层电子对数的计算式为
(2)Y的价层电子排布式为
(3)D、E的最简单氢化物的分子空间结构分别是正四面体形与三角锥形,这是因为
a.两种分子的中心原子的价层电子对数不同
b.D、E的非金属性不同
c.E的氢化物分子中有一个孤电子对,而D的氢化物分子中没有
Ⅱ.有A、B、C、D、E、F六种主族元素,有关信息如下:
①短周期元素C原子的价电子排布式为ns2np2,E的单质可在空气中燃烧;
②如图是元素周期表中主族元素的一部分:

③A、B同周期,其电离能数据如下(单位:kJ·mol-1):
| I1 | I2 | I3 | I4 | |
| A | 738 | 1 451 | 7 733 | 10 540 |
| B | 578 | 1 817 | 2 745 | 11 575 |
(4)F原子的核外电子排布式为
(5)C、D、E元素的电负性相对大小为
(6)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3∶2
21-22高二下·广东湛江·周测
类题推荐
有A、B、C、D、E、F六种主族元素,有关信息如下:
①短周期元素C原子的价电子排布式为:ns2np2,E的单质可在空气中燃烧;
②下表是元素周期表中主族元素的一部分:
③A、B同周期,其电离能数据如下(单位:kJ·mol-1):
试回答下列问题:
(1)F原子的核外电子排布式为__________________ 。
(2)C、D、E元素的电负性相对大小为____________________ (用元素符号表示)。
(3)C的最高价氧化物与烧碱溶液反应的离子方程式为_______________________ 。
(4)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是________ (填序号)。
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3:2
①短周期元素C原子的价电子排布式为:ns2np2,E的单质可在空气中燃烧;
②下表是元素周期表中主族元素的一部分:
| C | D | E |
| F |
| I1 | I2 | I3 | I4 | |
| A | 738 | 1451 | 7733 | 10540 |
| B | 578 | 1817 | 2745 | 11575 |
(1)F原子的核外电子排布式为
(2)C、D、E元素的电负性相对大小为
(3)C的最高价氧化物与烧碱溶液反应的离子方程式为
(4)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3:2
A、B、C、D、E、F、G是元素周期表前四周期常见元素,有关信息如下:
①E、F同周期,其电离能数据如下(单位:kJ·mol-1):
②短周期元素A原子的价电子排布式为ns2np2,D的单质可在C的单质中燃烧;
③元素周期表中主族元素的一部分如图;
④元素G最大能层符号为N,有4个单电子。
试回答下列问题:
(1)A在周期表中的位置为_______ 。
(2)基态D原子的核外电子排布式为_______ ,其能量最高的轨道呈_______ 形。
(3)A、B、C三种元素的第一电离能由大到小的顺序为_______ (用元素符号表示)。
(4)元素B与元素M在周期表中的位置呈现对角线关系,已知元素B、M的电负性分别为3.0和1.8,则它们形成的化合物是_______ (填“离子化合物”或“共价化合物”)。
(5)化合价是元素的一种性质,由E、F的电离能数据判断下列说法正确的是_______ (填标号)。
aE通常显十1价,F通常显+4价
b.元素F的第一电离能较小,其活泼性比E强
c.E、F的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3:2
(6)元素G位于周期表的_______ 区,该元素可形成G2+、G3+,其中较稳定的是G3+,原因是_______ 。
(7)由A、B、C、D四种元素中的某种元素与氢元素组成的三角锥形分子R和由以上某种元素组成的分子P反应,生成一种V型分子L和一种分子Q,反应如图所示,该反应的化学方程式是_______ 。

①E、F同周期,其电离能数据如下(单位:kJ·mol-1):
| I1 | I2 | I3 | I4 | |
| E | 738 | 1451 | 7733 | 10540 |
| F | 578 | 1817 | 2745 | 11575 |
②短周期元素A原子的价电子排布式为ns2np2,D的单质可在C的单质中燃烧;
③元素周期表中主族元素的一部分如图;
| A | B | C |
| D |
④元素G最大能层符号为N,有4个单电子。
试回答下列问题:
(1)A在周期表中的位置为
(2)基态D原子的核外电子排布式为
(3)A、B、C三种元素的第一电离能由大到小的顺序为
(4)元素B与元素M在周期表中的位置呈现对角线关系,已知元素B、M的电负性分别为3.0和1.8,则它们形成的化合物是
(5)化合价是元素的一种性质,由E、F的电离能数据判断下列说法正确的是
aE通常显十1价,F通常显+4价
b.元素F的第一电离能较小,其活泼性比E强
c.E、F的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3:2
(6)元素G位于周期表的
(7)由A、B、C、D四种元素中的某种元素与氢元素组成的三角锥形分子R和由以上某种元素组成的分子P反应,生成一种V型分子L和一种分子Q,反应如图所示,该反应的化学方程式是

有A、B、C、D、E、F六种主族元素,有关信息如下:
①A、B同周期,其电离能数据如下(单位:kJ•mol-1):
②短周期元素C原子的价电子排布式为:ns2np2,E的单质可在空气中燃烧;
③如图是元素周期表中主族元素的一部分:
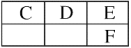
试回答下列问题:
(1)D在周期表的位置___ 。
(2)F原子的简化电子排布式为__ 。
(3)E、F可以与氢形成化合物,该化合物中键能H—E___ H—F(填“>”“<”或“=”)。
(4)C元素基态原子核外最高能级的电子自旋状态__ (填“相同”或“相反”)。
(5)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是__ (填字母)。
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3:2
(6)E在空气中燃烧的产物是一种有毒气体,实验室经常用NaOH进行处理,若所得溶液中只有一种溶质且能促进水的电离,该溶液中离子浓度的大小关系是___ 。
①A、B同周期,其电离能数据如下(单位:kJ•mol-1):
| I1 | I2 | I3 | I4 | |
| A | 738 | 1451 | 7733 | 10540 |
| B | 578 | 1817 | 2745 | 11575 |
③如图是元素周期表中主族元素的一部分:

试回答下列问题:
(1)D在周期表的位置
(2)F原子的简化电子排布式为
(3)E、F可以与氢形成化合物,该化合物中键能H—E
(4)C元素基态原子核外最高能级的电子自旋状态
(5)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3:2
(6)E在空气中燃烧的产物是一种有毒气体,实验室经常用NaOH进行处理,若所得溶液中只有一种溶质且能促进水的电离,该溶液中离子浓度的大小关系是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


