解答题-原理综合题 适中0.65 引用1 组卷90
CO2大量排放会加剧温室效应。自然界的光合作用将二氧化碳转化为有机物,同时人们也在研究将CO2转化为高附加值的燃料,进而缓解能源和环境的双重危机。
Ⅰ.已知25℃,101kPa时:
①CO2(g)与H2O(l)经过光合作用生成1mol葡萄糖[C6H12O6(s)]和O2(g),吸收2804kJ能量。
②H2(g)的燃烧热为285.5kJ/mol
③H2O(l)=H2O(g) ∆H=+44kJ/mol。
(1)葡萄糖[C6H12O6(s)]的燃烧热的热化学方程式为___________ 。
(2)2H2(g)+O2(g)═2H2O(g) ∆H=___________ 。
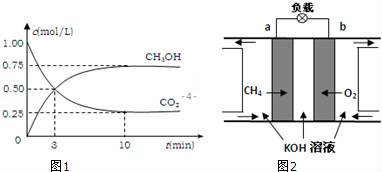
Ⅱ.用H2还原CO2可以在一定条件下合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H<0
(3)某温度下,在恒容密闭容器中发生可逆反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。下列情况能说明该反应一定达到化学平衡的是___________ (填字母)。
a.H2的含量保持不变 b.υ(CO2)∶υ(H2)=1∶3
c.体系的压强不再发生变化 d.混合气体的密度不变
(4)提高甲醇的平衡产率采取的措施为___________ (填字母)
a.升高温度 b.降低温度 c.增大压强 d.降低压强
(5)某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为1mol/L和2mol/L,反应平衡时,CO2的转化率为50%,该温度下反应的平衡常数为___________ 。
Ⅲ.我国科学家研究出一种电化学的方法,可以实现将CO2转化为C2H4,装置如图所示。
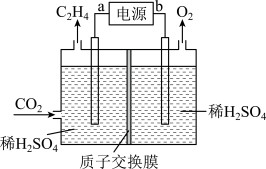
(6)b为电源的___________ (填“正极”或“负极”),阴极的电极反应式为___________ ,生成的C2H4和O2的质量之比为___________ (最简整数比)。
Ⅰ.已知25℃,101kPa时:
①CO2(g)与H2O(l)经过光合作用生成1mol葡萄糖[C6H12O6(s)]和O2(g),吸收2804kJ能量。
②H2(g)的燃烧热为285.5kJ/mol
③H2O(l)=H2O(g) ∆H=+44kJ/mol。
(1)葡萄糖[C6H12O6(s)]的燃烧热的热化学方程式为
(2)2H2(g)+O2(g)═2H2O(g) ∆H=
Ⅱ.用H2还原CO2可以在一定条件下合成CH3OH:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H<0
(3)某温度下,在恒容密闭容器中发生可逆反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。下列情况能说明该反应一定达到化学平衡的是
a.H2的含量保持不变 b.υ(CO2)∶υ(H2)=1∶3
c.体系的压强不再发生变化 d.混合气体的密度不变
(4)提高甲醇的平衡产率采取的措施为
a.升高温度 b.降低温度 c.增大压强 d.降低压强
(5)某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为1mol/L和2mol/L,反应平衡时,CO2的转化率为50%,该温度下反应的平衡常数为
Ⅲ.我国科学家研究出一种电化学的方法,可以实现将CO2转化为C2H4,装置如图所示。

(6)b为电源的
22-23高二下·安徽马鞍山·期末
类题推荐
当今世界多国相继规划了碳达峰、碳中和的时间节点,中国承诺2030年前,二氧化碳的排放不再增长,达到峰值之后逐步降低。2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。因此,降低空气中二氧化碳含量成为研究热点,其中研发二氧化碳的利用技术,将二氧化碳转化为能源是缓解环境和解决能源问题的方案之一、
Ⅰ.二氧化碳在一定条件下转化为甲烷,其反应过程如下图所示。
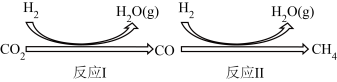
已知:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔHl=-205kJ∙mol-1
反应Ⅱ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH2=-246kJ∙mol-1
(1)则反应Ⅰ的热化学方程式为___________ 。
(2)一定条件下,向2L恒容密闭容器中加入1molCO2和5molH2,只发生上述反应Ⅰ和反应Ⅱ;10min后容器内总压强(P)不再变化,容器中CH4为0.6mol,CO2为0.2mol,H2O为1.4mol,10min内H2的平均反应速率
___________ ,CH4的体积分数=___________ 。
Ⅱ.在催化剂作用下CO2加氢还可制得甲醇。
(3)能说明反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=+50kJ∙mol-1已达平衡状态的是___________(填字母)。
Ⅲ.催化重整制备CH3OCH3的过程中存在反应:
①2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ΔH<0;
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0。
(4)向密闭容器中以物质的量之比为1∶3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、P3由大到小的顺序为___________ ;T2℃时主要发生反应________ (填“①”或“②”)。
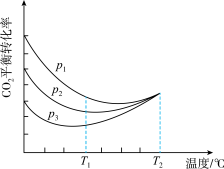
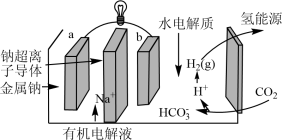
(5)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。系统工作时,a极为________ 极,b极区的电极反应式为___________ 。
Ⅰ.二氧化碳在一定条件下转化为甲烷,其反应过程如下图所示。

已知:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔHl=-205kJ∙mol-1
反应Ⅱ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH2=-246kJ∙mol-1
(1)则反应Ⅰ的热化学方程式为
(2)一定条件下,向2L恒容密闭容器中加入1molCO2和5molH2,只发生上述反应Ⅰ和反应Ⅱ;10min后容器内总压强(P)不再变化,容器中CH4为0.6mol,CO2为0.2mol,H2O为1.4mol,10min内H2的平均反应速率
Ⅱ.在催化剂作用下CO2加氢还可制得甲醇。
(3)能说明反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=+50kJ∙mol-1已达平衡状态的是___________(填字母)。
| A.单位时间内生成1molCH3OH(g)的同时消耗了3molH2(g) |
| B.在恒温恒容的容器中,混合气体的密度保持不变 |
| C.在绝热恒容的容器中,反应的平衡常数不再变化 |
| D.在恒温恒压的容器中,气体的平均摩尔质量不再变化 |
Ⅲ.催化重整制备CH3OCH3的过程中存在反应:
①2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ΔH<0;
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0。
(4)向密闭容器中以物质的量之比为1∶3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、P3由大到小的顺序为

(5)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。系统工作时,a极为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


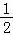 O2(g)+2e﹣
O2(g)+2e﹣ CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)