填空题 较难0.4 引用1 组卷418
钇是稀土元素之一。我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),用NaOH初步处理钇矿石可以得到Y(OH)3、Fe2O3、Na2SiO3和Na2BeO2的共熔物。工业上利用该共熔物制取氧化钇,并获得副产物铍,流程如图:
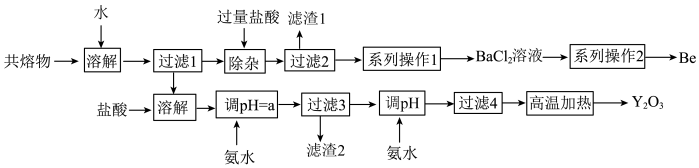
已知i.铍和铝处于元素周期表的对角线位置,化学性质相似;
ii.Fe3+、Y3+形成氢氧化物沉淀时的pH如表:
(1)滤渣1的主要成分是_______ 。
(2)过滤2所得滤液中含有NaCl、BeCl2和少量HCl。为提纯BeCl2。选择合理步骤并排序完成系列操作1_______ 。
a.加入适量的盐酸
b.通入过量的CO2
c.过滤
d.加入过量的NaOH溶液
e.加入过量的氨水
f.洗涤
(3)由BeCl2溶液制得BeCl2固体的操作为_______ 。
(4)用氨水调节pH=a时,a的取值范围是_______ 。
(5)计算常温下Y3++3H2O Y(OH)3+3H+的平衡常数K=
Y(OH)3+3H+的平衡常数K=_______ 。(常温下Ksp[Y(OH)3]=8.0×10-23)
(6)“除杂”中Na2BeO2与过量盐酸反应的离子方程式为_______ 。
(7)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并说明理由_______ 。

已知i.铍和铝处于元素周期表的对角线位置,化学性质相似;
ii.Fe3+、Y3+形成氢氧化物沉淀时的pH如表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.0 | 8.3 |
(2)过滤2所得滤液中含有NaCl、BeCl2和少量HCl。为提纯BeCl2。选择合理步骤并排序完成系列操作1
a.加入适量的盐酸
b.通入过量的CO2
c.过滤
d.加入过量的NaOH溶液
e.加入过量的氨水
f.洗涤
(3)由BeCl2溶液制得BeCl2固体的操作为
(4)用氨水调节pH=a时,a的取值范围是
(5)计算常温下Y3++3H2O
(6)“除杂”中Na2BeO2与过量盐酸反应的离子方程式为
(7)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并说明理由
2023·广西南宁·二模
类题推荐
著名化学家徐光宪在稀土领域贡献突出,被誉为“稀土界的袁隆平”。钇是稀土元素之一,我国蕴藏着丰富的钇矿石 ,工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
,工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
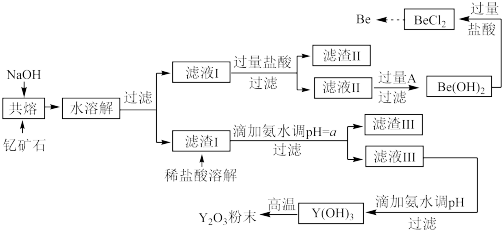
已知:
 钇
钇 的常见化合价为
的常见化合价为 价;
价;
 铍和铝处于元素周期表的对角线位置,化学性质相似;
铍和铝处于元素周期表的对角线位置,化学性质相似;
 、
、 形成氢氧化物沉淀时的pH如下表:
形成氢氧化物沉淀时的pH如下表:
(1)将钇矿石与NaOH共熔的反应方程式补充完整:_____ 。








(2)滤渣II的主要成分是_________ 。
(3)试剂A可以是_________ (填序号)。
A.NaOH溶液 B.氨水 C.CO2 D.CaO
(4)用氨水调节 时,a的取值范围是
时,a的取值范围是_____________ 。
(5)计算常温下 的平衡常数
的平衡常数
____________ 。 常温下
常温下
(6)滤液III加入氨水产生沉淀的离子方程式为___________ 。
(7)从 溶液中得到
溶液中得到 固体的操作是
固体的操作是_______ 。

已知:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2:1 | 3:1 |
| Y3+ | 6.0 | 8.3 |
(2)滤渣II的主要成分是
(3)试剂A可以是
A.NaOH溶液 B.氨水 C.CO2 D.CaO
(4)用氨水调节
(5)计算常温下
(6)滤液III加入氨水产生沉淀的离子方程式为
(7)从
金属钇是稀土元素中含量最丰富的元素之一,主要存在于硅铍钇矿等矿石中。我国蕴藏着丰富的硅铍钇矿(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:
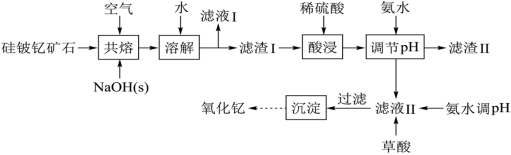
已知:①钇(Y)的常见化合价为+3;
②铍(Be)与铝化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的pH范围如下表:
(假设表中金属离子初始浓度co(Mn+)=0.01mol/L,当溶液中某种离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全)。
请回答下列问题:
(1)用氧化物形式表示硅铍钇矿石组成的化学式_______ 。写出Be的氧化物与氢氧化钠“共熔”时的化学方程式_______ 。
(2)“共熔”时,可选择的容器是_______ (填“石英”、“氧化铝耐高温”或“生铁”)坩埚。“滤液I ”中溶质的主要成分除过量的NaOH外,还有_______ (填化学式)。
(3)沉钇。往“滤液Ⅱ”中先加氨水调节pH = 8.2,此时Y3+转化为Y(OH)3,此时溶液中c(Y3+)为_______ mol • L-1。
(4)实验室洗涤过滤所得Y(OH)3沉淀的操作是_______ 。
(5)滤液I经过一系列处理后,得到无水BeCl2。某同学拟用得到的无水BeCl2制取单质Be,设计用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为_______ 。(已知:混熔时发生反应2NaCl+BeCl2=Na2[BeCl4])

已知:①钇(Y)的常见化合价为+3;
②铍(Be)与铝化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的pH范围如下表:
(假设表中金属离子初始浓度co(Mn+)=0.01mol/L,当溶液中某种离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全)。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.5 | 7.5 |
请回答下列问题:
(1)用氧化物形式表示硅铍钇矿石组成的化学式
(2)“共熔”时,可选择的容器是
(3)沉钇。往“滤液Ⅱ”中先加氨水调节pH = 8.2,此时Y3+转化为Y(OH)3,此时溶液中c(Y3+)为
(4)实验室洗涤过滤所得Y(OH)3沉淀的操作是
(5)滤液I经过一系列处理后,得到无水BeCl2。某同学拟用得到的无水BeCl2制取单质Be,设计用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为
我国是世界上稀土资源最丰富的国家,钇(Y)作为稀土元素之一,在激光材料和超导材料方面有着重要的应用。工业上通过钇矿石(主要成分为Y2FeBe2Si2O10)制取氧化钇和铍的工艺流程如下图所示:

已知:①钇(Y)的常见化合价为+3;
②铍(Be)与铝化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的PH范围如下表:
(假设表中金属离子初始浓度co(Mn+)=0.01mol/L,当溶液中某种离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全)。
(1)Y2FeBe2Si2O10可用氧化物的形式表示为_______ 。
(2)已知将钇矿石与NaOH(s)在高温下共熔,生成的固体产物有Y(OH)3、Fe2O3、Na2SiO3和Na2BeO2,试写出相关的化学反应方程式并配平_______ 。
(3)若向滤液Ⅱ中加入过量的氢氧化钠溶液发生的离子反应有_______ 。
(4)根据表中数据计算常温下Ksp[Y(OH)3]=_______ 。
(5)实验室洗涤过滤所得Y(OH)3沉淀的操作是_______ 。
(6)某同学设计用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为_______ 。

已知:①钇(Y)的常见化合价为+3;
②铍(Be)与铝化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的PH范围如下表:
(假设表中金属离子初始浓度co(Mn+)=0.01mol/L,当溶液中某种离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全)。
离子 | 开始沉淀时的PH | 完全沉淀时的PH |
Fe3+ | 2.1 | 3.1 |
Y3+ | 6.5 | 7.5 |
(1)Y2FeBe2Si2O10可用氧化物的形式表示为
(2)已知将钇矿石与NaOH(s)在高温下共熔,生成的固体产物有Y(OH)3、Fe2O3、Na2SiO3和Na2BeO2,试写出相关的化学反应方程式并配平
(3)若向滤液Ⅱ中加入过量的氢氧化钠溶液发生的离子反应有
(4)根据表中数据计算常温下Ksp[Y(OH)3]=
(5)实验室洗涤过滤所得Y(OH)3沉淀的操作是
(6)某同学设计用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


