解答题-实验探究题 较难0.4 引用1 组卷138
实验小组对硫代硫酸钠( )进行探究。
)进行探究。
Ⅰ.硫代硫酸钠的制备。
实验室将 通入
通入 和
和 混合溶液中可制得
混合溶液中可制得 ,装置如下图:
,装置如下图:
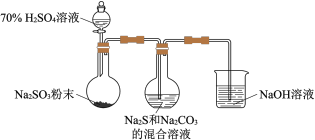
(1)用化学用语解释 和
和 的混合溶液呈碱性的原因:
的混合溶液呈碱性的原因: 、
、_______ 。
(2)为保证 的产量,实验中通入的
的产量,实验中通入的 不能过量,则理论上
不能过量,则理论上 和
和 的最佳物质的量之比应为
的最佳物质的量之比应为_______ 。
Ⅱ.测定样品纯度。
步骤①:准确称取10.00g产品,溶于蒸馏水配成250.00mL溶液。
步骤②:取25.00mL上述溶液注入锥形瓶,加入2~3滴淀粉溶液,用 标准碘溶液滴定。已知:
标准碘溶液滴定。已知: ,回答下列问题:
,回答下列问题:
(3)步骤②中滴定终点的现象为_______ 。
(4)实验数据如表,产品中 的质量分数为
的质量分数为_______ (精确到0.1%)。
(5)下列操作会使样品纯度偏小的是_______ 。
A.读数时,滴定前仰视,滴定后俯视
B.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出
C.滴定管用蒸馏水洗净后,未用标准碘溶液润洗
Ⅲ.小组查阅资料:可视为一个S原子取代了 中的一个О原子。该实验小组运用类比学习的思想预测了的某些性质,并通过实验进行验证。
中的一个О原子。该实验小组运用类比学习的思想预测了的某些性质,并通过实验进行验证。
假设1:从结构角度,与 结构相似,化学性质也相似
结构相似,化学性质也相似
假设2:从化合价角度,与 性质相似
性质相似
(6)实验:用玻璃棒蘸取 溶液点在pH试纸中部,将试纸颜色与标准比色卡对照,发现pH
溶液点在pH试纸中部,将试纸颜色与标准比色卡对照,发现pH_______ 证明假设1不成立;向新制氯水(pH<2)中滴加少量 溶液,观察到
溶液,观察到_______ 证明假设2成立。(反应在25℃下进行)
Ⅰ.硫代硫酸钠的制备。
实验室将

(1)用化学用语解释
(2)为保证
Ⅱ.测定样品纯度。
步骤①:准确称取10.00g产品,溶于蒸馏水配成250.00mL溶液。
步骤②:取25.00mL上述溶液注入锥形瓶,加入2~3滴淀粉溶液,用
(3)步骤②中滴定终点的现象为
(4)实验数据如表,产品中
| 滴定次数 | 滴定前/mL | 滴定后/mL |
| 第一次 | 0.10 | 19.90 |
| 第二次 | 0.25 | 20.25 |
| 第三次 | 0.00 | 20.20 |
A.读数时,滴定前仰视,滴定后俯视
B.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出
C.滴定管用蒸馏水洗净后,未用标准碘溶液润洗
Ⅲ.小组查阅资料:可视为一个S原子取代了
假设1:从结构角度,与
假设2:从化合价角度,与
(6)实验:用玻璃棒蘸取
22-23高二上·福建宁德·期末
类题推荐
硫代硫酸钠(Na2S2O3),又名大苏打,在化学实验中应用广泛。实验室进行如下实验测定某硫代硫酸钠样品的纯度(杂质不参与反应)。
步骤I:准确称取10.00g产品,溶于蒸馏水配成250.00mL溶液。
步骤II:取25.00mL注入锥形瓶,加入指示剂,用0.05mol·L-1标准碘溶液滴定。(已知:2S2O +I2=S4O
+I2=S4O (无色)+2I-),回答下列问题:
(无色)+2I-),回答下列问题:
(1)步骤II中选用的指示剂为____ ,滴定终点的现象为____ 。
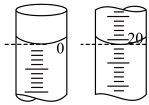
(2)第一次滴定开始和结束时,滴定管中的液面如图,则消耗标准碘溶液的体积为____ mL。
(3)重复上述操作,记录另两次数据如表,则产品中Na2S2O3•5H2O(M=248g/mol)的质量分数为____ (精确到0.1%)。
(4)下列操作会使测得Na2S2O3•5H2O的质量分数偏大的是____ 。
a.用蒸馏水冲洗锥形瓶
b.读数时,滴定前俯视,滴定后仰视
c.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出
d.滴定管用蒸馏水洗净后,未用标准碘溶液润洗
步骤I:准确称取10.00g产品,溶于蒸馏水配成250.00mL溶液。
步骤II:取25.00mL注入锥形瓶,加入指示剂,用0.05mol·L-1标准碘溶液滴定。(已知:2S2O
(1)步骤II中选用的指示剂为
(2)第一次滴定开始和结束时,滴定管中的液面如图,则消耗标准碘溶液的体积为

(3)重复上述操作,记录另两次数据如表,则产品中Na2S2O3•5H2O(M=248g/mol)的质量分数为
| 滴定次数 | 滴定前/mL | 滴定后/mL |
| 第二次 | 0.50 | 19.50 |
| 第三次 | 0.22 | 20.22 |
a.用蒸馏水冲洗锥形瓶
b.读数时,滴定前俯视,滴定后仰视
c.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出
d.滴定管用蒸馏水洗净后,未用标准碘溶液润洗
硫代硫酸钠 ,又名次亚硫酸钠、大苏打、海波,是重要的化工原料。
,又名次亚硫酸钠、大苏打、海波,是重要的化工原料。
Ⅰ.某同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(1)硫代硫酸钠与稀硫酸反应的离子反应方程式为_______ 。
(2)该实验①、②可探究_______ 对反应速率的影响,因此
_______ 、
_______ 。
(3)实验_______ (填实验序号)可探究硫酸浓度对反应速率的影响,因此
_______ 。
Ⅱ.测定某硫代硫酸钠样品的纯度(杂质不参与反应)
准确称取7.00g产品,溶于蒸馏水配成100.00mL溶液,取20.00mL注入锥形瓶,以淀粉作指示剂,用0.10mol/L标准确溶液滴定。已知: 。
。
(4)标准碘溶液应盛放在_______ (填“酸式”或“碱式”)滴定管中。
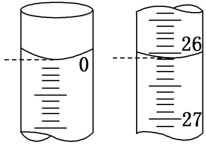
(5)第一次滴定开始和结束时,滴定管中的液面如图,则消耗标准碘溶液的体积为_______ mL。
(6)滴定终点的现象为_______ 。
(7)重复上述操作,记录另两次数据如下,则产品中 的质量分数为
的质量分数为_______ (精确到0.1%)。
(8)下列操作测得 的质量分数偏大的是_______
的质量分数偏大的是_______
Ⅰ.某同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
| 实验 序号 | 反应温度/℃ | 稀硫酸 | ||||
| V/mL | c/mol/L) | V/mL | c/mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | 0.10 | 0.50 | |||
| ③ | 20 | 0.10 | 4.0 | 0.50 | ||
(2)该实验①、②可探究
(3)实验
Ⅱ.测定某硫代硫酸钠样品的纯度(杂质不参与反应)
准确称取7.00g产品,溶于蒸馏水配成100.00mL溶液,取20.00mL注入锥形瓶,以淀粉作指示剂,用0.10mol/L标准确溶液滴定。已知:
(4)标准碘溶液应盛放在
(5)第一次滴定开始和结束时,滴定管中的液面如图,则消耗标准碘溶液的体积为

(6)滴定终点的现象为
(7)重复上述操作,记录另两次数据如下,则产品中
| 滴定次数 | 滴定前/mL | 滴定后/mL |
| 第二次 | 1.56 | 30.30 |
| 第三次 | 0.22 | 26.34 |
| A.滴定前滴定管内有气泡,滴定后气泡消失 |
| B.读取标准碘溶液体积刻度时,滴定前平视,滴定后俯视 |
| C.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出 |
| D.定管用蒸馏水洗净后,直接加入标准碘溶液 |
某学习小组在通过反应Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O研究反应速率的影响因素后,对Na2S2O3产生了兴趣,查资料知Na2S2O3的名称为硫代硫酸钠,可视为一个S原子取代了Na2SO4中的一个O原子。该实验小组运用类比学习的思想预测了Na2S2O3的某些性质,并通过实验探究了自己的预测。
【提出假设】
(1)部分学生认为Na2S2O3与Na2SO4结构相似,化学性质也相似,因此推测室温时Na2S2O3溶液的pH____ 7(填“>”、“=”或“<”)。
(2)部分学生从S元素化合价推测Na2S2O3与Na2SO3性质相似,推测具有较强的______________ 。
【实验探究】取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)。
【实验结论】
(5)从探究①、②的结论:_________________________________________________________ 。
【问题讨论】
(6)甲同学向“探究②”反应后的溶液中滴加AgNO3溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由______________________________ 。
(7)请你重新设计一个实验方案,证明Na2S2O3被氯水氧化,你的方案是______________________________ 。
【提出假设】
(1)部分学生认为Na2S2O3与Na2SO4结构相似,化学性质也相似,因此推测室温时Na2S2O3溶液的pH
(2)部分学生从S元素化合价推测Na2S2O3与Na2SO3性质相似,推测具有较强的
【实验探究】取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)。
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| 探究① | 用玻璃棒蘸取Na2S2O3溶液点在pH试纸中部,将试纸颜色与标准比色卡对照 | 溶液pH=8 | (3) |
| 探究② | 向新制氯水(pH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 | (4) |
(5)从探究①、②的结论:
【问题讨论】
(6)甲同学向“探究②”反应后的溶液中滴加AgNO3溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由
(7)请你重新设计一个实验方案,证明Na2S2O3被氯水氧化,你的方案是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


