解答题-工业流程题 较难0.4 引用2 组卷106
某含镁废弃物中主要含有 ,还含有少量的
,还含有少量的 、
、 ,以该固体废弃物为原料制备
,以该固体废弃物为原料制备 的流程如下:
的流程如下:

已知:部分离子开始沉淀和完全沉淀的
回答下列问题:
(1)滤渣1的主要成分为_______ (填化学式),其阴离子空间构型为_______ 。
(2)“酸浸”时,发生反应的基本反应类型均为_______ ,所使用的稀盐酸的质量浓度为 ,则其物质的量浓度为
,则其物质的量浓度为_______  。
。
(3)“氧化”时,反应的离子方程式为_______ 。
(4)“调 ”时,
”时, 的调节范围为
的调节范围为_______ (滤渣2中有两种氢氧化物)。
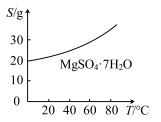
(5)已知 的溶解度曲线如图所示。“操作”应包括
的溶解度曲线如图所示。“操作”应包括_______ 、过滤、洗涤、干燥。
(6)若测定 晶体中结晶水的含量,下列仪器一定不需要的是_______(填字母)。
晶体中结晶水的含量,下列仪器一定不需要的是_______(填字母)。

已知:部分离子开始沉淀和完全沉淀的
| 氢氧化物 | |||
| 开始沉淀时的 | 4.0 | 8.4 | 1.9 |
| 完全沉淀时的 | 5.2 | 11.2 | 3.2 |
(1)滤渣1的主要成分为
(2)“酸浸”时,发生反应的基本反应类型均为
(3)“氧化”时,反应的离子方程式为
(4)“调
(5)已知

(6)若测定
| A | B | C | D |
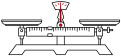 | 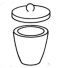 |  |  |
| 天平 | 坩埚 | 马弗炉(一种加热设备) | 分液漏斗 |
| A.A | B.B | C.C | D.D |
22-23高二下·辽宁朝阳·期末
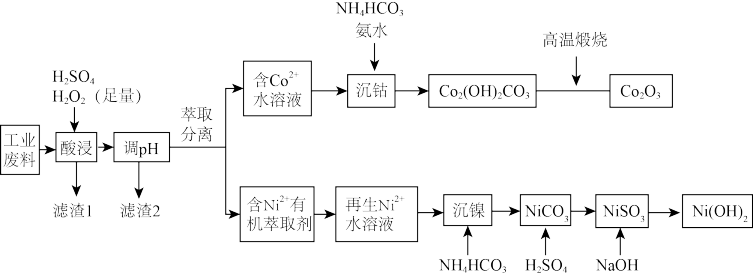
类题推荐 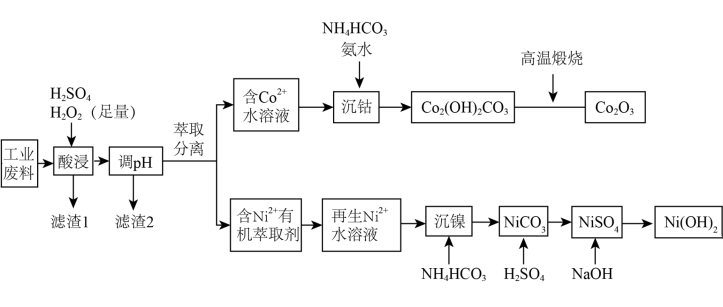 三氧化二钴(Co2O3)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。用某工业含钴废料(主要成分为Co2O3,含有少量PbO、NiO、FeO、SiO2)制备Co2O3和Ni(OH)2的流程如下:
三氧化二钴(Co2O3)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。用某工业含钴废料(主要成分为Co2O3,含有少量PbO、NiO、FeO、SiO2)制备Co2O3和Ni(OH)2的流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH范围如下表:
回答下列问题:
(1)滤渣1的主要成分是___________ (填物质名称);检验滤渣2中阳离子可选用的化学试剂为___________ (填化学式)。
(2)“调pH”时,调节pH的范围是___________ ;“高温煅烧”时,如果是在实验室中进行该项操作,装Co2(OH)2CO3的仪器名称是___________ 。
(3)“酸浸”时H2O2的作用是___________ 。
(4)“沉镍”时发生反应的离子方程式为___________ ;此步骤需加热,温度不能太高也不能太低,原因是___________ 。
碲化锌(ZnTe)可用作半导体和红外材料。以一种锌合金废渣(主要含锌、铝、铜、镁,还含少量铁)制备碲化锌的工艺流程如下:
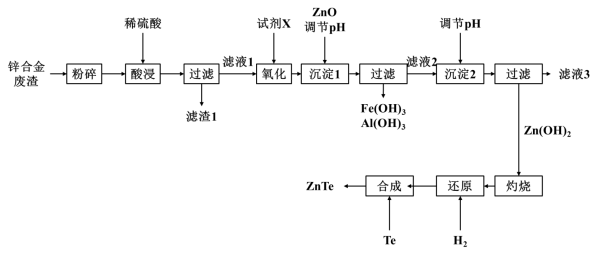
已知:常温下,金属离子开始沉淀和沉淀完全时的pH如下表所示:
请回答下列问题:
(1) Te与O同主族,则Te在元素周期表中的位置是_____________ 。
(2)滤渣1的主要成分是_________ ( 填化学式)。
(3)“灼烧”时,用到的硅酸盐仪器有泥三角、玻璃棒、_______ 、________ 。
(4)“氧化”时,若试剂X为KClO3,则该过程中发生反应的离子方程式为_____________ 。
(5)常温下,“沉淀1”中加ZnO调节pH的范围是_____________ 。
(6)Zn与Al性质相似,其氧化物和氢氧化物都具有两性。常温下“沉淀2”中______ (填“能”或“不能”)加KOH调节pH,其原因是________________ 。

已知:常温下,金属离子开始沉淀和沉淀完全时的pH如下表所示:
| 金属离子 | 开始沉淀pH | 沉淀完全pH |
| Al3+ | 4.1 | 5.0 |
| Fe3+ | 2.2 | 3.5 |
| Mg2+ | 9.6 | 11.6 |
| Zn2+ | 6.5 | 8.5 |
请回答下列问题:
(1) Te与O同主族,则Te在元素周期表中的位置是
(2)滤渣1的主要成分是
(3)“灼烧”时,用到的硅酸盐仪器有泥三角、玻璃棒、
(4)“氧化”时,若试剂X为KClO3,则该过程中发生反应的离子方程式为
(5)常温下,“沉淀1”中加ZnO调节pH的范围是
(6)Zn与Al性质相似,其氧化物和氢氧化物都具有两性。常温下“沉淀2”中
 三氧化二钴(Co2O3)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。用某工业含钴废料(主要成分为Co2O3,含有少量PbO、NiO、FeO、SiO2)制备Co2O3和Ni(OH)2的流程如下:
三氧化二钴(Co2O3)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。用某工业含钴废料(主要成分为Co2O3,含有少量PbO、NiO、FeO、SiO2)制备Co2O3和Ni(OH)2的流程如下:已知:部分阳离子以氢氧化物形式沉淀时溶液的pH范围如下表:
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Co(OH)2 | Ni(OH)2 |
| 开始沉淀时的pH | 7.5 | 2.7 | 7.6 | 6.9 |
| 完全沉淀时的pH | 9.7 | 3.7 | 9.0 | 9.2 |
(1)滤渣1的主要成分是
(2)“调pH”时,调节pH的范围是
(3)“酸浸”时H2O2的作用是
(4)“沉镍”时发生反应的离子方程式为
三氧化二钴( )主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。用某工业含钴废料(主要成分为
)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。用某工业含钴废料(主要成分为 ,含有少量
,含有少量 、
、 、
、 、
、 )制备
)制备 和
和 的流程如下:
的流程如下: 范围如下表:
范围如下表:
回答下列问题:
(1)滤渣1的主要成分是_______ ;检验滤渣2中阳离子可选用的化学试剂为_______ 。
(2)“调 ”时,调节
”时,调节 的范围是
的范围是_______ ;“高温煅烧”时,如果是在实验室中进行该项操作,装 的仪器名称是
的仪器名称是_______ 。
(3)“酸浸”时 的作用是
的作用是_______ 。
(4)“沉镍”时发生反应的离子方程式为_______ ;此步骤需加热,温度不能太高也不能太低,原因是_______ 。
(5) 可用于制备镍氢电池,该电池充电时总反应为
可用于制备镍氢电池,该电池充电时总反应为 (
( 为储氢合金),电解液为
为储氢合金),电解液为 溶液,则放电时正极的电极反应式为
溶液,则放电时正极的电极反应式为_______ 。
| 沉淀物 | ||||
| 开始沉淀时的 | 7.5 | 2.7 | 7.6 | 6.9 |
| 完全沉淀时的 | 9.7 | 3.7 | 9.0 | 9.2 |
(1)滤渣1的主要成分是
(2)“调
(3)“酸浸”时
(4)“沉镍”时发生反应的离子方程式为
(5)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


