解答题-工业流程题 适中0.65 引用2 组卷101
一种由铜镉渣生产金属镉的流程如下:(铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。)
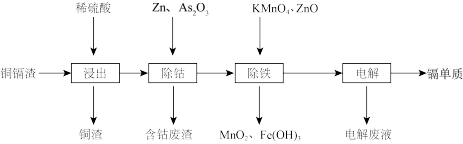
下表列出了相关金属离子生成氢氧化物沉淀的pH
(1)浸出过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出。写出通空气将Cu氧化浸出的离子方程式___________ 。
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3,该微电池的正极反应式为_______ 。
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH。
①除铁过程中,理论上参加反应的物质n(KMnO4):n(Fe2+)=___________ 。
②除铁时加入ZnO控制反应液pH的范围为___________ 。
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证:___________ 。
(5)净化后的溶液可电解获得镉单质。镉的金属性___________ 金属铜(填“强于”或“弱于”)。

下表列出了相关金属离子生成氢氧化物沉淀的pH
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3,该微电池的正极反应式为
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH。
①除铁过程中,理论上参加反应的物质n(KMnO4):n(Fe2+)=
②除铁时加入ZnO控制反应液pH的范围为
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证:
(5)净化后的溶液可电解获得镉单质。镉的金属性
22-23高一下·江苏连云港·阶段练习
类题推荐
湿法炼锌产生的铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质,生产金属镉的工艺流程如下:
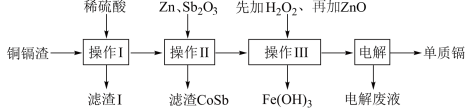
下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1 mol/L)
(1)酸浸时粉碎铜镉渣的目的是__________ 。
(2)操作Ⅰ产生的滤渣主要成分为________ (填化学式)。
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为______ 。
②再加入ZnO控制反应液的pH,pH范围为______ 。
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案鉴别________ 。
(4)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是_________ 。

下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1 mol/L)
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)酸浸时粉碎铜镉渣的目的是
(2)操作Ⅰ产生的滤渣主要成分为
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为
②再加入ZnO控制反应液的pH,pH范围为
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案鉴别
(4)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是
利用湿法炼锌产生的铜镉渣生产金属镉的流程如下:
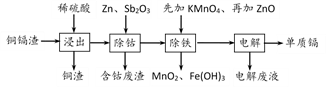
已知:铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
(1)为了提高铜镉渣浸出的速率,可采取的措施有:①适当升高温度;②搅拌;③______ 等。已知浸出的金属离子均为二价,写出浸出钴的化学方程式__________________ 。
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3、Co2+的溶液形成微电池并产生合金CoSb。该微电池的正极反应式为________________________________ 。
(3)除铁的过程分两步进行:
①先加入适量KMnO4,发生反应的离子方程式为______________________________ ,
②再加入ZnO控制反应液的pH范围为_____________ 。
(4)除铁过程第①步,若加入KMnO4时条件控制不当,MnO2会继续反应,造成的结果是______________ ,若加入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证_________________ 。
(5)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是____ 。
(6)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):
Ksp(CdCO3)=5.210-12, Ksp(CdS)=3.610-29,Ksp(Cd(OH)2)=2.010-16,根据上述信息:
沉淀Cd2+效果最佳的试剂是____________ 。
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳pH为11,此时溶液中c(Cd2+)=_________ 。

已知:铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 | 8.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 | 10.6 |
(1)为了提高铜镉渣浸出的速率,可采取的措施有:①适当升高温度;②搅拌;③
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3、Co2+的溶液形成微电池并产生合金CoSb。该微电池的正极反应式为
(3)除铁的过程分两步进行:
①先加入适量KMnO4,发生反应的离子方程式为
②再加入ZnO控制反应液的pH范围为
(4)除铁过程第①步,若加入KMnO4时条件控制不当,MnO2会继续反应,造成的结果是
(5)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是
(6)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):
Ksp(CdCO3)=5.210-12, Ksp(CdS)=3.610-29,Ksp(Cd(OH)2)=2.010-16,根据上述信息:
沉淀Cd2+效果最佳的试剂是
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳pH为11,此时溶液中c(Cd2+)=
我国是世界上最早制得和使用金属锌的国家。湿法炼锌产生的铜镉渣[主要含锌、铜、铁、镉(Cd)等单质]用于生产金属镉的工艺流程如图:
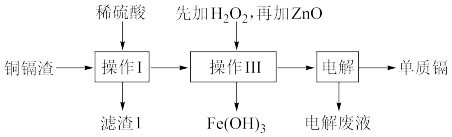
已知:相关金属离子生成氢氧化物沉淀的pH如下表(金属离子的起始浓度为0.1mol·L-1)
(1)操作I、III中都用到过滤操作,实验室中过滤操作适用于分离___________ 。
(2)操作I过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,若通入空气搅拌时,氧化浸出Cu2+的离子方程式为___________ 。
(3)①操作III中先加入适量H2O2,发生反应的离子方程式为___________ 。
②再加入ZnO控制反应液的pH,合适的pH范围为___________ 。
(4)净化后的溶液用惰性电极电解可获得镉单质,电解废液中含有Zn2+,电解废液中可循环利用的溶质是___________ ,说明活泼性Zn___________ Cd(填“>”或“<”)。
(5)该湿法炼锌废水中含有Zn2+,排放前需处理。向废水中加入CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2++H2S⇌ZnS(s)+2H+。处理后的废水中部分微粒浓度如下表:
处理后的废水的c(Zn2+)=________ mol∙L-1,pH=________ [已知:Ksp(ZnS)=1.0×10-23,Ka(CH3COOH)=2.0×10-5]

已知:相关金属离子生成氢氧化物沉淀的pH如下表(金属离子的起始浓度为0.1mol·L-1)
| 开始沉淀时pH | 完全沉淀时pH | |
| Cd2+ | 7.0 | 9.4 |
| Fe2+ | 6.3 | 8.3 |
| Fe3+ | 1.5 | 3.2 |
(2)操作I过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,若通入空气搅拌时,氧化浸出Cu2+的离子方程式为
(3)①操作III中先加入适量H2O2,发生反应的离子方程式为
②再加入ZnO控制反应液的pH,合适的pH范围为
(4)净化后的溶液用惰性电极电解可获得镉单质,电解废液中含有Zn2+,电解废液中可循环利用的溶质是
(5)该湿法炼锌废水中含有Zn2+,排放前需处理。向废水中加入CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2++H2S⇌ZnS(s)+2H+。处理后的废水中部分微粒浓度如下表:
| 微粒 | H2S | CH3COOH | CH3COO- | S2- |
| 浓度/mol•L-1 | 0.10 | 0.05 | 0.10 | 1.0×10-12 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


