解答题-原理综合题 适中0.65 引用1 组卷102
以 为原料制备甲烷等能源具有较好的发展前景。
为原料制备甲烷等能源具有较好的发展前景。 催化(固体催化剂)加氢合成甲烷的反应为
催化(固体催化剂)加氢合成甲烷的反应为 。
。
(1)该反应中各化学键的键能数据如表所示:
则生成 可以
可以___________ (填“放出”或“吸收”)___________  热量。
热量。
(2) 加氢制
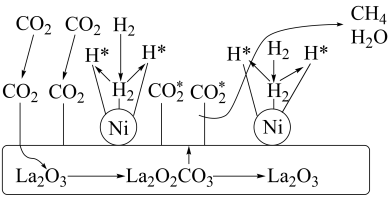
加氢制 的一种催化机理如图,下列说法正确的是___________(填标号)。
的一种催化机理如图,下列说法正确的是___________(填标号)。
(3)保持温度不变,向 的恒容密闭容器中充入
的恒容密闭容器中充入 和
和 ,发生上述反应,若
,发生上述反应,若 后反应达到平衡,此时测得
后反应达到平衡,此时测得 。
。
① 内,
内,
___________  ,
, 的转化率
的转化率
___________ (取整数) 。
。
②下列表述能说明该反应达到平衡状态的是___________ (填标号)。
A.
B.混合气体的密度不再发生改变
C.混合气体的平均相对分子质量不再改变
D.断开 键的同时断开
键的同时断开 键
键
(4)图示装置可以把 蕴含的化学能转化为电能。
蕴含的化学能转化为电能。
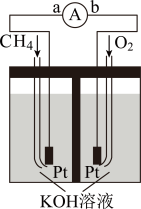
①电池工作时,溶液中的 向
向___________ (填“左”或“右”)移动,负极的电极反应式为___________ 。
②当外电路中转移 电子时,消耗的
电子时,消耗的 的体积是
的体积是___________ L(标准状况下)。
(1)该反应中各化学键的键能数据如表所示:
| 化学键 | C—H | H—O | H—H | |
| 键能 | 750 | 413 | 463 | 436 |
(2)

| A.反应过程中的催化剂为 |
| B. |
| C. |
| D. |
①
②下列表述能说明该反应达到平衡状态的是
A.
B.混合气体的密度不再发生改变
C.混合气体的平均相对分子质量不再改变
D.断开
(4)图示装置可以把

①电池工作时,溶液中的
②当外电路中转移
22-23高一下·河南新乡·期末
类题推荐
以CO2为原料制备甲烷等能源具有较好的发展前景。CO2催化(固体催化剂)加氢合成甲烷的反应为 。
。
(1)该反应中各化学键的键能数据如表所示:
则生成1molH2O(g)可以_______ (填“放出”或“吸收”)_______ kJ热量。
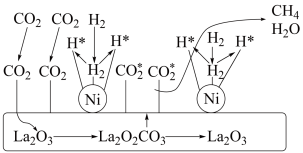
(2)CO2加氢制CH4的一种催化机理如图,下列说法正确的是_______(填标号)。
(3)保持温度不变,向2L的恒容密闭容器中充入4molCO2和12molH2,发生上述反应,若5min后反应达到平衡,此时测得c(H2O)=2.5mol/L。
①0-5min内,v(CO2)=_______ mol·L-1.min-1,H2的转化率为_______ %(取整数)。
②下列表述能说明该反应达到平衡状态的是_______ (填标号)。
A.n(CH4):n(H2O)=1:2
B.混合气体的密度不再发生改变
C.混合气体的平均相对分子质量不再改变
D.生成4molC-H键的同时断开2molC=O键
(4)TiO2-aNb是常见的光学活性物质,由TiO2通过氮掺杂反应生成,表示如下图。
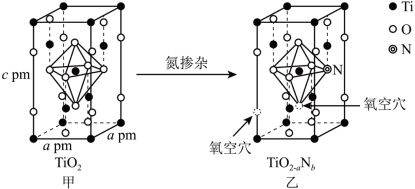
①立方晶系TiO2晶胞参数如图甲所示,其晶体的密度为_______ g·cm-3(写计算式,NA代表阿伏加德罗常数)。
②图乙TiO2-aNb晶体中a:b=_______ 。
(1)该反应中各化学键的键能数据如表所示:
| 化学键 | C=O | C-H | H-O | H-H |
| 键能/(kJ/mol) | 750 | 413 | 463 | 436 |
(2)CO2加氢制CH4的一种催化机理如图,下列说法正确的是_______(填标号)。

| A.反应过程中的催化剂为La2O3和La2O2CO3 |
| B.La2O2CO3可以释放CO2* |
| C.H2经过Ni时,断键裂解产生H*的过程为放热过程 |
| D.CO2加氢制CH4的过程需要La2O3与Ni共同完成 |
①0-5min内,v(CO2)=
②下列表述能说明该反应达到平衡状态的是
A.n(CH4):n(H2O)=1:2
B.混合气体的密度不再发生改变
C.混合气体的平均相对分子质量不再改变
D.生成4molC-H键的同时断开2molC=O键
(4)TiO2-aNb是常见的光学活性物质,由TiO2通过氮掺杂反应生成,表示如下图。

①立方晶系TiO2晶胞参数如图甲所示,其晶体的密度为
②图乙TiO2-aNb晶体中a:b=
甲醇( )是一种重要的有机化工原料,某温度下
)是一种重要的有机化工原料,某温度下 加氢制甲醇的总反应为
加氢制甲醇的总反应为
 ,该反应为放热反应,一定温度下,在容积为2 L的恒容密闭容器中,加入6 mol
,该反应为放热反应,一定温度下,在容积为2 L的恒容密闭容器中,加入6 mol  和8 mol
和8 mol  以及催化剂,测得
以及催化剂,测得 的物质的量随时间变化如表。
的物质的量随时间变化如表。
请回答:
(1)对于该反应,反应物的化学键断裂要吸收的能量______ (填“大于”、“小于”或“等于”)生成物的化学键形成要放出的能量。
(2)①0~5min内,以 表示的该反应速率
表示的该反应速率
______ 。
②达到平衡时, 的转化率为
的转化率为______ (精确到小数点后一位)。
(3)能说明该反应已达到化学平衡状态的是______ (填字母序号)。
A.
B.单位时间内,断开C=O键的数目和断开H—O键的数目相同
C.容器内 时
时
D. 的转化率达到最大值
的转化率达到最大值
E.混合气体的平均相对分子质量不再变化
(4)若以熔融 作为电解质,一极充入甲醇,另一极充入空气和
作为电解质,一极充入甲醇,另一极充入空气和 气体设计成燃料电池。则充入空气和
气体设计成燃料电池。则充入空气和 气体的电极为
气体的电极为______ 极,写出充入甲醇电极的反应式:_____________ 。
时间 | 0 | 5 min | 10 min | 15 min |
| 8.0 | 3.5 | 2.0 | 2.0 |
(1)对于该反应,反应物的化学键断裂要吸收的能量
(2)①0~5min内,以
②达到平衡时,
(3)能说明该反应已达到化学平衡状态的是
A.
B.单位时间内,断开C=O键的数目和断开H—O键的数目相同
C.容器内
D.
E.混合气体的平均相对分子质量不再变化
(4)若以熔融
CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为__ (写离子符号);若所得溶液c(HCO3−):c(CO32−)=2:1,溶液pH=__ 。(室温下,H2CO3的K1=4×10−7;K2=5×10−11)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)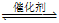 2CO(g)+2H2(g)
2CO(g)+2H2(g)
已知上述反应中相关的化学键键能数据如下:
则该反应的ΔH=__ 。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是__ (填“A”或“B”)。
(3)向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①下列叙述能说明此反应达到平衡状态的是___ 。
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H-H键断裂
②产物甲醇可以用作燃料电池,碱性条件下的甲醇(CH3OH)燃料电池负极反应式:__ 。
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)
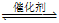 2CO(g)+2H2(g)
2CO(g)+2H2(g)已知上述反应中相关的化学键键能数据如下:
| 化学键 | C—H | C=O | H—H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=
(3)向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)①下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H-H键断裂
②产物甲醇可以用作燃料电池,碱性条件下的甲醇(CH3OH)燃料电池负极反应式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


