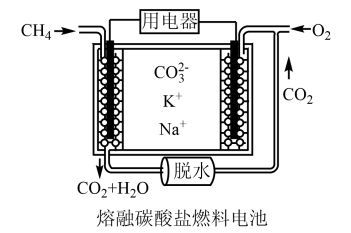
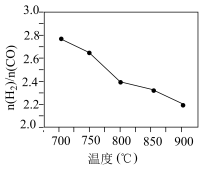
解答题-原理综合题 较难0.4 引用1 组卷295
据国际能源署预测,2050年氢燃料电池汽车的比重将提高至15%。
Ⅰ.天然气(CH4)和H2O重整制氢
反应①:
反应②:
(1)已知 ,相关物质的燃烧热如下表,则
,相关物质的燃烧热如下表,则
___________ 。
(2)700℃时,向一恒容容器中投入1MPaCH4和3MPaH2O,达到平衡时CO、CO2的分压分别为aMPa和bMPa,则反应①的平衡常数
___________ 。
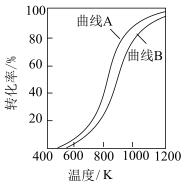
(3)H2的平衡产率随反应温度的变化关系如图1所示。请从平衡移动的角度解释T>600℃时,H2的平衡产率几乎不变的原因___________ 。
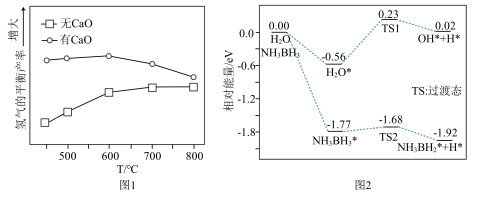
(4)已知反应③: 。研究发现加入适量CaO有利于重整制氢,如图1所示。加入CaO的优点有___________(填字母)。
。研究发现加入适量CaO有利于重整制氢,如图1所示。加入CaO的优点有___________(填字母)。
Ⅱ.氨硼烷(NH3BH3,熔点104℃)水解制氢
(5)1molNH3BH3完全水解可以生成3molH2和一种可溶性的含氧酸盐(N、B均未变价),请写出NH3BH3完全水解的离子反应方程式___________ 。
(6)吉林大学于吉红院士团队研究发现Pt催化剂上NH3BH3的水解速度主要受H2O和NH3BH3脱氢反应的影响,如图2所示。请写出决速步的化学反应方程式___________ 。
Ⅰ.天然气(CH4)和H2O重整制氢
反应①:
反应②:
(1)已知
| 物质 | CH4(g) | CO(g) | H2(g) |
| 燃烧热( | 890.3 | 282.8 | 285.8 |
(3)H2的平衡产率随反应温度的变化关系如图1所示。请从平衡移动的角度解释T>600℃时,H2的平衡产率几乎不变的原因
(4)已知反应③:
| A.促进反应②平衡正向移动,提高H2的平衡产率 | B.消耗CO2,提高H2的纯度 |
| C.反应③放热,为重整体系提供能量 | D.减少CO2排放,有利于碳中和 |

Ⅱ.氨硼烷(NH3BH3,熔点104℃)水解制氢
(5)1molNH3BH3完全水解可以生成3molH2和一种可溶性的含氧酸盐(N、B均未变价),请写出NH3BH3完全水解的离子反应方程式
(6)吉林大学于吉红院士团队研究发现Pt催化剂上NH3BH3的水解速度主要受H2O和NH3BH3脱氢反应的影响,如图2所示。请写出决速步的化学反应方程式
22-23高三下·湖北武汉·阶段练习
类题推荐
甲烷是重要的资源,通过一系列过程可实现由甲烷到氢气的转化。
Ⅰ.500℃时,CH4与H2O重整主要发生下列反应:
反应1:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.1kJ/mol
CO(g)+3H2(g) ΔH=+206.1kJ/mol
反应2:CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
(1)恒温恒容下,不能证明反应体系已达平衡的是_________
(2)已知:CaO(s)+CO2(g)=CaCO3(s) ΔH=-178.8kJ/mol,向重整反应体系中加入适量多孔CaO,其优点是___________ 。
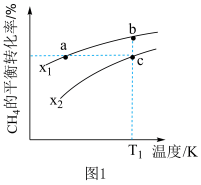
(3)向一恒容密闭容器中加入1molCH4和一定量的H2O,若只发生反应1,CH4的平衡转化率按不同投料x(x= )随温度的变化曲线如图1所示。下列说法不正确的是
)随温度的变化曲线如图1所示。下列说法不正确的是
Ⅱ.CH4与CO2重整的主要反应的热化学方程式为
反应a:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+246.5kJ/mol K1
反应b:H2(g)+CO2(g)=CO(g)+H2O(g) ΔH=+41.2kJ/mol K2
反应c:2CO(g)=CO2(g)+C(s) ΔH=-172.5kJ/mol K3
(4)在CH4与CO2重整体系中通入适量H2O(g),可减少C(s)的生成,反应3CH4(g)+CO2(g)+2H2O(g)=4CO(g)+8H2(g)的ΔH=___________ ,K=___________ (用K1、K2或K3表示)
(5)将1molCH4与1molCO2在2L密闭容器中反应制取CO和H2时,若只发生反应a和反应b,CH4和CO2的平衡转化率随温度变化关系如图2所示。
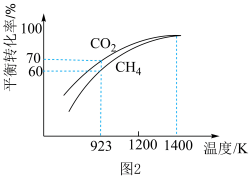
①请列出923K时反应a的化学平衡常数K的计算式(不用计算结果):K=___________ 。
②CH4还原能力R可衡量CO2转化效率,(R= ),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是
),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是___________ 。
Ⅰ.500℃时,CH4与H2O重整主要发生下列反应:
反应1:CH4(g)+H2O(g)
反应2:CO(g)+H2O(g)
(1)恒温恒容下,不能证明反应体系已达平衡的是_________
| A.体系的气体平均相对分子质量不变 |
| B.1molH2O消耗的同时有3molH2消耗 |
| C.体系的压强不再变化 |
| D.CO与H2的物质的量之比不再改变 |
(2)已知:CaO(s)+CO2(g)=CaCO3(s) ΔH=-178.8kJ/mol,向重整反应体系中加入适量多孔CaO,其优点是
(3)向一恒容密闭容器中加入1molCH4和一定量的H2O,若只发生反应1,CH4的平衡转化率按不同投料x(x=

| A.x1>x2 |
| B.点a、b、c对应的平衡常数:Ka<Kb=Kc |
| C.反应速率:vb正<vc正 |
| D.反应温度为T1,当容器内压强不变时,反应达到平衡状态 |
Ⅱ.CH4与CO2重整的主要反应的热化学方程式为
反应a:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+246.5kJ/mol K1
反应b:H2(g)+CO2(g)=CO(g)+H2O(g) ΔH=+41.2kJ/mol K2
反应c:2CO(g)=CO2(g)+C(s) ΔH=-172.5kJ/mol K3
(4)在CH4与CO2重整体系中通入适量H2O(g),可减少C(s)的生成,反应3CH4(g)+CO2(g)+2H2O(g)=4CO(g)+8H2(g)的ΔH=
(5)将1molCH4与1molCO2在2L密闭容器中反应制取CO和H2时,若只发生反应a和反应b,CH4和CO2的平衡转化率随温度变化关系如图2所示。

①请列出923K时反应a的化学平衡常数K的计算式(不用计算结果):K=
②CH4还原能力R可衡量CO2转化效率,(R=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网