解答题-实验探究题 适中0.65 引用1 组卷419
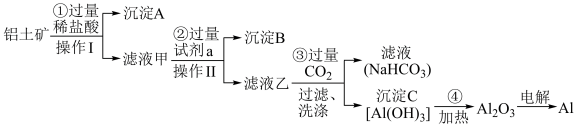
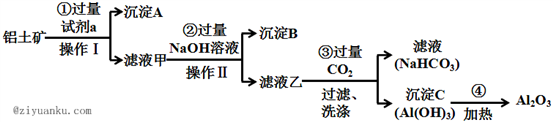
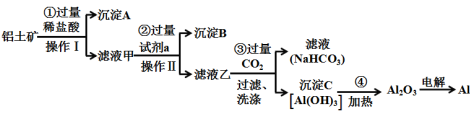
铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
(1)用电解饱和食盐水制备试剂a的化学方程式为___________ ;
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为___________ ;
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是___________ ;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为___________ 。
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________ ;
a.MgO b.V2O5 c.Fe3O4 d.MnO2
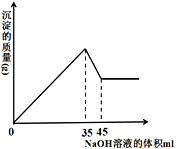
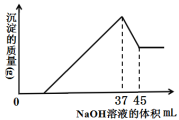
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为___________ 。

(1)用电解饱和食盐水制备试剂a的化学方程式为
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是
a.MgO b.V2O5 c.Fe3O4 d.MnO2
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为

22-23高一下·山东临沂·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网