填空题 适中0.65 引用1 组卷112
金属铝在生产生活中有广泛用途。
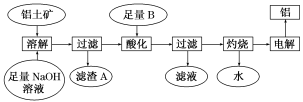
(1)写出工业通过电解法生产铝的化学方程式___________
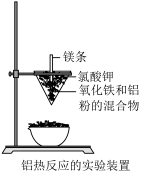
(2)写出该铝热反应的化学方程式___________ ;利用铝热反应在工业上可冶炼___________ 金属(填编号)。
A.强还原性 B.难熔性 C.易导电 D.活泼
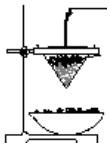
(3)反应结束后,从沙中取出生成的固体物质,该固体可能是铁铝合金,请同学设计实验证明。______
(4)某溶液中含有 0.15mol 的AlCl3,向其中加入 1mol/L 的NaOH溶液,得到沉淀7.8g,加入NaOH溶液的体积为___________ 。

(1)写出工业通过电解法生产铝的化学方程式
(2)写出该铝热反应的化学方程式
A.强还原性 B.难熔性 C.易导电 D.活泼
(3)反应结束后,从沙中取出生成的固体物质,该固体可能是铁铝合金,请同学设计实验证明。
(4)某溶液中含有 0.15mol 的AlCl3,向其中加入 1mol/L 的NaOH溶液,得到沉淀7.8g,加入NaOH溶液的体积为
22-23高一下·上海徐汇·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网