解答题-工业流程题 较难0.4 引用1 组卷255
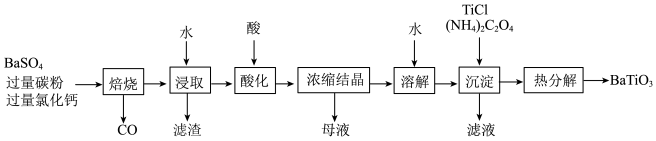
BaTiO3是电子陶瓷工业的支柱。以BaSO4为原料,采用下列路线可制备粉状BaTiO3。
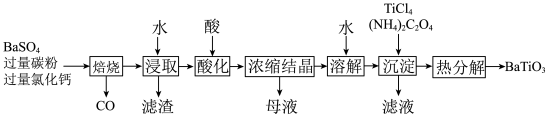
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是___________ 。
(2)“焙烧”后固体产物有BaCl2、易溶于水的BaS和微溶于水的CaS。“浸取”时主要反应的离子方程式为___________ 。
(3)焙烧后的产物不能直接用酸浸取,原因是___________ 。
(4)“沉淀”步骤中生成BaTiO(C2O4)2的化学方程式为___________ 。
(5)隔绝空气条件下,BaTiO(C2O4)2灼烧得到BaTiO3.该反应的化学方程式为___________ 。
(6)测定产品纯度。
取wgBaTiO3产品溶于过量的一定浓度硫酸中配制成250mL溶液(生成TiO2+),取25.00mL溶液于锥形瓶,加入过量V1mLc1mol·L-1(NH4)2Fe(SO4)2溶液,充分反应后,用c2mol·L-1KMnO4溶液滴定至终点消耗KMnO4溶液V2mL。计算产品纯度。(写出必要的计算过程)___________
已知氧化性顺序TiO2+> >Fe3+;2H++TiO2++Fe2+=Fe3++Ti3++H2O。
>Fe3+;2H++TiO2++Fe2+=Fe3++Ti3++H2O。

回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是
(2)“焙烧”后固体产物有BaCl2、易溶于水的BaS和微溶于水的CaS。“浸取”时主要反应的离子方程式为
(3)焙烧后的产物不能直接用酸浸取,原因是
(4)“沉淀”步骤中生成BaTiO(C2O4)2的化学方程式为
(5)隔绝空气条件下,BaTiO(C2O4)2灼烧得到BaTiO3.该反应的化学方程式为
(6)测定产品纯度。
取wgBaTiO3产品溶于过量的一定浓度硫酸中配制成250mL溶液(生成TiO2+),取25.00mL溶液于锥形瓶,加入过量V1mLc1mol·L-1(NH4)2Fe(SO4)2溶液,充分反应后,用c2mol·L-1KMnO4溶液滴定至终点消耗KMnO4溶液V2mL。计算产品纯度。(写出必要的计算过程)
已知氧化性顺序TiO2+>
22-23高一下·江苏南京·期末
类题推荐
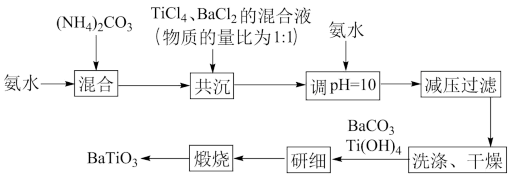
钛酸钡(BaTiO3)被誉为“电子工业的支柱”。某小组设计方案在实验室里制备钛酸钡,简易流程如图(提示:四氯化钛易挥发):
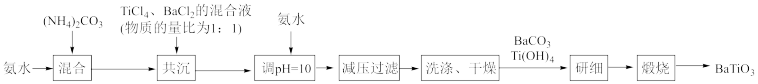
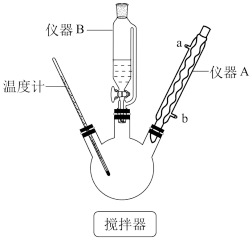
已知:氧化性顺序有Ti4+>MnO >Fe3+,Ti4++Fe2+=Fe3++Ti3+。“共沉”在如图所示装置中完成。
>Fe3+,Ti4++Fe2+=Fe3++Ti3+。“共沉”在如图所示装置中完成。
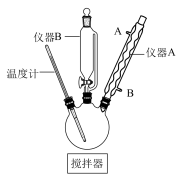
(1)仪器A的作用是___ ;仪器B的名称是___ 。
(2)“减压过滤”中通过抽气实现,其减压的目的是___ 。
(3)“煅烧”发生化学方程式为___ 。
(4)表1、表2为实验过程中不同的反应时间和煅烧时间对产品纯度的影响,则最佳反应时间、煅烧时间分别为___ 、___ 。
表1反应时间对产品纯度的影响
表2煅烧时间对产品纯度的影响
(5)测定产品纯度。取wgBaTiO3产品溶于稍过量的稀硫酸中配制成250mL溶液,取25.00mL溶液于锥形瓶,加入过量V1mLcmol•L-1(NH4)2Fe(SO4)2溶液,充分反应后,用cmol•L-1KMnO4溶液滴定至终点消耗KMnO4溶液V2mL(BaTiO3的相对分子质量为M)。产品纯度为__ %;若滴定管没有用溶液润洗,测得结果会__ (填“偏高”“偏低”或“无影响”)。

已知:氧化性顺序有Ti4+>MnO

(1)仪器A的作用是
(2)“减压过滤”中通过抽气实现,其减压的目的是
(3)“煅烧”发生化学方程式为
(4)表1、表2为实验过程中不同的反应时间和煅烧时间对产品纯度的影响,则最佳反应时间、煅烧时间分别为
表1反应时间对产品纯度的影响
| 反应时间/h | 产品纯度/% |
| 1 | 95.04 |
| 2 | 96.98 |
| 3 | 98.29 |
| 4 | 99.38 |
| 5 | 99.35 |
| 煅烧时间/h | 产品纯度/% |
| 1 | 95.42 |
| 2 | 97.46 |
| 3 | 98.98 |
| 4 | 99.46 |
| 5 | 99.43 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网