解答题-原理综合题 较难0.4 引用2 组卷398
2030年实现“碳达峰”,2060年达到“碳中和”的承诺,体现了我国的大国风范。二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
二氧化碳加氢制甲醇涉及的反应可表示为:
①

②

③

(1)根据上述反应求:④ 的
的
___________  。
。
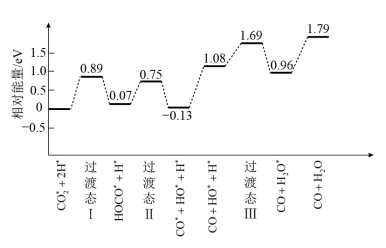
(2)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上反应④的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。
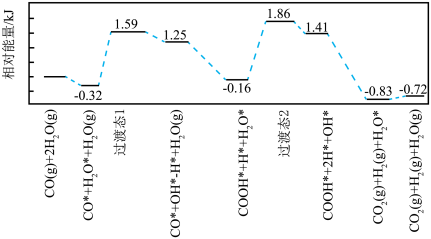
写出该历程中决速步骤的化学方程式:________ 。
(3)一体积可变的密闭容器中,在保持a MPa下,按照 投料,平衡时,CO和CH3OH在含碳产物中物质的量分数及CO2的转化率随温度的变化如图所示:
投料,平衡时,CO和CH3OH在含碳产物中物质的量分数及CO2的转化率随温度的变化如图所示:
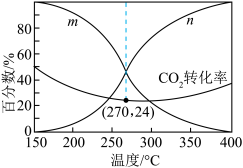
①图中m曲线代表的物质为________ 。
②下列说法正确的是________ (填标号)。
A.180~380℃范围内,H2的平衡转化率始终低于CO2
B.温度越高,越有利于工业生产CH3OH
C.一定时间内反应,加入选择性高的催化剂,可提高CH3OH的产率
D.150~400℃范围内,随着温度的升高,CO2的反应速率先减小后增大
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,270℃时反应①的分压平衡常数为
,270℃时反应①的分压平衡常数为________ (保留2位有效数字)。
(4)在一定条件下,密闭容器中加入一定量的CO、H2O(g)和催化剂仅发生反应 ,其速率方程为
,其速率方程为 ,
, ,其中
,其中 、
、 为正、逆反应速率,
为正、逆反应速率, 、
、 分别为速率常数,p为气体的分压。已知降低温度时,
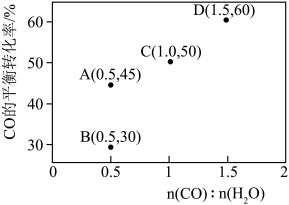
分别为速率常数,p为气体的分压。已知降低温度时, 增大,调整CO和H2O初始投料比,测得CO的平衡转化率如图,A、B、C、D四点中温度由高到低的顺序是
增大,调整CO和H2O初始投料比,测得CO的平衡转化率如图,A、B、C、D四点中温度由高到低的顺序是________ ,在C点所示投料比下,当CO转化率达到40%时,
________ 。
二氧化碳加氢制甲醇涉及的反应可表示为:
①
②
③
(1)根据上述反应求:④
(2)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上反应④的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。

写出该历程中决速步骤的化学方程式:
(3)一体积可变的密闭容器中,在保持a MPa下,按照

①图中m曲线代表的物质为
②下列说法正确的是
A.180~380℃范围内,H2的平衡转化率始终低于CO2
B.温度越高,越有利于工业生产CH3OH
C.一定时间内反应,加入选择性高的催化剂,可提高CH3OH的产率
D.150~400℃范围内,随着温度的升高,CO2的反应速率先减小后增大
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
(4)在一定条件下,密闭容器中加入一定量的CO、H2O(g)和催化剂仅发生反应

22-23高二下·湖北咸宁·期末
类题推荐
研发CO2利用技术、降低空气中CO2含量可采用“CO2催化加氢制甲醇”方法。
该反应体系中涉及以下两个反应:
Ⅰ.
Ⅱ.
回答下列问题:
(1)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
(2)反应Ⅰ、Ⅱ的InK(K代表化学平衡常数)随 (温度的倒数)的变化如图所示。
(温度的倒数)的变化如图所示。
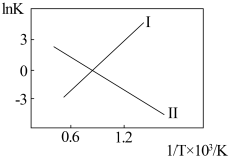
试判断升高温度,反应 的化学平衡常数
的化学平衡常数___________ (填“增大”或“减小”或“不变”)。
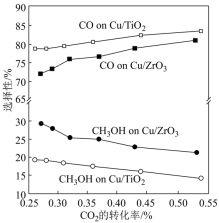
(3)恒压下将CO2和H2按体积比1∶3混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内CH3OH的选择性和产率随温度的变化如图。
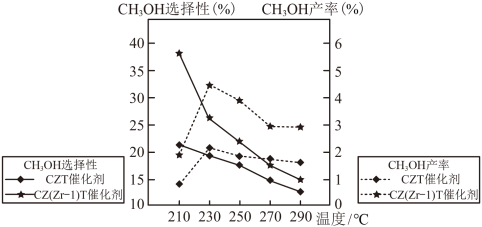
其中:CH3OH的选择性
①在上述条件下合成甲醇的工业条件是___________ 。
A.210℃ B.230℃ C.催化ZT D.催化剂CZ(Zr-1)T
②在230℃以上,升高温度CO2的转化率增大,但甲醇的产率降低,原因是___________ 。
(4)恒温恒压密闭容器中,加入2molCO2和4molH2,只发生反应Ⅰ和反应Ⅱ,初始压强为p0,在300℃发生反应,反应达平衡时,CO2的转化率为50%,容器体积减小20%。则反应Ⅱ的平衡常数K=___________ (保留两位有效数字)。
(5)已知对于反应Ⅰ, ,
, 。其中
。其中 分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。在540K下,按初始投料比
分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。在540K下,按初始投料比 分别为3∶1、1∶1、1∶3,得到不同压强条件下H2的平衡转化率关系如图所示。
分别为3∶1、1∶1、1∶3,得到不同压强条件下H2的平衡转化率关系如图所示。
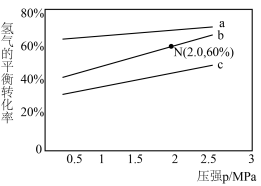
①比较a、b、c各曲线所表示的投料比大小顺序为___________ (用字母表示)。
②计算540K的压强平衡常数
___________ (用平衡分压代替平衡浓度计算)。
③540K条件下,某容器测得某时刻 ,
, ,
, ,此时
,此时
___________ 。
该反应体系中涉及以下两个反应:
Ⅰ.
Ⅱ.
回答下列问题:
(1)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
| A.增大CO的浓度,反应Ⅰ的平衡向正反应方向移动 |
| B.降低温度,反应Ⅰ和Ⅱ的正、逆反应速率都减小 |
| C.恒温恒容下充入氦气,反应Ⅰ的平衡向正反应方向移动 |
| D.增大压强,反应Ⅰ和Ⅱ重新达到平衡的时间不同 |

试判断升高温度,反应
(3)恒压下将CO2和H2按体积比1∶3混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内CH3OH的选择性和产率随温度的变化如图。

其中:CH3OH的选择性
①在上述条件下合成甲醇的工业条件是
A.210℃ B.230℃ C.催化ZT D.催化剂CZ(Zr-1)T
②在230℃以上,升高温度CO2的转化率增大,但甲醇的产率降低,原因是
(4)恒温恒压密闭容器中,加入2molCO2和4molH2,只发生反应Ⅰ和反应Ⅱ,初始压强为p0,在300℃发生反应,反应达平衡时,CO2的转化率为50%,容器体积减小20%。则反应Ⅱ的平衡常数K=
(5)已知对于反应Ⅰ,

①比较a、b、c各曲线所表示的投料比大小顺序为
②计算540K的压强平衡常数
③540K条件下,某容器测得某时刻
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网