解答题-原理综合题 适中0.65 引用1 组卷43
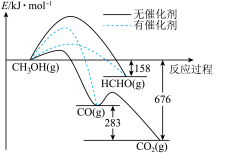
将煤液化得到的甲醇是重要的化工原料。下图所示为一定条件下1molCH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。
(1)在有催化剂作用下,CH3OH与O2反应主要生成___________ (填“CO”、“CO2”或HCHO”)。请补全热化学方程式HCHO(g)+1/2O2(g)=CO(g)+H2O(g)___________ 。
(2)请从有效碰撞理论的角度说明加入催化剂可以加快化学反应速率的原因:___________ 。
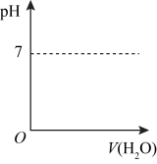
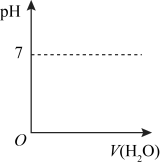
(3)HCHO可进一步被氧化为重要工业原料HCOOH(其酸性比H2SO3弱,比CH3COOH强)。在下图中画出常温下向甲酸钠溶液中加水时溶液的pH的变化___________ 。

(1)在有催化剂作用下,CH3OH与O2反应主要生成
(2)请从有效碰撞理论的角度说明加入催化剂可以加快化学反应速率的原因:
(3)HCHO可进一步被氧化为重要工业原料HCOOH(其酸性比H2SO3弱,比CH3COOH强)。在下图中画出常温下向甲酸钠溶液中加水时溶液的pH的变化

22-23高二下·上海嘉定·阶段练习
类题推荐
煤炭是我国最主要能源。煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)已知该产业链中,有炭参与的某反应平衡常数表达式为:K= ,写出它所对应反应的化学方程式:
,写出它所对应反应的化学方程式:___________ ,若该反应只有在持续高温下才能自发进行 则该反应为___________ (“吸热”或“放热”)反应。
(2) 将不同量的CO(g)和H2O(g)分别通入体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下2组数据:
CO2(g)+H2(g),得到如下2组数据:
①实验1中以v(CO2)表示的反应速率为___________ 。
②900 ℃时,反应CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数
CO2(g)+H2(g)的平衡常数___________ 。向实验2的平衡混合物中再加入0.4 mol H2O(g)和0.4 mol CO2,平衡___________ (选填“正反应方向”、“逆反应方向”或“不”)移动。
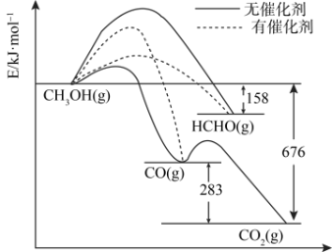
(3)将煤液化得到的甲醇是重要的化工原料。下图所示为一定条件下1 mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。
①在有催化剂作用下,CH3OH与O2反应主要生成___________ (填“CO”、“CO2”或HCHO”)。请补全热化学方程式HCHO(g)+1/2O2(g)→CO(g)+H2O(g)___________ 。
②HCHO可进一步被氧化为重要工业原料 HCOOH(其酸性比H2SO3弱,比CH3COOH强)。在下图中画出常温下向甲酸钠溶液中加水时溶液的pH的变化__________ 。
(1)已知该产业链中,有炭参与的某反应平衡常数表达式为:K=
(2) 将不同量的CO(g)和H2O(g)分别通入体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
| 2 | 900 | 0.5 | 1 | 0.2 | 0.8 | 3 |
②900 ℃时,反应CO(g)+H2O(g)
(3)将煤液化得到的甲醇是重要的化工原料。下图所示为一定条件下1 mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。

①在有催化剂作用下,CH3OH与O2反应主要生成
②HCHO可进一步被氧化为重要工业原料 HCOOH(其酸性比H2SO3弱,比CH3COOH强)。在下图中画出常温下向甲酸钠溶液中加水时溶液的pH的变化

CO2是主要的温室气体,以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向,回答下列问题:
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H1=-51kJ·mol-1
CH3OH(g)+H2O(g)△H1=-51kJ·mol-1
反应II:CO2(g)+H2(g) CO(g)+H2O(g)△H2=+41.17kJ·mol-1
CO(g)+H2O(g)△H2=+41.17kJ·mol-1
①已知:键能指断开1mol气态键所吸收的能量或形成1mol气态键所释放的能量。几种化学键的键能如表所示:
则a=______ kJ·mol-1。
②若反应II逆反应活化能Ea(逆)为124kJ·mol-1,则该反应的Ea(正)活化能为______ kJ·mol-1。
(2)向恒容容器中充入1molCO2和2molH2,此时容器内总压强为P0。若只发生反应I,测得反应在不同压强、不同温度下,CO2的平衡转化率如图1所示,测得反应时逆反应速率与容器中c(CH3OH)关系如图II所示:
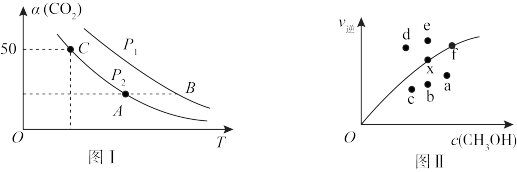
①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序排列为_____ ,图I中C点CO2的转化率为____ 。
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是____ 。
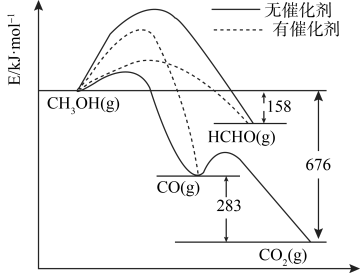
(3)反应I得到的甲醇是重要的化工原料。如图所示为一定条件下1molCH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。
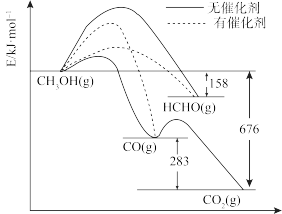
①在有催化剂作用下,CH3OH与O2反应主要生成____ (填“CO”、“CO2”或HCHO”)。
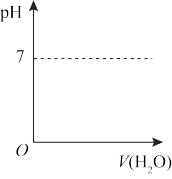
②HCHO可进一步被氧化为重要工业原料HCOOH(其酸性比H2SO3弱,比CH3COOH强)。在图中画出常温下向甲酸钠溶液中加水时溶液的pH的变化____ 。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:CO2(g)+3H2(g)
反应II:CO2(g)+H2(g)
①已知:键能指断开1mol气态键所吸收的能量或形成1mol气态键所释放的能量。几种化学键的键能如表所示:
| 化学键 | C—H | C—O | H—O(H2O中) | H—O(CH3OH中) | H—H | C=O |
| 键能/kJ·mol-1 | 406 | 351 | 462.5 | 465 | 436 | a |
②若反应II逆反应活化能Ea(逆)为124kJ·mol-1,则该反应的Ea(正)活化能为
(2)向恒容容器中充入1molCO2和2molH2,此时容器内总压强为P0。若只发生反应I,测得反应在不同压强、不同温度下,CO2的平衡转化率如图1所示,测得反应时逆反应速率与容器中c(CH3OH)关系如图II所示:

①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序排列为
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是
(3)反应I得到的甲醇是重要的化工原料。如图所示为一定条件下1molCH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。

①在有催化剂作用下,CH3OH与O2反应主要生成
②HCHO可进一步被氧化为重要工业原料HCOOH(其酸性比H2SO3弱,比CH3COOH强)。在图中画出常温下向甲酸钠溶液中加水时溶液的pH的变化

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网