解答题-结构与性质 较难0.4 引用1 组卷62
铜和钛可呈现多种化合价,回答下列问题。
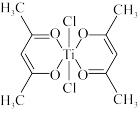
(1)配位化合物中心原子也存在轨道杂化现象, 中
中 采取sp杂化,
采取sp杂化, 的空间结构为
的空间结构为___________ 。
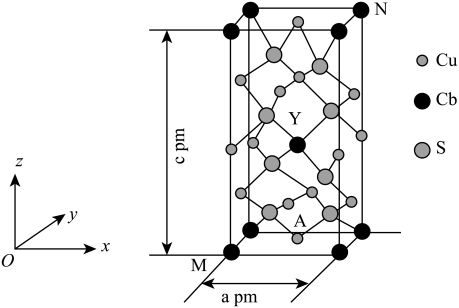
(2)某种含铜热电材料,晶胞结构如图,Cu位于棱、面上,Sb位于体心、顶点,S位于晶胞内,底部边长为 ,高为
,高为 ,该晶体化学式为
,该晶体化学式为___________ ,其中部分原子坐标为 、
、 、
、 ,Y点的原子坐标为
,Y点的原子坐标为___________ 。
(3)基态Ti原子的价电子轨道表示式为___________ 。
(4)钛基配合物可用于催化环烯烃聚合,其结构如图所示:
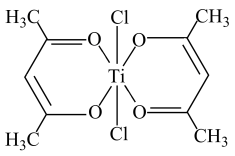
钛的配位数为___________ 。
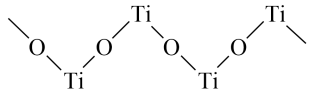
(5)已知 与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为
与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为___________ 。
(1)配位化合物中心原子也存在轨道杂化现象,
(2)某种含铜热电材料,晶胞结构如图,Cu位于棱、面上,Sb位于体心、顶点,S位于晶胞内,底部边长为

(3)基态Ti原子的价电子轨道表示式为
(4)钛基配合物可用于催化环烯烃聚合,其结构如图所示:

钛的配位数为
(5)已知

22-23高二下·山东济宁·期中
类题推荐
钛被誉为“21世纪的金属”,可呈现多种化合价,其中以Ti4+最为稳定,回答下列问题:
(1)已知电离能:I2(Ti) =1310 kJ·mol-1,I2(K)=3051 kJ·mol-1,I2(Ti)<I2(K),其原因为_______ 。
(2)某种钛的化合物可用于催化环烯烃聚合,其结构如图所示:
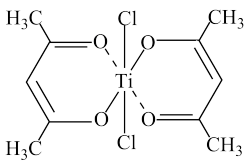
①碳原子的杂化轨道类型有_______ 。
②该化合物中存在的化学键有_______ (填字母)。
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(3)钛与卤素形成化合物的熔、沸点如下表所示:
分析TiCl4、TiBr4、TiI4熔沸点呈现一定变化规律的原因是_______ 。
(4)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为_______ ,阴离子的空间结构为_______ 。

(1)已知电离能:I2(Ti) =1310 kJ·mol-1,I2(K)=3051 kJ·mol-1,I2(Ti)<I2(K),其原因为
(2)某种钛的化合物可用于催化环烯烃聚合,其结构如图所示:

①碳原子的杂化轨道类型有
②该化合物中存在的化学键有
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(3)钛与卤素形成化合物的熔、沸点如下表所示:
| 化合物 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | -24.1 | 38.3 | 155 |
| 沸点/℃ | 136.5 | 233.5 | 377 |
(4)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为

钛被誉为“21世纪的金属”,可呈现多种化合价,其中以+4价的Ti最为稳定。回答下列问题:
(1)基态Ti原子的价电子轨道表示式为___ 。
(2)已知电离能:I2(Ti)=1 310 kJ/mol,I2(K)=3051 kJ/mol,I2(Ti)<I2(K),其原因为_____________
(3)钛某配合物可用于催化环烯烃聚合,其结构如下图所示:

①钛的配位数为___ ,碳原子的杂化类型____ 。
②该配合物中存在的化学键有____ (填字母代号)。
A.离子键 B.配位键 C.金属键 D.共价键 e.氢键
(4)钛与卤素形成的化合物熔沸点如下表所示:
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是_________________
(5)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为____ ,阴离子的空间构型为__________ .


(6)已知TiN晶体的晶胞结构如图所示,若该晶胞的密度为ρg/cm3,阿伏加 德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为____ pm(用含p、NA的代数式表示)。
(1)基态Ti原子的价电子轨道表示式为
(2)已知电离能:I2(Ti)=1 310 kJ/mol,I2(K)=3051 kJ/mol,I2(Ti)<I2(K),其原因为
(3)钛某配合物可用于催化环烯烃聚合,其结构如下图所示:

①钛的配位数为
②该配合物中存在的化学键有
A.离子键 B.配位键 C.金属键 D.共价键 e.氢键
(4)钛与卤素形成的化合物熔沸点如下表所示:
| TiCl4 | TiBr4 | TiI4 | |
| 熔点/℃ | -24.1 | 38.3 | 155 |
| 沸点/℃ | 136.5 | 233.5 | 377 |
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是
(5)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为


(6)已知TiN晶体的晶胞结构如图所示,若该晶胞的密度为ρg/cm3,阿伏加 德罗常数值为NA,则晶胞中Ti原子与N原子的最近距离为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网