解答题-实验探究题 适中0.65 引用3 组卷142
环己烯(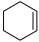 )是重要的化工原料,实验室环己醇(
)是重要的化工原料,实验室环己醇(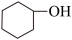 )可在
)可在催化下制备环己烯。
如图所示,将环己醇加入试管A中,再加入
密度( | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
(2)实验时水浴温度应高于
(3)环己烯粗品中含少量环己醇和HCl等物质。加入饱和食盐水除去HCl,经振荡、静置、分层后,产品在
Ⅱ.环己烯含量测定
向a g环己烯样品中加入b mol
(4)样品中环己烯的质量分数为
22-23高二下·山东济宁·期中
类题推荐
环己烯是重要的化工原料,实验室常用下列反应制备环己烯:

环己醇、环己烯的部分物理性质如表:
*括号中的数据表示该有机物与水形成的具有固定组成的混合物中有机物的质量分数
Ⅰ.环己烯的制备与提纯
制备环己烯粗品。实验中将环己醇与浓硫酸混合加入烧瓶中,按图示装置,油浴加热,蒸馏约1 h,收集馏分,得到主要含环己烯和水的混合物
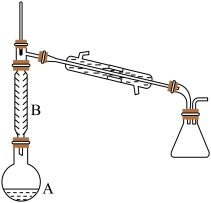
(1)原料环己醇中若含苯酚杂质,检验试剂为__ ,现象为__ 。上述装置中仪器B的作用为__ 。
环己烯的提纯操作步骤主要有:向馏出液中加入精盐至饱和;加入3~4 mL 5% Na2CO3溶液;静置,分液;加入无水CaCl2固体;蒸馏。
(2)蒸馏不能彻底分离环己烯和水的原因是____ 。
(3)加入3~4 mL 5% Na2CO3溶液的作用是____ 。
Ⅱ.环己烯含量的测定
在一定条件下,向a g环己烯样品中加入定量制得的bmol Br2,与环己烯充分反应后,剩余的Br2与足量KI作用生成I2,用cmol·L-1的Na2S2O3标准溶液滴定,终点时消耗Na2S2O3标准溶液V mL(以上数据均已扣除干扰因素)。测定过程中,发生的反应如下:
①Br2+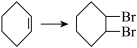 ②Br2+2KI=I2+2KBr③I2+2Na2S2O3=2NaI+Na2S4O6
②Br2+2KI=I2+2KBr③I2+2Na2S2O3=2NaI+Na2S4O6
(4)滴定所用指示剂为___ 。样品中环己烯的质量分数为___ (用含字母的代数式表示)。
(5)下列情况会导致测定结果偏低的是____ (填字母)。
a.样品中含有苯酚杂质 b.在测定过程中部分环己烯挥发c. Na2S2O3标准溶液部分被氧化

环己醇、环己烯的部分物理性质如表:
物质 | 沸点(℃) | 密度(g·cm-3,20 ℃) | 溶解性 |
环己醇 | 161.1(97.8)* | 0.9624 | 能溶于水 |
环己烯 | 83(70.8)* | 0.8085 | 不溶于水 |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物中有机物的质量分数
Ⅰ.环己烯的制备与提纯
制备环己烯粗品。实验中将环己醇与浓硫酸混合加入烧瓶中,按图示装置,油浴加热,蒸馏约1 h,收集馏分,得到主要含环己烯和水的混合物

(1)原料环己醇中若含苯酚杂质,检验试剂为
环己烯的提纯操作步骤主要有:向馏出液中加入精盐至饱和;加入3~4 mL 5% Na2CO3溶液;静置,分液;加入无水CaCl2固体;蒸馏。
(2)蒸馏不能彻底分离环己烯和水的原因是
(3)加入3~4 mL 5% Na2CO3溶液的作用是
Ⅱ.环己烯含量的测定
在一定条件下,向a g环己烯样品中加入定量制得的bmol Br2,与环己烯充分反应后,剩余的Br2与足量KI作用生成I2,用cmol·L-1的Na2S2O3标准溶液滴定,终点时消耗Na2S2O3标准溶液V mL(以上数据均已扣除干扰因素)。测定过程中,发生的反应如下:
①Br2+
 ②Br2+2KI=I2+2KBr③I2+2Na2S2O3=2NaI+Na2S4O6
②Br2+2KI=I2+2KBr③I2+2Na2S2O3=2NaI+Na2S4O6(4)滴定所用指示剂为
(5)下列情况会导致测定结果偏低的是
a.样品中含有苯酚杂质 b.在测定过程中部分环己烯挥发c. Na2S2O3标准溶液部分被氧化
环己烯是重要的化工原料。其实验室制备流程如下:
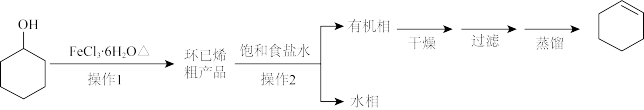
可能用到的有关数据如下:
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)FeCl3∙6H2O晶体可由FeCl3溶液制得,其操作步骤为减压蒸发浓缩,__________ ,过滤,洗涤,干燥。若FeCl3溶液中含FeCl2杂质,检验的方法为_______________ 。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
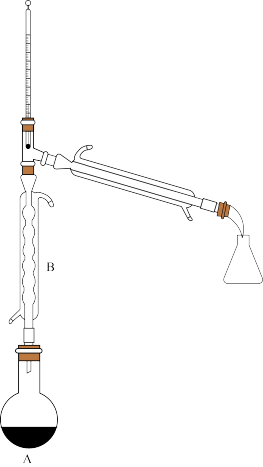
①浓硫酸也可作该反应的催化剂,选择FeCl3·6H2O而不用浓硫酸的优点为________ (任答一点即可)。
②仪器B的作用为____________________________________ 。
(3)蒸馏操作的正确顺序为______________ (填序号)。
①加热 ②安装装置,加入待蒸馏的物质和沸石
③弃去前馏分,收集83℃的馏分 ④通冷凝水
Ⅱ.环己烯含量的测定
在一定条件下,向mg环己烯样品中加入含amolBr2的溴水,充分反应后,向所得溶液中加入足量KI和几滴淀粉溶液,再用b mol∙L-1的Na2S2O3标准溶液滴定该溶液,达到滴定终点时消耗Na2S2O3标准溶液VmL(以上数据均已扣除干扰因素)。已知:I2+2Na2S2O3=2NaI+Na2S4O6
(4)滴定终点的现象是________________________________________________ 。样品中环己烯的质量分数为_____________ (用字母表示)。
(5)若滴定终点时仰视读数会导致最终测定的环己烯含量_______ (填“偏高”、“偏低”或“无影响”)。

可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)FeCl3∙6H2O晶体可由FeCl3溶液制得,其操作步骤为减压蒸发浓缩,
(2)操作1的装置如图所示(加热和夹持装置已略去)。

①浓硫酸也可作该反应的催化剂,选择FeCl3·6H2O而不用浓硫酸的优点为
②仪器B的作用为
(3)蒸馏操作的正确顺序为
①加热 ②安装装置,加入待蒸馏的物质和沸石
③弃去前馏分,收集83℃的馏分 ④通冷凝水
Ⅱ.环己烯含量的测定
在一定条件下,向mg环己烯样品中加入含amolBr2的溴水,充分反应后,向所得溶液中加入足量KI和几滴淀粉溶液,再用b mol∙L-1的Na2S2O3标准溶液滴定该溶液,达到滴定终点时消耗Na2S2O3标准溶液VmL(以上数据均已扣除干扰因素)。已知:I2+2Na2S2O3=2NaI+Na2S4O6
(4)滴定终点的现象是
(5)若滴定终点时仰视读数会导致最终测定的环己烯含量
环己烯是重要的化工原料。其实验室制备流程如下:


 +H2O
+H2O
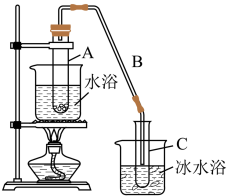
(1)制备粗品:采用如图所示装置,用环己醇制备环己烯。

将10.0环己醇加入试管A中,再加入1mL浓硫酸,摇匀放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①原料环己醇中若含苯酚杂质,检验试剂为________ ,现象为________ 。
②A中碎瓷片的作用是________ 。
③试管C置于冰水浴中的目的是_____ 。
(2)制备精品:
①环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、青置、分层,环己烯在_____ 层(填“上”或“下”),分液后用_______ 洗涤(填字母)。
A. 溶液 B.稀
溶液 B.稀 C.
C. 溶液
溶液
②再将环己烯进行蒸馏,收集产品时,应收集________ ℃的馏分,若最终收集到环己烯5.74g,则产率为________ 。

 +H2O
+H2O| 密度( | 熔点(℃) | 沸点(℃) | 溶解性 | 摩尔质量( | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 | 100 |
环己烯 | 0.81 | 83 | 难溶于水 | 82 |

将10.0环己醇加入试管A中,再加入1mL浓硫酸,摇匀放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①原料环己醇中若含苯酚杂质,检验试剂为
②A中碎瓷片的作用是
③试管C置于冰水浴中的目的是
(2)制备精品:
①环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、青置、分层,环己烯在
A.
②再将环己烯进行蒸馏,收集产品时,应收集
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


