解答题-无机推断题 适中0.65 引用1 组卷161
元素周期表是化学发展史上的重要里程碑之一。“价-类”二维图有助于认识物质之间的转化,更有利于提升对元素周期表的认识。
(1)元素周期表共有_______ 个周期。其中氮元素在周期表中的位置是_______ 。
(2)在放电或高温下,空气中的N2会转化为HNO3,过程如下图。
N2 NO
NO NO2
NO2 HNO3
HNO3
其中属于固氮的转化是_______ 。(选填上图中编号)写出③的化学方程式_______ 。
(3)检验硝酸铵固体中铵根离子的方法为_______ 。
(4)对“N”“P”元素及其化合物相关性质进行比较,下列说法不正确的是_______。
下图是某元素的“价-类”二维图:
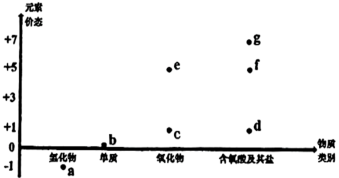
(5)已知该元素是第3周期元素,此元素是_______ (填写元素符号),画出该元素的原子结构示意图_______ 。
(6)有同学猜测向含d的含氧酸根离子的溶液中加入含a的浓溶液,能产生_______(选填编号)。
(7)从元素化合价角度分析能发生上述反应的原因_______ 。
(1)元素周期表共有
(2)在放电或高温下,空气中的N2会转化为HNO3,过程如下图。
N2
其中属于固氮的转化是
(3)检验硝酸铵固体中铵根离子的方法为
(4)对“N”“P”元素及其化合物相关性质进行比较,下列说法不正确的是_______。
| A.原子半径大小:P<N |
| B.原子得电子的能力:P<N |
| C.气态氢化物的热稳定性:PH3<NH3 |
| D.最高价氧化物对应水化物的酸性:H3PO4<HNO3 |
下图是某元素的“价-类”二维图:

(5)已知该元素是第3周期元素,此元素是
(6)有同学猜测向含d的含氧酸根离子的溶液中加入含a的浓溶液,能产生_______(选填编号)。
| A.b | B.e | C.f | D.g |
22-23高二下·上海闵行·期中
类题推荐
Ⅰ.元素周期表是化学发展史上的重要里程碑之一。“价-类” 二维图有助于认识物质之间的转化,更有利于提升对元素周期表的认识。
(1)元素周期表共有________ 个周期。其中氮元素在周期表中的位置是第________ 周期,第________ 主族。
(2)在放电或高温下,空气中的N2会转化为HNO3,过程如图:________ (选填图中编号);写出③的化学方程式____________ 。
(3)检验硝酸铵溶液中铵根离子的方法为________________ 。
(4)对“N”“P”元素及其化合物相关性质进行比较,下列说法不正确 的是________。
Ⅱ.下图是某元素的“价-类”二维图:________ (填写元素符号)。
Ⅲ.从元素周期表中我们可以知道元素原子的基本结构,而元素周期律的发现是化学系统化过程中的一个重要里程碑,根据元素周期律,我们可以根据元素在周期表中的位置预测其性质。
(6)元素性质呈现周期性变化的根本原因是________。
(7)放射性同位素 的中子数为________。
的中子数为________。
(8)下列元素中,原子半径最大的是________。
(9)下列元素的最高价氧化物对应的水化物中碱性最强的是________。
(1)元素周期表共有
(2)在放电或高温下,空气中的N2会转化为HNO3,过程如图:
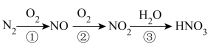
(3)检验硝酸铵溶液中铵根离子的方法为
(4)对“N”“P”元素及其化合物相关性质进行比较,下列说法
| A.原子半径大小: P<N | B.原子得电子的能力: P<N |
| C.气态氢化物的热稳定性: PH3<NH3 | D.最高价氧化物对应水化物的酸性: H3PO4<HNO3 |
Ⅱ.下图是某元素的“价-类”二维图:
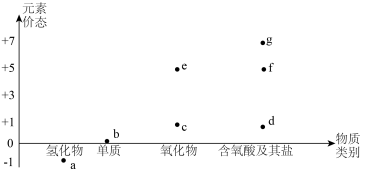
Ⅲ.从元素周期表中我们可以知道元素原子的基本结构,而元素周期律的发现是化学系统化过程中的一个重要里程碑,根据元素周期律,我们可以根据元素在周期表中的位置预测其性质。
(6)元素性质呈现周期性变化的根本原因是________。
| A.核外电子排布呈周期性变化 | B.元素的相对原子质量逐渐增大 |
| C.核电荷数逐渐增大 | D.元素化合价呈周期性变化 |
(7)放射性同位素
| A.184 | B.131 | C.78 | D.53 |
(8)下列元素中,原子半径最大的是________。
| A.Mg | B.Al | C.Si | D.P |
(9)下列元素的最高价氧化物对应的水化物中碱性最强的是________。
| A.Al | B.Li | C.Na | D.Mg |
“价—类”二维图是以物质的类别为横坐标,以某种元素的化合价为纵坐标,在二维平面内绘制的含有该元素物质的图像,该图是高中化学学习元素化合物知识的重要工具。氮及其部分化合物的“价—类”二维图如图所示:

(1)以上①~⑤的转化过程,其中属于氮的固定的是_______ (填写编号)
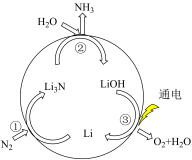
(2)固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理如图所示。下列叙述正确的是_______。
(3)NO、 对环境有污染,可用NaOH溶液吸收。用不同浓度的NaOH溶液吸收
对环境有污染,可用NaOH溶液吸收。用不同浓度的NaOH溶液吸收 含量不同的尾气,关系如图:
含量不同的尾气,关系如图:
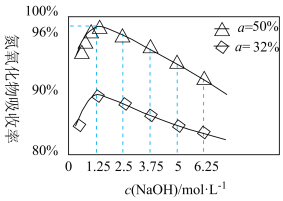
(α表示尾气里NO、 中
中 的含量)
的含量)
①用NaOH溶液吸收氮氧化物的最佳条件为:
_______ ,
_______ 。
②从图上可知, 含量越大,氮氧化物的吸收率越大。当
含量越大,氮氧化物的吸收率越大。当 时,加入
时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是_______
(4)从物质类别角度分析,硝酸属于酸,具有酸的通性;从氮元素化合价的角度分析,硝酸具有氧化性。与下列物质反应既能体现硝酸酸性又能体现硝酸氧化性的是_______ 。
A. B.Cu C.C
B.Cu C.C
(5)对于 和
和 的混合溶液,若
的混合溶液,若 和
和 物质的量浓度存在如下关系:
物质的量浓度存在如下关系: ,理论上最多能溶解铜的物质的量为
,理论上最多能溶解铜的物质的量为_______ 。

(1)以上①~⑤的转化过程,其中属于氮的固定的是
(2)固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理如图所示。下列叙述正确的是_______。

| A.转化过程中所涉及的元素均呈现了两种价态 |
| B.反应①②③均为氧化还原反应 |
| C.Li是催化剂,只有 |
| D.整个过程的总反应可表示为 |

(α表示尾气里NO、
①用NaOH溶液吸收氮氧化物的最佳条件为:
②从图上可知,
(4)从物质类别角度分析,硝酸属于酸,具有酸的通性;从氮元素化合价的角度分析,硝酸具有氧化性。与下列物质反应既能体现硝酸酸性又能体现硝酸氧化性的是
A.
(5)对于
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



