解答题-原理综合题 较易0.85 引用1 组卷204
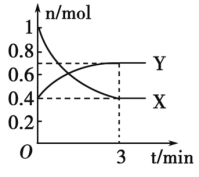
Ⅰ、在某温度时,在0.5L的恒容容器中发生气体M、N两种物质的相互转化,M、N的物质的量随时间变化的曲线如图所示,请根据图中数据分析,完成下列问题:
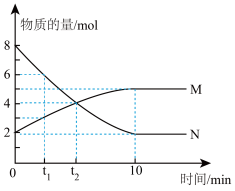
(1)该反应的化学方程式___________ 。
(2)反应开始的一瞬间进行的反应___________ (填“只有正反应发生”或者“只有逆反应发生”、“正、逆反应同时发生”),在t2时刻M的正反应速率___________ M的逆反应速率(填“大于”或者“小于”、“等于”),反应进行到10min时,N的平均反应速率为___________ 。
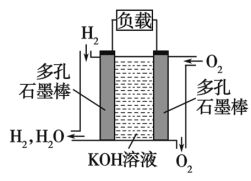
Ⅱ、被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,回答下列问题:
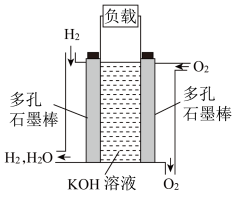
(3)O2进入的电极为___________ (填“正极”或“负极”)。
(4)电池工作时,溶液中的OH−向___________ (填“正极”或“负极”)迁移。
(5)若电池工作时转移0.04mol电子,理论上消耗标准状态下___________ mL O2。

(1)该反应的化学方程式
(2)反应开始的一瞬间进行的反应
Ⅱ、被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,回答下列问题:

(3)O2进入的电极为
(4)电池工作时,溶液中的OH−向
(5)若电池工作时转移0.04mol电子,理论上消耗标准状态下
22-23高一下·福建南平·期中
类题推荐
工业上常用CO和 合成甲醇,反应的化学方程式为
合成甲醇,反应的化学方程式为 ,该反应为放热反应。向容积为2L的刚性容器中通入一定量的CO、
,该反应为放热反应。向容积为2L的刚性容器中通入一定量的CO、 和
和 ,在一定温度下发生上述反应,其中两种物质的物质的量随时间变化如下图所示。
,在一定温度下发生上述反应,其中两种物质的物质的量随时间变化如下图所示。
(1)图中A物质为______ ,反应开始至4min,CO的平均反应速率为______ 。
(2)4min时,反应是否达到平衡状态?______ (填“是”或“否”);8min时该反应的正反应速率______ 逆反应速率(填“ ”“
”“ ”或“
”或“ ”,下同);该反应的反应物总能量
”,下同);该反应的反应物总能量______ 生成物总能量。
(3)对于上述条件下的该反应,下列情况不能说明反应达到平衡状态的是______(填字母)。
(4)对于反应 ,下述方法能加快反应速率的是______(填字母)。
,下述方法能加快反应速率的是______(填字母)。
(5)一种甲醇燃料电池的结构示意图如下:______ (填“正极”或“负极”),该电极的电极反应式为______ 。
②若电路中转移1mol ,理论上正极消耗标准状况下氧气的体积为
,理论上正极消耗标准状况下氧气的体积为______ L。
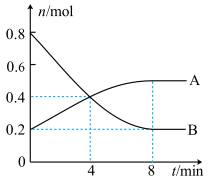
(1)图中A物质为
(2)4min时,反应是否达到平衡状态?
(3)对于上述条件下的该反应,下列情况不能说明反应达到平衡状态的是______(填字母)。
| A.气体的总物质的量不变 |
| B.气体的密度不变 |
| C.容器内CO的浓度不变 |
| D.相同时间内,断裂 |
(4)对于反应
| A.一定温度下,保持容器体积不变,及时移走产物 |
| B.一定温度下,保持容器压强不变,通入稀有气体 |
| C.一定温度下,保持容器体积不变,通入一定量的CO气体 |
| D.保持容器体积不变,升高温度 |
(5)一种甲醇燃料电池的结构示意图如下:
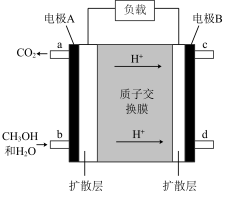
②若电路中转移1mol
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网