解答题-实验探究题 适中0.65 引用1 组卷62
某研究小组在实验室以含铁的铜屑为原料制备Cu(NO3)2•3H2O晶体,并用滴定法测定Cu(NO3)2•3H2O晶体的纯度。
Ⅰ.设计的合成路线如图:
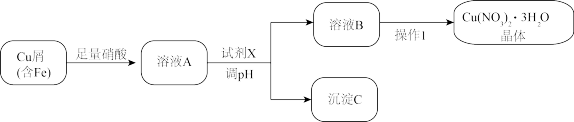
(1)试剂X是______ (填化学式),沉淀C为______ (填化学式)。
(2)操作Ⅰ的过程为______ 、过滤、洗涤等步骤。
Ⅱ.学习小组用“间接碘量法”测定Cu(NO3)2•3H2O (摩尔质量:242g•mol-1)晶体的纯度,过程如下:取0.4400g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000mol•L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL。
已知:I2+2S2O =S4O
=S4O +2I-
+2I-
(3)可选用______ 作滴定指示剂,滴定终点的现象是______ 。
(4)Cu(NO3)2溶液与KI反应的离子方程式为______ 。
(5)该试样中Cu(NO3)2•3H2O的质量百分数为_______ 。
(6)计算表明Cu(NO3)2•3H2O的质量百分数大于100%,可能原因是______ 。
Ⅰ.设计的合成路线如图:

(1)试剂X是
(2)操作Ⅰ的过程为
Ⅱ.学习小组用“间接碘量法”测定Cu(NO3)2•3H2O (摩尔质量:242g•mol-1)晶体的纯度,过程如下:取0.4400g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000mol•L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL。
已知:I2+2S2O
(3)可选用
(4)Cu(NO3)2溶液与KI反应的离子方程式为
(5)该试样中Cu(NO3)2•3H2O的质量百分数为
(6)计算表明Cu(NO3)2•3H2O的质量百分数大于100%,可能原因是
22-23高一下·浙江·阶段练习
类题推荐
常温下,几种物质的溶度积常数见下表:
(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净的CuCl2溶液,宜加入_______ 调至溶液pH=4,使Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_______ 。
(2)过滤后,将所得滤液经过_______ 、_______ 操作,可得到CuCl2·2H2O晶体。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.800 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液40.00 mL(已知:I2+2S2O =S4O
=S4O +2I-)。
+2I-)。
①可选用_______ 作指示剂,滴定终点的现象是_______ 。
②CuCl2溶液与KI反应的离子方程式为_______ 。
③该试样中CuCl2·2H2O的质量百分数为_______ 。
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净的CuCl2溶液,宜加入
(2)过滤后,将所得滤液经过
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.800 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液40.00 mL(已知:I2+2S2O
①可选用
②CuCl2溶液与KI反应的离子方程式为
③该试样中CuCl2·2H2O的质量百分数为
Ⅰ.某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性质杂质)的纯度,过程如下:取0.800g 试样溶于水,加入过量KI 固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3 标准溶液滴定,到达滴定终点时,平均消耗Na2S2O3 标准溶液40.00 mL。(已知:2Cu2++4I-=2CuI↓+I2;I2+2S2O32-=S4O62-+2I-。)
(1)可选用________ 作滴定指示剂,滴定终点的现象是________________ 。
(2)该试样中CuCl2·2H2O 的质量百分数为________________ 。
Ⅱ.25℃,两种酸的电离平衡常数如表,按要求回答下列问题。
(1)用离子方程式表示亚硫酸钠溶液呈碱性的原因________________________________ 。
(2)浓度均为0.1mol/L的Na2SO3和Na2CO3的溶液中SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为________________________________ 。
(3)亚硫酸钠溶液中通入少量CO2气体的化学方程式________________________________ 。
(1)可选用
(2)该试样中CuCl2·2H2O 的质量百分数为
Ⅱ.25℃,两种酸的电离平衡常数如表,按要求回答下列问题。
| K1 | K2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
(2)浓度均为0.1mol/L的Na2SO3和Na2CO3的溶液中SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为
(3)亚硫酸钠溶液中通入少量CO2气体的化学方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


