解答题-实验探究题 适中0.65 引用2 组卷177
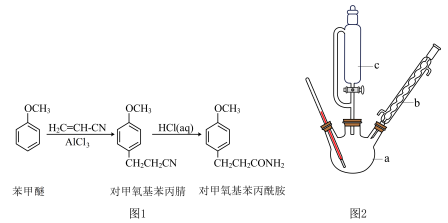
对甲氧基苯丙酰胺(相对分子质量为179)为难溶于冷水的白色晶体,且是一种医药中间体,可以由苯甲醚通过两步反应合成,合成路线如图1所示。
②丙烯腈蒸汽与空气可形成爆炸性混合物。
步骤一:用图2所示装置合成对甲氧基苯丙腈
在a中加入108g苯甲醚,室温下缓慢加入70g粉末状三氯化铝,加入过程中温度不超过25℃,加完后降温至5℃,然后逐滴加入130g丙烯腈(沸点77℃),滴加结束后再升温至90~95℃,反应2h。将反应液倒入500g冰水中,搅匀,静置分层,分出油相。减压蒸馏,收集2.67kPa下150~160℃的馏分,得到对甲氧基苯丙腈。
步骤二:合成对甲氧基苯丙酰胺
将步骤一中合成的对甲氧基苯丙腈加到a中,再加入300mL浓盐酸,经过一系列操作后得到对甲氧基苯丙酰胺134.25g。
(1)a的名称是______ ,对甲氧基苯丙腈的合成过程中宜采用的加热方式为______ 。
(2)图2中合成对甲氧基苯丙腈的装置有一缺陷,请提出改进方法并说明理由:______ 。
(3)用c加丙烯腈的优点有______ 。(写出两条)
(4)合成对甲氧基苯丙酰胺的过程中加浓盐酸后的一系列操作为:升温至40~50℃。搅拌1h→加入活性炭回流0.5h→______ →将滤液慢慢倒入1000g冷水中,析出晶体→抽滤→洗涤、烘干。
(5)下列关于实验操作的说法正确的是______ 。
(6)本实验中对甲氧基苯丙酰胺的产率为_______ 。
②丙烯腈蒸汽与空气可形成爆炸性混合物。
步骤一:用图2所示装置合成对甲氧基苯丙腈
在a中加入108g苯甲醚,室温下缓慢加入70g粉末状三氯化铝,加入过程中温度不超过25℃,加完后降温至5℃,然后逐滴加入130g丙烯腈(沸点77℃),滴加结束后再升温至90~95℃,反应2h。将反应液倒入500g冰水中,搅匀,静置分层,分出油相。减压蒸馏,收集2.67kPa下150~160℃的馏分,得到对甲氧基苯丙腈。
步骤二:合成对甲氧基苯丙酰胺
将步骤一中合成的对甲氧基苯丙腈加到a中,再加入300mL浓盐酸,经过一系列操作后得到对甲氧基苯丙酰胺134.25g。
(1)a的名称是
(2)图2中合成对甲氧基苯丙腈的装置有一缺陷,请提出改进方法并说明理由:
(3)用c加丙烯腈的优点有
(4)合成对甲氧基苯丙酰胺的过程中加浓盐酸后的一系列操作为:升温至40~50℃。搅拌1h→加入活性炭回流0.5h→
(5)下列关于实验操作的说法正确的是
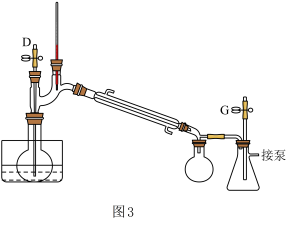
| A.减压蒸馏采用如图3所示装置,装置中的D为毛细管,也可以用沸石代替 |
| B.减压蒸馏过程中,可以通过控制G处的旋塞停止减压 |
| C.在对甲氧基苯丙酰胺的合成过程中,析出的晶体可以用冷水洗涤 |
| D.减压过滤不宜用于过滤颗粒太小的沉淀,因为颗粒太小的沉淀在快速过滤时易透过滤纸 |
(6)本实验中对甲氧基苯丙酰胺的产率为
22-23高二下·山东滨州·阶段练习
类题推荐
苯乙腈是一种重要的精细化工产品,主要用于农药、医药、染料和香料中间体的生产。相关科研机构对苯乙腈的生成方法提出改进,使其生产效率进一步提高,同时降低了反应中有毒物质的逸出。相关物质性质:
反应原理: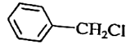 (氯化苄)+NaCN
(氯化苄)+NaCN
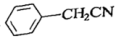 (苯以腈)+NaCl
(苯以腈)+NaCl
主要装置: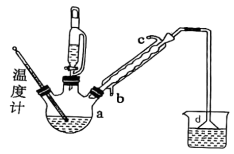
实验步骤:①向仪器a中加入氯化苄25.3g,缓慢加入适量二甲胺水溶液,放入磁子搅拌。
②安装好球形冷凝管、恒压漏斗及温度计,开启冷凝水,并对仪器a进行加热至90℃。
③向恒压漏斗中加入30%氰化钠水溶液49.0g。
④控制滴加速度与反应温度,使反应在90±5℃下进行。
⑤滴加结束后,加热回流20小时。
⑥反应结束并冷却至室温后,向混合物中加100mL水,洗涤,分液。
⑦往得到的粗产品中加入无水 颗粒,静置片刻,倒入蒸馏烧瓶中,弃去
颗粒,静置片刻,倒入蒸馏烧瓶中,弃去 ,进行减压(2700Pa)蒸馏,收集115~125℃馏分,得到产品无色透明液体22.3g。
,进行减压(2700Pa)蒸馏,收集115~125℃馏分,得到产品无色透明液体22.3g。
回答下列问题:
(1)图中仪器a的名称是______ ,仪器d的作用是______ 。
(2)进行分液操作时产品在混合物______ (填“上层”或“下层”)。
(3)无水 颗粒的作用是
颗粒的作用是______ 。
(4)在蒸馏过程中,减压蒸馏得到的产品纯度和产率均比常压下蒸馏收集233℃馏分高,原因是______ 。
(5)若反应中缺少二甲胺,相同条件下几乎没有产品得到,说明二甲胺在反应中起到______ 的作用。反应温度控制在90±5℃的原因可能是______ 。
(6)本实验所得到的苯乙腈产率是______ (保留三位有效数字)。
物质名称 | 相对分子 质量 | 颜色、状态 | 溶解性 | 沸点/℃ | 毒性 |
苯乙腈 | 117 | 无色油状液体,密度比水大 | 难溶于水,溶于醇 | 233.5 | 有毒,受热易分解产生有毒气体 |
氯化苄 | 126.5 | 无色或微黄色的透明液体 | 微溶于水,混溶于乙醇 | 179.4 | 有毒 |
氰化钠 | 49 | 白色结晶颗粒或粉末 | 易溶于水 | 1496 | 剧毒 |
二甲胺 | 45 | 无色气体,高浓度时有类似氨的气味 | 易溶于水,溶于乙醇 | 6.9 | 有毒 |
 (氯化苄)+NaCN
(氯化苄)+NaCN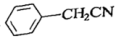 (苯以腈)+NaCl
(苯以腈)+NaCl主要装置:

实验步骤:①向仪器a中加入氯化苄25.3g,缓慢加入适量二甲胺水溶液,放入磁子搅拌。
②安装好球形冷凝管、恒压漏斗及温度计,开启冷凝水,并对仪器a进行加热至90℃。
③向恒压漏斗中加入30%氰化钠水溶液49.0g。
④控制滴加速度与反应温度,使反应在90±5℃下进行。
⑤滴加结束后,加热回流20小时。
⑥反应结束并冷却至室温后,向混合物中加100mL水,洗涤,分液。
⑦往得到的粗产品中加入无水
回答下列问题:
(1)图中仪器a的名称是
(2)进行分液操作时产品在混合物
(3)无水
(4)在蒸馏过程中,减压蒸馏得到的产品纯度和产率均比常压下蒸馏收集233℃馏分高,原因是
(5)若反应中缺少二甲胺,相同条件下几乎没有产品得到,说明二甲胺在反应中起到
(6)本实验所得到的苯乙腈产率是
苯乙酮不仅是重要的化工原料,还是精细化学品,如农药、医药、香料的中间体。一种制备苯乙酮的实验方法及相关信息如下:
I.反应原理:
 +
+

 +CH3COOH
+CH3COOH
已知:①苯乙酮能与氯化铝在无水条件下形成稳定的配合物;
②制备过程中存在副反应CH3COOH+AlCl3→CH3COOAlCl2+HCl↑。
Ⅱ.相关数据:
Ⅲ.实验步骤:
步骤1:合成
实验装置如图,在三颈烧瓶中加入20g AlCl3和30mL苯,在不断搅拌的条件下通过装置M慢慢滴加5.1mL乙酸酐和10mL苯的混合液,在70~80℃下加热回流1小时。
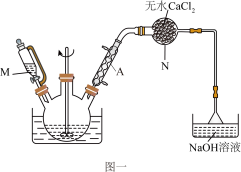
回答下列问题:
(1)仪器A的名称:___________ 。
(2)若将乙酸酐和苯的混合液一次性倒入三颈烧瓶,可能导致___________ 。
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢
(3)反应中所使用的氯化铝会过量很多,原因是___________ 。
步骤2:分离提纯
(4)可通过如下步骤对粗产品提纯:
a.冰水浴冷却下,边搅拌边滴加浓盐酸与冰水的混合液,直至固体完全溶解后停止搅拌,静置,分液。
b.水层用苯萃取,萃取液并入有机层。
c.依次用5% NaOH溶液和水各20mL洗涤。
d.加入无水MgSO4固体。
e.过滤。
f.蒸馏除去苯后,收集198℃~202℃馏分。
其中c操作的目的是除掉有机层中的有机物为___________ ;f操作中收集198℃~202℃馏分的最佳加热方式为___________ 。
A.水浴 B.酒精灯直接加热 C.油浴
(5)本实验为收集产品用了减压蒸馏装置(如图二),其中毛细管的作用是___________ 。经蒸馏后收集到4.8g纯净物,其产率是___________ %(保留三位有效数字)。

I.反应原理:
 +
+
 +CH3COOH
+CH3COOH已知:①苯乙酮能与氯化铝在无水条件下形成稳定的配合物;
②制备过程中存在副反应CH3COOH+AlCl3→CH3COOAlCl2+HCl↑。
Ⅱ.相关数据:
| 物质 | 沸点/℃ | 密度 (g/cm3、20℃) | 相对分子质量 | 溶解性 |
| 苯乙酮 | 202 | 1.03 | 120 | 不溶于水,易溶于多数有机溶剂 |
| 苯 | 80 | 0.88 | 78 | 难溶于水 |
| 乙酸 | 118 | 1.05 | 60 | 能溶于水、乙醇、乙醚、等有机溶剂 |
| 乙酸酐 | 139.8 | 1.08 | 102 | 遇水反应,溶于氯仿、乙醚和苯 |
步骤1:合成
实验装置如图,在三颈烧瓶中加入20g AlCl3和30mL苯,在不断搅拌的条件下通过装置M慢慢滴加5.1mL乙酸酐和10mL苯的混合液,在70~80℃下加热回流1小时。

回答下列问题:
(1)仪器A的名称:
(2)若将乙酸酐和苯的混合液一次性倒入三颈烧瓶,可能导致
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢
(3)反应中所使用的氯化铝会过量很多,原因是
步骤2:分离提纯
(4)可通过如下步骤对粗产品提纯:
a.冰水浴冷却下,边搅拌边滴加浓盐酸与冰水的混合液,直至固体完全溶解后停止搅拌,静置,分液。
b.水层用苯萃取,萃取液并入有机层。
c.依次用5% NaOH溶液和水各20mL洗涤。
d.加入无水MgSO4固体。
e.过滤。
f.蒸馏除去苯后,收集198℃~202℃馏分。
其中c操作的目的是除掉有机层中的有机物为
A.水浴 B.酒精灯直接加热 C.油浴
(5)本实验为收集产品用了减压蒸馏装置(如图二),其中毛细管的作用是

某兴趣小组查阅资料发现:
①苯甲醛在浓NaOH溶液能反应如反应2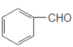 +NaOH→
+NaOH→ +
+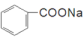
②C6H5CHO+NaHSO3 → C6H5CH(OH)SO3Na
已知相关物质的性质如表所示:
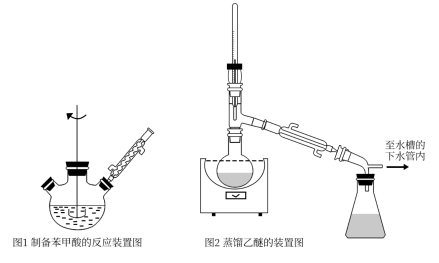
该兴趣小组同学利用上述原理制备苯甲醇,具体实验装置和实验步骤如下:
步骤1:向图1所示装置中加入8gNaOH和30mL水,搅拌溶解。稍冷,加入10mL新蒸馏的苯甲醛。搅拌,加热回流约40min。
步骤2:停止加热,从球形冷凝管上口缓慢加入20mL冷水,摇匀,冷却至室温,然后用乙醚萃取三次,每次10mL,合并有机层,并对其进行一系列洗涤操作。
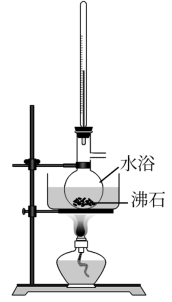
步骤3:洗涤后的有机层,倒入干燥的锥形瓶,加入无水硫酸镁,过滤,将滤液倒入如图2所示的蒸馏装置,先缓慢加热蒸出乙醚;当乙醚蒸出完毕后,改变加热方式继续升温并收集T℃左右的馏分得到苯甲醇。
请回答:
(1)步骤1中所使用的苯甲醛需新蒸馏的原因是___________ 。
(2)步骤2中,进行萃取时所需的玻璃仪器是___________ ;在萃取振摇过程中应进行___________ 操作,分液时分离得到有机层的操作是___________ 。
(3)步骤2中对有机层进行一系列洗涤操作时洗涤剂使用的正确顺序是___________ ;其中加入饱和NaHSO3溶液的作用是___________ 。
a.10mL 10%的Na2CO3溶液 b.5mL 饱和NaHSO3溶液 c.10mL H2O
(4)下列说法正确的是___________ 。
A.步骤1中需冷却、搅拌的原因是防止苯甲醛因温度太高而发生副反应
B.图1,图2装置中都含有冷凝管,进出水方向相同,故可交换使用
C.步骤2萃取可采用30mL乙醚一次性完成,既操作方便又节约时间,提高效率
D.步骤3,无水硫酸镁做干燥剂除去有机层中的水,也可用无水氯化钙代替
E.步骤3,乙醚的沸点较低,故蒸馏时可采用如图所示的水浴加热方式
F.步骤3,T应控制在206℃左右,可采用空气冷凝的方式代替水冷
①苯甲醛在浓NaOH溶液能反应如反应2
 +NaOH→
+NaOH→ +
+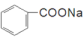
②C6H5CHO+NaHSO3 → C6H5CH(OH)SO3Na
已知相关物质的性质如表所示:
| 名称 | 相对 分子质量 | 密度(g/cm3) | 熔点(oC) | 沸点(oC) | 性质 |
| 苯甲醛 | 106 | 1.04 | -26 | 179.62 | 微溶于水,易溶于醇和醚 |
| 苯甲醇 | 108 | 1.04 | -15.3 | 206 | / |
| 苯甲酸 | 122 | / | 122.13 | 249 | 微溶于水,易溶于醇和醚 |
| 乙醚 | 74 | 0.71 | -116.3 | 34.6 | 不溶于水,易溶于醇;易燃易爆 |
步骤1:向图1所示装置中加入8gNaOH和30mL水,搅拌溶解。稍冷,加入10mL新蒸馏的苯甲醛。搅拌,加热回流约40min。
步骤2:停止加热,从球形冷凝管上口缓慢加入20mL冷水,摇匀,冷却至室温,然后用乙醚萃取三次,每次10mL,合并有机层,并对其进行一系列洗涤操作。
步骤3:洗涤后的有机层,倒入干燥的锥形瓶,加入无水硫酸镁,过滤,将滤液倒入如图2所示的蒸馏装置,先缓慢加热蒸出乙醚;当乙醚蒸出完毕后,改变加热方式继续升温并收集T℃左右的馏分得到苯甲醇。
请回答:

(1)步骤1中所使用的苯甲醛需新蒸馏的原因是
(2)步骤2中,进行萃取时所需的玻璃仪器是
(3)步骤2中对有机层进行一系列洗涤操作时洗涤剂使用的正确顺序是
a.10mL 10%的Na2CO3溶液 b.5mL 饱和NaHSO3溶液 c.10mL H2O
(4)下列说法正确的是

A.步骤1中需冷却、搅拌的原因是防止苯甲醛因温度太高而发生副反应
B.图1,图2装置中都含有冷凝管,进出水方向相同,故可交换使用
C.步骤2萃取可采用30mL乙醚一次性完成,既操作方便又节约时间,提高效率
D.步骤3,无水硫酸镁做干燥剂除去有机层中的水,也可用无水氯化钙代替
E.步骤3,乙醚的沸点较低,故蒸馏时可采用如图所示的水浴加热方式
F.步骤3,T应控制在206℃左右,可采用空气冷凝的方式代替水冷
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


