单选题 适中0.65 引用2 组卷157
周期表前四周期的元素A、B、C、D、E原子序数依次增大。基态原子A的原子轨道半充满,B的价电子层中有3个未成对电子,D的价层电子排布式为nsn-1np2n-2,C与D同族,E的最外层只有1个电子,次外层有18个电子。这5种元素形成的一种1:1型离子化合物中,由C、D所形成的阴离子呈正四面体结构、阳离子呈轴向狭长的八面体结构(如图所示)。下列说法正确的是
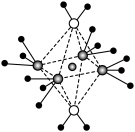
| A.5种原子中第一电离能最大的是C |
| B.A、B所形成的化合物中只含极性键 |
| C.1mol该阳离子中含有24molσ键 |
| D.B、C、D所形成的简单氢化物中,沸点最低的是D |
2023·安徽芜湖·二模
类题推荐
已知A、B、C、D、E是原子序数依次增大且位于周期表中前四周期的元素,其中A、B、C是同一周期的非金属元素,化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构, 为非极性分子,B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高,E的基态原子中有6个未成对电子。下列说法正确的是
为非极性分子,B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高,E的基态原子中有6个未成对电子。下列说法正确的是
| A.A、B、C三种元素的第一电离能依次增大 |
| B.D的二价阳离子半径比C的阴离子半径大 |
| C.元素C与氢元素按原子个数比1∶1形成的化合物是非极性分子 |
| D.E的基态原子的价层电子排布为 |
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,c的最外层电子数为其内层电子数的3倍,b3-与C2-核外电子排布相同, d与c同族;e的最外层只有1个电子,次外层全充满。下列说法错误的是
| A.a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为sp3 |
| B.b、c、d中电负性最大的是d |
C.e的价层电子排布图为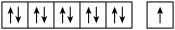 |
| D.这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,该晶体结构中的作用力有离子键、极性键、配位键 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



