解答题-工业流程题 适中0.65 引用2 组卷199
锰酸锂(LiMn2O4)是一种锂电池的正极材料。工业上以方锰矿(主要成分为MnO,还含有少量的Fe3O4、Al2O3、CaO、SiO2))为原料制备锰酸锂的流程如下:
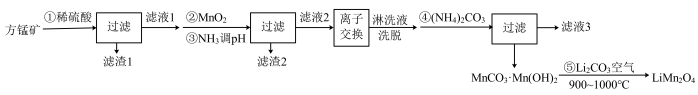
已知:i.25℃时,相关物质的Ksp或Kb如下表:
ii.离子浓度低于1x10-5mol·L-1时即为该离子沉淀完全。回答下列问题:
(1)能加快步骤①反应速率和提高锰元素浸取率的措施有___________ (任写一种)。
(2)滤液1中主要含有的金属离子是___________ ,步骤②中加入MnO2的作用是___________
(3)为了使A13+沉淀完全,步骤③中pH至少调至___________ ;反应Al3+(aq)+3NH3·H2O(aq) Al(OH)3(s)+3NH
Al(OH)3(s)+3NH (aq)的平衡常数K=
(aq)的平衡常数K=___________ 。
(4)步骤④反应未见气体生成,则反应的离子方程式为___________ 。步骤⑤发生的反应中氧化剂与还原剂的物质的量之比为___________ 。
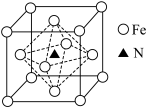
(5)某铁氮化合物晶体的晶胞如图所示,则该晶体的化学式为___________ ;若晶胞中距离最近的两个铁原子距离为apm,阿伏伽德罗常数的值为NA,则晶体的密度为___________ g/cm3(列出计算式即可)。

已知:i.25℃时,相关物质的Ksp或Kb如下表:
| 物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 | NH3·H2O |
| Ksp或Kb | 2×10-13 | 5×10-17 | 1×10-39 | 1×10-32 | 6×10-6 | 2×10-5 |
(1)能加快步骤①反应速率和提高锰元素浸取率的措施有
(2)滤液1中主要含有的金属离子是
(3)为了使A13+沉淀完全,步骤③中pH至少调至
(4)步骤④反应未见气体生成,则反应的离子方程式为
(5)某铁氮化合物晶体的晶胞如图所示,则该晶体的化学式为

2023·安徽·三模
类题推荐
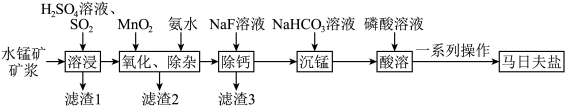
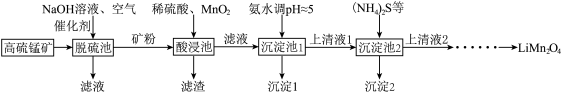
LiMn2O4是一种锂电池材料,以高硫锰矿(主要成分为MnCO3,主要杂质为SiO2、CaCO3,还有少量MnS、FeS、CuS、NiS、FeCO3等)为原料,可按如下工艺生产得到。
已知:①碱性溶液中,在催化剂存在下空气只与硫化物反应,其中硫元素被氧化为单质。
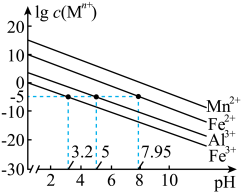
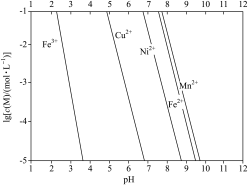
②金属离子的1gc(M)与溶液pH的关系如下图所示。
③25℃时,相关物质的平衡常数见下表。
回答下列问题:
(1)基态Ni原子的价电子中,两种自旋状态的电子数之比为___________ 。
(2)根据矿物组成,“脱硫池”中能被NaOH溶液溶解的杂质是___________ (填化学式,下同)。若未经脱硫直接酸浸,会产生的污染物是___________ 。“滤渣”含有S和___________ 。
(3)①“酸浸池”中主要含锰组分发生反应的化学方程式为___________ 。
②“酸浸池”中加入MnO2的作用是___________ (用离子方程式表示)。
(4)“沉淀1”主要成分是___________ 。25℃时,为了使Cu2+、Ni2+沉淀完全,“上清液2”中H+浓度不大于___________ mol/L(设H2S的平衡浓度为1.0×10-6 mol/L)。
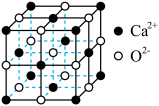
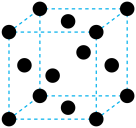
(5)LiMn2O4的晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为apm,已知阿伏加德罗常数的值为NA,则该晶体的摩尔体积Vm=___________ m3/mol。

已知:①碱性溶液中,在催化剂存在下空气只与硫化物反应,其中硫元素被氧化为单质。
②金属离子的1gc(M)与溶液pH的关系如下图所示。

③25℃时,相关物质的平衡常数见下表。
| 化学式 | CuS | NiS | MnS | H2S |
| 平衡常数 | Ksp=6.3×10-36 | Ksp=2.0×10-19 | Ksp=2.5×10-10 | Ka1=1.0×10-7、Ka2=8.0×10-15 |
回答下列问题:
(1)基态Ni原子的价电子中,两种自旋状态的电子数之比为
(2)根据矿物组成,“脱硫池”中能被NaOH溶液溶解的杂质是
(3)①“酸浸池”中主要含锰组分发生反应的化学方程式为
②“酸浸池”中加入MnO2的作用是
(4)“沉淀1”主要成分是
(5)LiMn2O4的晶胞中的氧原子以面心立方堆积(如图),若该晶胞参数为apm,已知阿伏加德罗常数的值为NA,则该晶体的摩尔体积Vm=

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网