单选题 适中0.65 引用1 组卷438
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量。一定条件下,氢气与氧气反应的能量变化如图所示,下列说法中正确的是
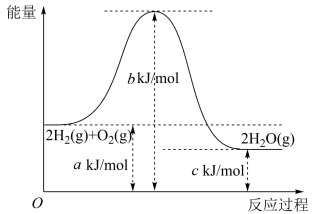

| A.该反应的反应热 |
| B.该反应为吸热反应 |
| C.断裂 |
| D. |
22-23高一下·广东广州·期中
类题推荐
在25℃和101kPa的条件下, 和
和 完全反应生成
完全反应生成 的能量变化如图所示,下列说法
的能量变化如图所示,下列说法不正确 的是


| A.H-H的键能为436kJ/mol |
| B.形成 |
| C.该反应的热化学方程式: |
| D.共价键断裂和形成时的能量变化是该化学反应能量变化的主要原因 |
下图为反应CH4(g)+Cl2(g)→CH3Cl(g)+HCl(g)的变化示意图,下列说法正确的是
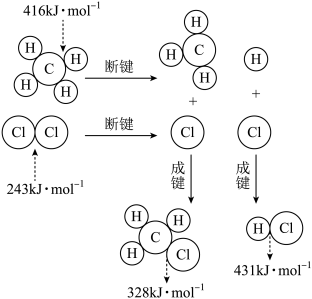

| A.该反应发生的条件为加热 |
| B.化学反应中能量的变化与键的断裂和形成无关 |
| C.断裂化学键放出能量,形成化学键吸收能量 |
| D.由图可知CH4(g)+Cl2(g)→CH3Cl(g)+HCl(g)ΔH=-100kJ·mol-1 |
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的,图为 和
和 反应生成
反应生成 过程中的能量变化,下列说法不正确的是
过程中的能量变化,下列说法不正确的是


| A. |
| B.该反应中反应物的总能量小于生成物的总能量 |
| C.该反应中,每生成1 mol |
| D.该过程说明 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


