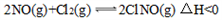解答题-原理综合题 适中0.65 引用1 组卷87
NOx会造成大气污染,在工业上采用多种方法进行处理。
I.氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知:常温下,Ksp(CaSO4)=9.1×10-6,Ksp(CaSO3)=3.1×10-7。
(1)NO与O3反应过程的能量变化如下:
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ•mol-1
NO(g)+ O2(g)=NO2(g) △H=-58.2kJ•mol-1
O2(g)=NO2(g) △H=-58.2kJ•mol-1
则3NO(g)+O3(g)=3NO2(g) △H=______ 。
(2)用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为______ 。
(3)在实际吸收NO2的过程中,通过向CaSO3悬浊液中加入Na2SO4固体,提高NO2的吸收速率,从溶解平衡的角度解释其原因:______ 。
Ⅱ.有人提出用活性炭对NOx进行吸附,比如吸收NO2的反应如下:2C(s)+2NO2(g) N2(g)+2CO2(g) △H=-62.4kJ•mol-1。在密闭容器中加入足量的C和一定量的NO2气体,维持温度为T2℃,如图为不同压强下反应经过相同时间NO2的转化率随着压强变化的示意图。
N2(g)+2CO2(g) △H=-62.4kJ•mol-1。在密闭容器中加入足量的C和一定量的NO2气体,维持温度为T2℃,如图为不同压强下反应经过相同时间NO2的转化率随着压强变化的示意图。
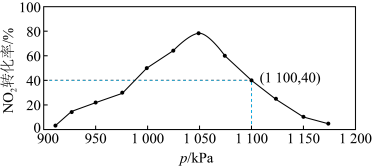
(4)请分析,1050kPa前,NO2转化率随着压强增大而增大的原因:______ 。
(5)在1100kPa时,NO2的体积分数为______ 。用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp),在T2℃、1100kPa时,该反应的化学平衡常数Kp=______ (只需列出计算式 )。已知:气体分压(p分)=气体总压(p总)×体积分数。
I.氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知:常温下,Ksp(CaSO4)=9.1×10-6,Ksp(CaSO3)=3.1×10-7。
(1)NO与O3反应过程的能量变化如下:
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ•mol-1
NO(g)+
则3NO(g)+O3(g)=3NO2(g) △H=
(2)用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为
(3)在实际吸收NO2的过程中,通过向CaSO3悬浊液中加入Na2SO4固体,提高NO2的吸收速率,从溶解平衡的角度解释其原因:
Ⅱ.有人提出用活性炭对NOx进行吸附,比如吸收NO2的反应如下:2C(s)+2NO2(g)

(4)请分析,1050kPa前,NO2转化率随着压强增大而增大的原因:
(5)在1100kPa时,NO2的体积分数为
22-23高二下·海南海口·期中
类题推荐
NOx的排放主要来自于汽车尾气,包含NO2和NO,有人提出用活性炭对NOx进行吸附,发生反应如下:
反应a:C(s)+2NO(g)⇌N2(g)+CO2(g)ΔH=-34.0kJ/mol
反应b:2C(s)+2NO2(g)⇌N2(g)+2CO2(g) ΔH=-64.2kJ/mol
(1)对于反应a,在T1℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
①0~10min内,NO的平均反应速率v(NO)=_____ ,当升高反应温度,该反应的平衡常数K____________ (选填“增大”、“减小”或“不变”)。
②30min后,只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是_________ (填字母)。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
(2)某实验室模拟反应b,在密闭容器中加入足量的C和一定量的NO2气体,维持温度为T2℃,如图为不同压强下反应b经过相同时间NO2的转化率随着压强变化的示意图。

请从动力学角度分析,1050kPa前,反应b中NO2转化率随着压强增大而增大的原因____________ ;在1100kPa时,NO2的体积分数为_________________________ 。
(3)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp);在T2℃、1.1×106Pa时,该反应的化学平衡常数Kp=___________ (计算表达式表示);已知:气体分压(P分)=气体总压(P总)×体积分数。
反应a:C(s)+2NO(g)⇌N2(g)+CO2(g)ΔH=-34.0kJ/mol
反应b:2C(s)+2NO2(g)⇌N2(g)+2CO2(g) ΔH=-64.2kJ/mol
(1)对于反应a,在T1℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
| 时间 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10min内,NO的平均反应速率v(NO)=
②30min后,只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
(2)某实验室模拟反应b,在密闭容器中加入足量的C和一定量的NO2气体,维持温度为T2℃,如图为不同压强下反应b经过相同时间NO2的转化率随着压强变化的示意图。

请从动力学角度分析,1050kPa前,反应b中NO2转化率随着压强增大而增大的原因
(3)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp);在T2℃、1.1×106Pa时,该反应的化学平衡常数Kp=
Ⅰ.分解HI曲线和液相法制备HI反应曲线分别如图1和图2所示:

(1)反应H2(g)+I2(g)⇌HI(g)的△H_____ (填“大于”或“小于”)0。
(2)将二氧化硫通入碘水中会发生反应:SO2+I2+2H2O⇌3H++HSO +2I-,I2+ I-⇌I
+2I-,I2+ I-⇌I ,图2中曲线a、b分别代表的微粒是
,图2中曲线a、b分别代表的微粒是_______ (填微粒符号);由图2知要提高碘的还原率,除控制温度外,还可以采取的措施是_________ 。
Ⅱ.NOx的排放主要来自于汽车尾气,包含NO2和NO,有人提出用活性炭对NOx进行吸附,发生反应如下:
反应a:C(s)+2NO(g)⇌N2(g)+CO2(g)△H =-34.0kJ/mol
反应b:2C(s)+2NO2(g)⇌N2(g)+2CO2(g)△H =-64.2kJ/mol
(3)对于密闭容器中反应a,在T1℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
30 min后,只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是______ (填字母代号)。
A加入一定量的活性炭B.通入一定量的NO
C.适当缩小容器的体积D.加入合适的催化剂
(4)①某实验室模拟反应b,在密用容器中加入足量的C和一定量的NOx气体,维持温度为T2℃,如图为不同压强下反应b经过相同时间NO2的转化率随着压强变化的示意图。请分析,1050kPa前,反应b中NO2转化率随着压强增大而增大的原因是______ 。

②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp);在T2℃、1.1×106Pa时,该反应的化学平衡常数Kp=_______ (用计算表达式表示);已知:气体分压(p分)=气体总压(p总)×体积分数。

(1)反应H2(g)+I2(g)⇌HI(g)的△H
(2)将二氧化硫通入碘水中会发生反应:SO2+I2+2H2O⇌3H++HSO
Ⅱ.NOx的排放主要来自于汽车尾气,包含NO2和NO,有人提出用活性炭对NOx进行吸附,发生反应如下:
反应a:C(s)+2NO(g)⇌N2(g)+CO2(g)△H =-34.0kJ/mol
反应b:2C(s)+2NO2(g)⇌N2(g)+2CO2(g)△H =-64.2kJ/mol
(3)对于密闭容器中反应a,在T1℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
| 0 | 10 | 20 | 30 | 40 | 50 | |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
30 min后,只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是
A加入一定量的活性炭B.通入一定量的NO
C.适当缩小容器的体积D.加入合适的催化剂
(4)①某实验室模拟反应b,在密用容器中加入足量的C和一定量的NOx气体,维持温度为T2℃,如图为不同压强下反应b经过相同时间NO2的转化率随着压强变化的示意图。请分析,1050kPa前,反应b中NO2转化率随着压强增大而增大的原因是

②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp);在T2℃、1.1×106Pa时,该反应的化学平衡常数Kp=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网