解答题-实验探究题 适中0.65 引用1 组卷198
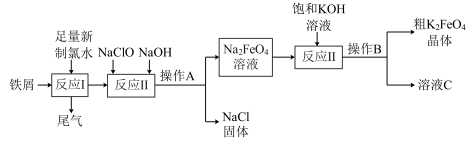
高铁酸钾(K2FeO4)是一种环保、高效饮水处理剂,利用铁屑制备的简略流程如图所示:

请回答下列问题:
(1)反应Ⅰ的生成物中可能含有的金属阳离子是___________ (用离子符号表示),如何检验该离子___________ 。
(2)操作A和操作B相同,其操作名称是___________ ;由操作B判断该生产条件下物质的溶解性:Na2FeO4___________ K2FeO4 (填“>”或“<”)。
(3)溶液C可与氯气反应制取漂白液,其离子方程式为___________ 。
(4)当生产过程中制得2mol的K2FeO4时,反应Ⅱ中转移的电子数为___________ 。
(5)反应Ⅱ中用到NaOH,若某同学做实验时要用到200mL 0.1mol/L NaOH溶液,现进行配制,则:
①配制该浓度的溶液需用托盘天平称量NaOH固体的质量为___________ g;
②配制过程中,下列操作导致所配溶液浓度偏大的是___________ (填标号)。
a.转移溶液时有少许液体溅出
b.溶解后,将溶液直接转移到容量瓶中
c.定容时俯视刻度线
d.定容摇匀后,发现液面下降,继续加水至刻度线

请回答下列问题:
(1)反应Ⅰ的生成物中可能含有的金属阳离子是
(2)操作A和操作B相同,其操作名称是
(3)溶液C可与氯气反应制取漂白液,其离子方程式为
(4)当生产过程中制得2mol的K2FeO4时,反应Ⅱ中转移的电子数为
(5)反应Ⅱ中用到NaOH,若某同学做实验时要用到200mL 0.1mol/L NaOH溶液,现进行配制,则:
①配制该浓度的溶液需用托盘天平称量NaOH固体的质量为
②配制过程中,下列操作导致所配溶液浓度偏大的是
a.转移溶液时有少许液体溅出
b.溶解后,将溶液直接转移到容量瓶中
c.定容时俯视刻度线
d.定容摇匀后,发现液面下降,继续加水至刻度线
22-23高一下·重庆巫溪·阶段练习
类题推荐
“84”消毒液是生活中常见的含氮消毒剂
(1)阅读资料,回答下列相关问题。
资料:“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。“84”消毒液呈无色或淡黄色,可由 与NaOH溶液反应制得,其主要成分为NaClO、NaCl。
与NaOH溶液反应制得,其主要成分为NaClO、NaCl。
①资料涉及的物质中,属于碱的是___________ (填化学式,下同);属于盐的是___________ 。
② 与NaOH溶液反应制取“84”消毒液的离子方程式为
与NaOH溶液反应制取“84”消毒液的离子方程式为___________ 。
③“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中 使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:___________ 。
(2)如果“84”消毒液与洁厕灵(浓盐酸)混用,会产生一种黄绿色有毒气体,无其它含氯产物,请写出产生该气体的离子方程式:___________ 。
(3)实验室需使用480mL 1.0mol/L的NaOH溶液来制备“84”消毒液。因此首先配制该NaOH溶液。回答下列问题。
①实验需要称量的NaOH固体的质量为___________ g。必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、胶头滴管和___________ 。称量NaOH固体___________ (填“是”或“否”)可以使用称量纸进行称量。
②下列实验操作步骤的顺序为_________________ (填字母序号)。
③配制过程中,下列操作会引起所配制溶液浓度偏低的是___________ (填字母序号)。
a.NaOH固体已经潮解 b.定容时,俯视容量瓶刻度
c.未洗涤烧杯和玻璃棒 d.摇匀后,发现液面低于刻度线,继续加水至刻度线
(1)阅读资料,回答下列相关问题。
资料:“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。“84”消毒液呈无色或淡黄色,可由
①资料涉及的物质中,属于碱的是
②
③“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中
(2)如果“84”消毒液与洁厕灵(浓盐酸)混用,会产生一种黄绿色有毒气体,无其它含氯产物,请写出产生该气体的离子方程式:
(3)实验室需使用480mL 1.0mol/L的NaOH溶液来制备“84”消毒液。因此首先配制该NaOH溶液。回答下列问题。
①实验需要称量的NaOH固体的质量为
②下列实验操作步骤的顺序为
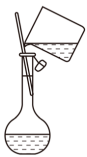 | 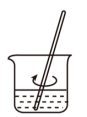 | 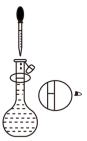 |  |
| a.转移 | b.溶解 | c.定容 | d.洗涤 |
a.NaOH固体已经潮解 b.定容时,俯视容量瓶刻度
c.未洗涤烧杯和玻璃棒 d.摇匀后,发现液面低于刻度线,继续加水至刻度线
高铁酸钾( )是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的方法主要有湿法和干法两种。
)是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的方法主要有湿法和干法两种。
Ⅰ.实验室模拟湿法制备高铁酸钾的流程如下:
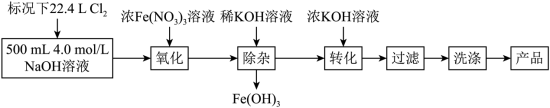
已知:“转化”过程发生复分解反应。
回答下列问题:
(1)配制上述NaOH溶液,下列操作可能导致溶液浓度偏大的是___________(填序号)。
(2)NaOH溶液应置于冰水浴中,否则温度升高将发生副反应:
主反应:Cl2+2NaOH=NaCl+NaClO+H2O
副反应: (未配平)
(未配平)
①配平该副反应:________
___________Cl2+___________NaOH=___________NaCl+___________NaClO3+___________H2O
②若有 发生该副反应,该过程中转移电子的物质的量为
发生该副反应,该过程中转移电子的物质的量为___________ mol;
(3)氧化过程中溶液保持强碱性,写出反应的离子方程式:___________ 。
Ⅱ.工业干法制备高铁酸钾:
第一步反应为:2FeSO4+6Na2O2 2Na2FeO4+2Na2O+2Na2SO4+O2↑
2Na2FeO4+2Na2O+2Na2SO4+O2↑
第二步反应在溶液中进行:
(4)该第一步反应中氧化产物为___________ 、___________ ,
(5)试解释第二步反应能发生的原因___________ 。
(6)K2FeO4在净水过程中能产生Fe(OH)3胶体,检验净水过程中产生了胶体的方法是___________ 。
Ⅰ.实验室模拟湿法制备高铁酸钾的流程如下:

已知:“转化”过程发生复分解反应。
回答下列问题:
(1)配制上述NaOH溶液,下列操作可能导致溶液浓度偏大的是___________(填序号)。
| A.摇匀后发现液面低于刻度线,再加水至刻度线 | B.NaOH在烧杯中溶解后,烧杯未洗涤 |
| C.容量瓶洗净之后未干燥 | D.定容时俯视刻度线 |
主反应:Cl2+2NaOH=NaCl+NaClO+H2O
副反应:
①配平该副反应:
___________Cl2+___________NaOH=___________NaCl+___________NaClO3+___________H2O
②若有
(3)氧化过程中溶液保持强碱性,写出反应的离子方程式:
Ⅱ.工业干法制备高铁酸钾:
第一步反应为:2FeSO4+6Na2O2
第二步反应在溶液中进行:
(4)该第一步反应中氧化产物为
(5)试解释第二步反应能发生的原因
(6)K2FeO4在净水过程中能产生Fe(OH)3胶体,检验净水过程中产生了胶体的方法是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网