解答题-工业流程题 较难0.4 引用1 组卷134
废钼催化剂中钼、钴、镍等金属作为二次资源可加以回收利用,一种从废钼催化剂(主要成分为MoO3、MoS2,含少量CoO、CoS、NiO、Fe2O3等)中回收金属的一种工艺流程如图:
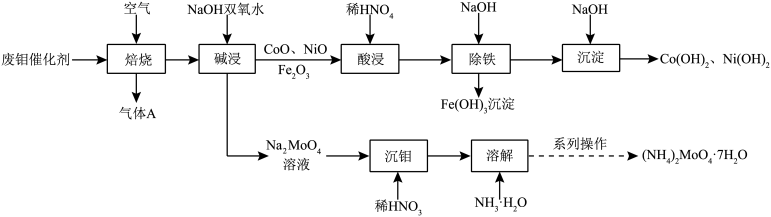
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)Ni2+价层电子轨道表示式为________ ,“焙烧”时产生的气体A的主要成分为________ 。
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式_________ 。
(3)“除铁”时应调节溶液pH的范围为___________ ,“沉淀”时调节溶液pH=9.0,则此时溶液中[ =
=___________ (pX=-lgX)。
(4)“系列操作”为________ 、________ 、过滤、洗涤、干燥得到(NH4)2MoO4·7H2O晶体。
(5)50.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为___________ %(保留小数点后一位数字,收率= )。
)。

已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Co2+ | Ni2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 2.2 3.2 | 6.4 9.0 | 7.2 8.7 |
(1)Ni2+价层电子轨道表示式为
(2)“焙烧”时MoS2转化为MoO3,写出“碱浸”时MoO3参与反应的离子方程式
(3)“除铁”时应调节溶液pH的范围为
(4)“系列操作”为
(5)50.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到15.05kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为
2023·安徽铜陵·模拟预测
类题推荐
废钼催化剂中含有钼、钴、镍等非常有价值的金属元素,回收其中的金属具有巨大的经济和环境意义。一种从废钼催化剂(主要成分为 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有价值金属的工艺流程如下图。
等)中回收有价值金属的工艺流程如下图。
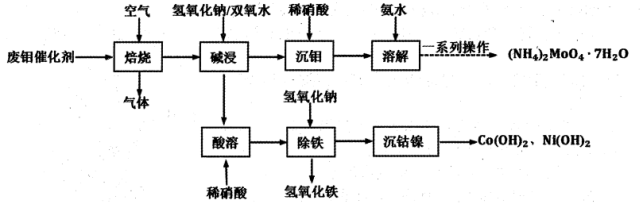
已知:①碱浸后滤液中主要成分为 。
。
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
③钼酸铵 为白色晶体,具有很高的水溶性,不溶于乙醇。
为白色晶体,具有很高的水溶性,不溶于乙醇。
回答下列问题:
(1)钼酸铵 中Mo元素的化合价为
中Mo元素的化合价为___________ ;“焙烧”时 转化为
转化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“碱浸”时NaOH加入量/钼理论耗量、浸出温度、浸出时间对钼浸出率的影响如图所示。
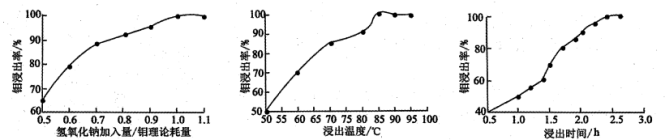
则“碱浸”时适宜的生产工艺条件:氢氧化钠加入量/钼理论耗量___________ 、浸出温度___________ 、浸出时间2.4h。
(3)“除铁”时应调节溶液pH的范围为___________ 。
(4)若“沉钴镍”时调节溶液pH=9.5,则此时溶液中
___________ (pX=-lgX)。
(5)经过降温结晶、过滤、洗涤、干燥等操作得到 晶体,洗涤时所选用的最佳试剂为
晶体,洗涤时所选用的最佳试剂为___________ 。
(6)100.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到30.10kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为___________ %(保留一位小数。收率 )。
)。

已知:①碱浸后滤液中主要成分为
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | |||
| 开始沉淀时的pH | 2.2 | 6.4 | 7.2 |
| 沉淀完全时( | 3.2 | 9.0 | 8.7 |
回答下列问题:
(1)钼酸铵
(2)“碱浸”时NaOH加入量/钼理论耗量、浸出温度、浸出时间对钼浸出率的影响如图所示。

则“碱浸”时适宜的生产工艺条件:氢氧化钠加入量/钼理论耗量
(3)“除铁”时应调节溶液pH的范围为
(4)若“沉钴镍”时调节溶液pH=9.5,则此时溶液中
(5)经过降温结晶、过滤、洗涤、干燥等操作得到
(6)100.00kg该废钼催化剂(含Mo元素质量分数为10.56%)通过该工艺最终得到30.10kg七水钼酸铵(相对分子质量为322)产品,则该工艺中七水钼酸铵的收率为
一种从废钼催化剂(主要成分为MoO3、MoS2,含少量CoO、CoS、NiO、Fe2O3等)中回收有价值金属的工艺流程如图。
②溶液中金属离子开始沉淀和完全沉淀的pH如表:
③钼酸铵[(NH4)2MoO4]为白色晶体,具有很高的水溶性,不溶于乙醇。
回答下列问题:
(1)催化剂中含多种金属元素,其中铁在元素周期表中的位置:第______ 周期第_____ 族。基态Co原子的价电子排布式为______ 。
(2)钼酸铵[(NH4)2MoO4]中Mo元素的化合价为______ ;“焙烧”时MoS2转化为MoO3,该反应的化学方程式为______ 。
(3)“碱浸”时,浸出温度、NaOH加入量/钼理论耗量对钼浸出率的影响如图。______ 、NaOH加入量/钼理论耗量______ 。
(4)“除铁”时应调节溶液pH的范围为_______ 。
(5)若“沉钴镍”时调节溶液pH=9.5,则此时溶液中p =
=______ (pX=-lgX)。
(6)经过降温结晶、过滤、洗涤、干燥等操作得到(NH4)2MoO4•7H2O晶体,洗涤时所选用的最佳试剂为______ 。

②溶液中金属离子开始沉淀和完全沉淀的pH如表:
| 金属离子 | Fe3+ | Co2+ | Ni2+ |
| 开始沉淀时的pH | 2.2 | 6.4 | 7.2 |
| 沉淀完全时(c=1.0×10-5mol•L-1)的pH | 3.2 | 9.0 | 8.7 |
回答下列问题:
(1)催化剂中含多种金属元素,其中铁在元素周期表中的位置:第
(2)钼酸铵[(NH4)2MoO4]中Mo元素的化合价为
(3)“碱浸”时,浸出温度、NaOH加入量/钼理论耗量对钼浸出率的影响如图。
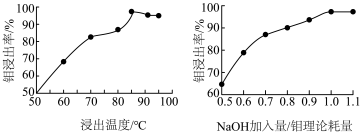
(4)“除铁”时应调节溶液pH的范围为
(5)若“沉钴镍”时调节溶液pH=9.5,则此时溶液中p
(6)经过降温结晶、过滤、洗涤、干燥等操作得到(NH4)2MoO4•7H2O晶体,洗涤时所选用的最佳试剂为
实现废钨——镍型加氢催化剂(主要成分为 ,还含有
,还含有 和少量含
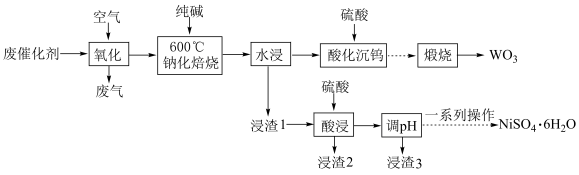
和少量含 有机物)中有价值金属回收的工艺流程如下。
有机物)中有价值金属回收的工艺流程如下。 ,纯碱不与
,纯碱不与 反应。
反应。
ⅱ.相关金属离子[c0(Mn+)=0.1mol/L]形成氢氧化物沉淀的 范围如下:
范围如下:
回答下列问题:
(1)28Ni位于元素周期表的第__________ 周期、__________ 族。
(2)“氧化”的目的为__________ 和将金属单质氧化至相应价态。
(3)“钠化焙烧”中生成 的化学方程式为
的化学方程式为__________ 。
(4)“酸化沉钨”后过滤,所得滤饼的主要成分为__________ (填化学式)。
(5)“调 ”除铁和铝,溶液的
”除铁和铝,溶液的 范围应调节为
范围应调节为__________ 。
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
“一系列操作”依次是__________ 、及时过滤、洗涤、干燥。
(7)强碱溶液中NaClO氧化NiSO4,可沉淀出用作电池正极材料的NiOOH,该反应的离子方程式为__________ 。
ⅱ.相关金属离子[c0(Mn+)=0.1mol/L]形成氢氧化物沉淀的
| 金属离子 | Ni2+ | Al3+ | Fe3+ |
| 开始沉淀时的pH | 6.9 | 3.4 | 1.5 |
| 沉淀完全时的pH | 8.9 | 4.7 | 2.8 |
(1)28Ni位于元素周期表的第
(2)“氧化”的目的为
(3)“钠化焙烧”中生成
(4)“酸化沉钨”后过滤,所得滤饼的主要成分为
(5)“调
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
| 温度 | 低于 | 高于 | ||
| 晶体形态 | 多种结晶水合物 |
(7)强碱溶液中NaClO氧化NiSO4,可沉淀出用作电池正极材料的NiOOH,该反应的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


