解答题-实验探究题 适中0.65 引用2 组卷293
2-甲基-2-丁醇是一种重要的有机化合物,可用于合成香料、农药等。某化学兴趣小组欲利用格氏试剂法制备2-甲基-2-丁醇。实验原理及具体操作步骤如下:
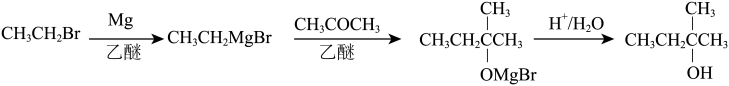
Ⅰ.乙基溴化镁的制备
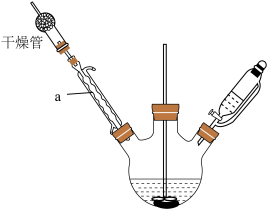
如图安装好装置(夹持仪器未画出),在三颈烧瓶中加入1.7g镁屑及一小粒碘。在恒压滴液漏斗中加入5.0mL溴乙烷和15mL无水乙醚,混匀。开动搅拌,慢慢滴加混合液,维持反应液呈微沸状态。滴加完毕后,用温热回流搅拌30min,使镁屑几乎作用完全。
Ⅱ.与丙酮的加成反应
将三颈烧瓶置于冰水浴中,在搅拌下从恒压漏斗中缓慢滴入5mL丙酮及5mL无水乙醚混合液,滴加完毕后,在室温下搅拌15min,瓶中有灰白色粘稠状固体析出。
Ⅲ.加成物的水解和产物的提取
将三颈烧瓶在冰水冷却和搅拌下,从恒压漏斗中滴入30mL20%硫酸溶液。滴加完毕后,分离出醚层,水层用无水乙醚萃取2次,合并醚层,用5%碳酸钠溶液洗涤,再用无水碳酸钾干燥。搭建蒸馏装置,热水浴蒸去乙醚后,收集95~105℃馏分。称重,计算产率。
已知:①RMgBr化学性质活泼,易与 、R′X等发生反应生成RH、R-R′;
、R′X等发生反应生成RH、R-R′;
②各物质的沸点见下表:
回答下列问题:
(1)仪器a的名称是___________ 。
(2)干燥管中无水氯化钙的作用是___________ 。
(3)微热或加入小颗粒碘单质可引发 与镁屑的反应,其中碘的作用可能是
与镁屑的反应,其中碘的作用可能是___________ ;不宜使用长时间放置的镁屑进行实验,其原因是___________ 。
(4)滴加丙酮及稀硫酸时采用冰水冷却的目的是___________ 。
(5)蒸去乙醚时采用热水浴的原因是___________ 。
(6)起始加入三颈烧瓶中溴乙烷的体积为5mL,密度为1.28g/mL,最终所得产品的质量为2.69g,则2-甲基-2-丁醇的产率为___________ (结果保留2位有效数字)。

Ⅰ.乙基溴化镁的制备
如图安装好装置(夹持仪器未画出),在三颈烧瓶中加入1.7g镁屑及一小粒碘。在恒压滴液漏斗中加入5.0mL溴乙烷和15mL无水乙醚,混匀。开动搅拌,慢慢滴加混合液,维持反应液呈微沸状态。滴加完毕后,用温热回流搅拌30min,使镁屑几乎作用完全。
Ⅱ.与丙酮的加成反应
将三颈烧瓶置于冰水浴中,在搅拌下从恒压漏斗中缓慢滴入5mL丙酮及5mL无水乙醚混合液,滴加完毕后,在室温下搅拌15min,瓶中有灰白色粘稠状固体析出。
Ⅲ.加成物的水解和产物的提取
将三颈烧瓶在冰水冷却和搅拌下,从恒压漏斗中滴入30mL20%硫酸溶液。滴加完毕后,分离出醚层,水层用无水乙醚萃取2次,合并醚层,用5%碳酸钠溶液洗涤,再用无水碳酸钾干燥。搭建蒸馏装置,热水浴蒸去乙醚后,收集95~105℃馏分。称重,计算产率。
已知:①RMgBr化学性质活泼,易与
②各物质的沸点见下表:
| 物质 | 无水乙醚 | 溴乙烷 | 丙酮 | 2-甲基-2-丁醇 |
| 沸点(℃) | 34.6 | 38.4 | 56.5 | 102.5 |

回答下列问题:
(1)仪器a的名称是
(2)干燥管中无水氯化钙的作用是
(3)微热或加入小颗粒碘单质可引发
(4)滴加丙酮及稀硫酸时采用冰水冷却的目的是
(5)蒸去乙醚时采用热水浴的原因是
(6)起始加入三颈烧瓶中溴乙烷的体积为5mL,密度为1.28g/mL,最终所得产品的质量为2.69g,则2-甲基-2-丁醇的产率为
2023·湖北武汉·模拟预测
类题推荐
2-甲基-2-己醇可以通过以下步骤合成:
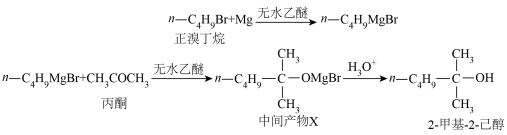
已知:①格氏试剂(RMgBr)是有机合成中的重要试剂,性质活泼,易水解,可与卤代烃、醛、酮、酸、酯等物质反应,如 ;
;
②共沸物是指当两种或多种不同成分的均相溶液,以一个特定的比例混合时,在固定的压力下,仅具有一个沸点,此时这个混合物即称做共沸物。
③几种物质的物理性质如下(*为该物质与水的共沸物的沸点):
实验步骤如下:
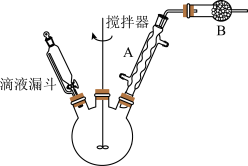
①制备格氏试剂:如图组装装置,在三颈烧瓶中加入3.0g镁条,在恒压滴液漏斗中加入14.5mL正溴丁烷和15mL无水乙醚混合液,先滴入约4mL混合液于三颈烧瓶中,反应开始后溶液微沸,开动搅拌器,缓慢滴入其余的混合液,以保持溶液微微沸腾,加完后,温水浴加热回流20min直至镁条完全反应。
②制备2-甲基-2-己醇:将三颈烧瓶在冰水浴冷却和搅拌下,自恒压滴液漏斗滴入10mL丙酮与15mL无水乙醚的混合液,控制滴加速度,保持微沸,加完后,在室温下继续搅拌15min。将三颈烧瓶在冰水浴冷却和搅拌下,自恒压滴液漏斗慢慢加入100mL 10%硫酸溶液。
③分离提纯:待反应完全后,将液体转入250mL的分液漏斗中,进行操作Ⅰ,水层用乙醚萃取2次,合并醚层,用30mL 5%的碳酸钠溶液洗涤一次,进行操作Ⅰ,用无水碳酸钾干燥,将干燥后的粗产物醚溶液倒入蒸馏烧瓶中,先蒸出乙醚,再蒸馏收集139~143℃的馏分,得到精制产品8.7g。
回答下列问题:
(1)仪器A的名称是___________ ,仪器B的作用是_______ 。
(2)步骤①中正溴丁烷不能大大过量,可能的原因是_______ 。回流结束后,需进行的操作有①停止加热 ②关闭冷凝水 ③移去水浴,正确的顺序为_______ (填标号)。
A.①②③ B.③①② C.②①③ D.①③②
(3)步骤②中反应的中间产物X极易水解生成碱式盐,该反应的化学方程式为___________ 。
(4)步骤③中,操作Ⅰ的主要内容是___________ ,用碳酸钠溶液洗涤的目的是___________ ,用碳酸钾固体干燥再蒸馏的原因是___________ 。
(5)理论上,该实验的产率为___________ %(保留整数)。

已知:①格氏试剂(RMgBr)是有机合成中的重要试剂,性质活泼,易水解,可与卤代烃、醛、酮、酸、酯等物质反应,如
②共沸物是指当两种或多种不同成分的均相溶液,以一个特定的比例混合时,在固定的压力下,仅具有一个沸点,此时这个混合物即称做共沸物。
③几种物质的物理性质如下(*为该物质与水的共沸物的沸点):
| 物质 | 摩尔质量( | 沸点(℃) | 密度( | 溶解性 |
| 乙醚 | 74 | 34.5 | 0.71 | 微溶于水 |
| 正溴丁烷 | 137 | 101 | 1.3 | 难溶于水,能溶于乙醚 |
| 丙酮 | 58 | 56.5 | 0.79 | 易溶于水、乙醚等溶剂 |
| 2-甲基-2-己醇 | 116 | 143(87.4) | 0.81 | 难溶于水,能溶于乙醚 |
①制备格氏试剂:如图组装装置,在三颈烧瓶中加入3.0g镁条,在恒压滴液漏斗中加入14.5mL正溴丁烷和15mL无水乙醚混合液,先滴入约4mL混合液于三颈烧瓶中,反应开始后溶液微沸,开动搅拌器,缓慢滴入其余的混合液,以保持溶液微微沸腾,加完后,温水浴加热回流20min直至镁条完全反应。

②制备2-甲基-2-己醇:将三颈烧瓶在冰水浴冷却和搅拌下,自恒压滴液漏斗滴入10mL丙酮与15mL无水乙醚的混合液,控制滴加速度,保持微沸,加完后,在室温下继续搅拌15min。将三颈烧瓶在冰水浴冷却和搅拌下,自恒压滴液漏斗慢慢加入100mL 10%硫酸溶液。
③分离提纯:待反应完全后,将液体转入250mL的分液漏斗中,进行操作Ⅰ,水层用乙醚萃取2次,合并醚层,用30mL 5%的碳酸钠溶液洗涤一次,进行操作Ⅰ,用无水碳酸钾干燥,将干燥后的粗产物醚溶液倒入蒸馏烧瓶中,先蒸出乙醚,再蒸馏收集139~143℃的馏分,得到精制产品8.7g。
回答下列问题:
(1)仪器A的名称是
(2)步骤①中正溴丁烷不能大大过量,可能的原因是
A.①②③ B.③①② C.②①③ D.①③②
(3)步骤②中反应的中间产物X极易水解生成碱式盐,该反应的化学方程式为
(4)步骤③中,操作Ⅰ的主要内容是
(5)理论上,该实验的产率为
三苯甲醇是一种重要的有机合成中间体,可以通过下列原理进行合成:
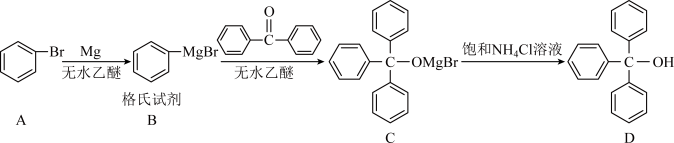
已知:①格氏试剂(RMgBr)性质活泼,可与水、卤代烃、醛、酮等物质反应。
②ROMgBr可发生水解。
③几种物质的物理性质如表所示(表中括号内的数据表示该有机物与水形成的具有固定组成的混合物的共沸点):
实验步骤如下:
制备三苯甲醇:在图1所示的仪器甲中加入1.5 g镁屑,恒压滴液漏斗中加入25.0 mL无水乙醚和7.0 mL溴苯(约0.065 mol)的混合液,启动搅拌器,先将部分混合液加入甲中,开始反应,再逐滴加入余下的混合液,充分反应后,将甲置于冰水浴中,滴加11.0 g二苯酮(约0.060 mol)和25.0 mL无水乙醚的混合液,水浴回流60 min,慢慢滴加30.0 mL饱和 溶液。
溶液。
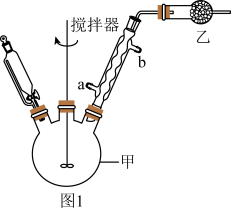
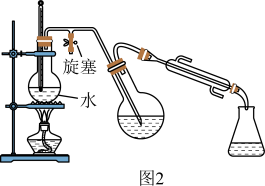
提纯三苯甲醇:用图2所示的水蒸气蒸馏装置分离出乙醚、溴苯并回收利用,向残留液中加入石油醚,获取粗产品。
请回答下列问题:
(1)除去镁条表面氧化膜并将其剪成屑状的目的是___________ 。
(2)仪器甲的名称为___________ ,球形冷凝管的进水口为___________ (填“a”或“b”),装置乙的作用为___________ 。
(3)反应原理中C→D使用饱和 溶液的作用是
溶液的作用是___________ 。
(4)水蒸气蒸馏能除去溴苯的原因是___________ ,加入石油醚后分离出粗产品的操作为___________ 。
(5)若粗产品经___________ (填提纯方法)得到8.8 g三苯甲醇,则三苯甲醇的产率为___________ (保留三位有效数字)。

已知:①格氏试剂(RMgBr)性质活泼,可与水、卤代烃、醛、酮等物质反应。
②ROMgBr可发生水解。
③几种物质的物理性质如表所示(表中括号内的数据表示该有机物与水形成的具有固定组成的混合物的共沸点):
| 物质 | 相对分子质量 | 沸点/℃ | 存在状态及溶解性 |
| 乙醚 | 74 | 34.6 | 微溶于水 |
| 溴苯 | 157 | 156.2(92.8) | 不溶于水的液体,溶于乙醚、乙醇 |
| 二苯酮 | 182 | 305.4 | 不溶于水的晶体,溶于乙醚 |
| 三苯甲醇 | 260 | 380.0 | 不溶于水及石油醚的白色晶体,溶于乙醇、乙醚 |
制备三苯甲醇:在图1所示的仪器甲中加入1.5 g镁屑,恒压滴液漏斗中加入25.0 mL无水乙醚和7.0 mL溴苯(约0.065 mol)的混合液,启动搅拌器,先将部分混合液加入甲中,开始反应,再逐滴加入余下的混合液,充分反应后,将甲置于冰水浴中,滴加11.0 g二苯酮(约0.060 mol)和25.0 mL无水乙醚的混合液,水浴回流60 min,慢慢滴加30.0 mL饱和

提纯三苯甲醇:用图2所示的水蒸气蒸馏装置分离出乙醚、溴苯并回收利用,向残留液中加入石油醚,获取粗产品。

请回答下列问题:
(1)除去镁条表面氧化膜并将其剪成屑状的目的是
(2)仪器甲的名称为
(3)反应原理中C→D使用饱和
(4)水蒸气蒸馏能除去溴苯的原因是
(5)若粗产品经
三苯甲醇是一种重要的有机合成中间体,可以通过下列原理进行合成。
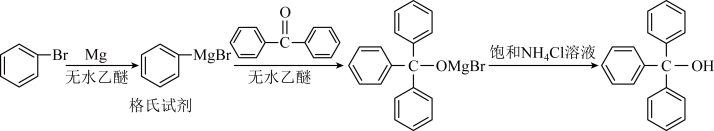
已知:
①格氏试剂(RMgBr)性质活泼,可与水、二氧化碳、卤代烃、醛、酮等物质反应,如:
②
③几种物质的物理性质如下表(*表示有机物与水形成的共沸物沸点)。
实验步骤如下:
Ⅰ.制备三苯甲醇
制备装置如图所示(加热及夹持装置略)。在仪器A中加入2.4g镁屑,向恒压滴液漏斗中加入10.6mL(0.10mol)溴苯和25.0mL无水乙醚的混合液,启动搅拌器,将部分混合液加入A中,开始反应后再逐滴加入余下的混合液。充分反应后,将A置于冰水浴中,滴加14.5g(0.08mol)二苯酮和25.0mL无水乙醚的混合液,水浴回流60min。然后慢慢滴加30.0mL饱和 溶液。
溶液。
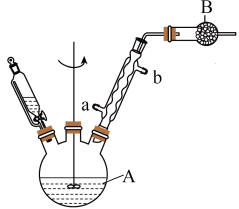
Ⅱ.提纯三苯甲醇
将A中的物质转移入圆底烧瓶中,用水蒸气蒸馏装置分离出乙醚、溴苯并回收利用,向残留液中加入石油醚,获取粗产品。
回答下列问题:
(1)装置图中A的名称为___________ ,球形冷凝管的进水口为___________ (填“a”或“b”),B中试剂为___________ (写名称)。
(2)步骤Ⅰ中,若溴苯和无水乙醚的混合液滴加过快,生成的有机副产物主要为___________ (写结构简式)。
(3)步骤Ⅰ中,饱和 溶液的作用是
溶液的作用是___________ 。
(4)步骤Ⅱ中,选择合适的仪器并组装蒸馏装置分离出乙醚、溴苯(加热及夹持装置略),安装顺序为①②___________ (填序号);水蒸气蒸馏能除去溴苯的原因是___________ 。
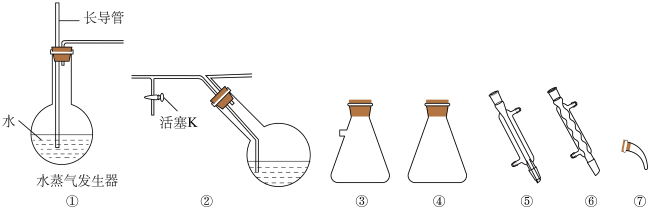
(5)加入石油醚后过滤得到粗产品,粗产品精制的实验方法是___________ 。
(6)若最后得到13.0g三苯甲醇,则三苯甲醇的产率为___________ 。

已知:
①格氏试剂(RMgBr)性质活泼,可与水、二氧化碳、卤代烃、醛、酮等物质反应,如:
②
③几种物质的物理性质如下表(*表示有机物与水形成的共沸物沸点)。
| 物质 | 相对分子质量 | 沸点/℃ | 存在状态及溶解性 |
| 无水乙醚 | 74 | 35(34*) | 微溶于水的液体 |
| 溴苯 | 157 | 156.2(92.8*) | 不溶于水的液体,溶于乙醚、乙醇 |
| 二苯酮 | 182 | 305.4 | 不溶于水的晶体,溶于乙醚 |
| 三苯甲醇 | 260 | 380 | 不溶于水及石油醚的白色晶体,溶于乙醇、乙醚 |
Ⅰ.制备三苯甲醇
制备装置如图所示(加热及夹持装置略)。在仪器A中加入2.4g镁屑,向恒压滴液漏斗中加入10.6mL(0.10mol)溴苯和25.0mL无水乙醚的混合液,启动搅拌器,将部分混合液加入A中,开始反应后再逐滴加入余下的混合液。充分反应后,将A置于冰水浴中,滴加14.5g(0.08mol)二苯酮和25.0mL无水乙醚的混合液,水浴回流60min。然后慢慢滴加30.0mL饱和

Ⅱ.提纯三苯甲醇
将A中的物质转移入圆底烧瓶中,用水蒸气蒸馏装置分离出乙醚、溴苯并回收利用,向残留液中加入石油醚,获取粗产品。
回答下列问题:
(1)装置图中A的名称为
(2)步骤Ⅰ中,若溴苯和无水乙醚的混合液滴加过快,生成的有机副产物主要为
(3)步骤Ⅰ中,饱和
(4)步骤Ⅱ中,选择合适的仪器并组装蒸馏装置分离出乙醚、溴苯(加热及夹持装置略),安装顺序为①②

(5)加入石油醚后过滤得到粗产品,粗产品精制的实验方法是
(6)若最后得到13.0g三苯甲醇,则三苯甲醇的产率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


