单选题 适中0.65 引用1 组卷587
氯及其化合物应用广泛。氯的单质Cl2可由MnO2与浓盐酸共热得到,Cl2能氧化Br-,可从海水中提取Br2;氯的氧化物ClO2可用于自来水消毒,ClO2是一种黄绿色气体,易溶于水,与碱反应会生成ClO 与ClO
与ClO ,在稀硫酸和NaClO3的混合溶液中通入SO2气体可制得ClO2;漂白液和漂白粉的有效成分是次氯酸盐,可作棉、麻的漂白剂。实验室制取高浓度的HClO溶液,有关实验装置和原理能达到实验目的的是
,在稀硫酸和NaClO3的混合溶液中通入SO2气体可制得ClO2;漂白液和漂白粉的有效成分是次氯酸盐,可作棉、麻的漂白剂。实验室制取高浓度的HClO溶液,有关实验装置和原理能达到实验目的的是
A.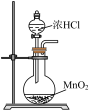 制取氯气 制取氯气 | B. 制取氯水 制取氯水 |
C. 提高HClO浓度 提高HClO浓度 | D. 分离HClO 分离HClO |
2023·江苏镇江·一模
类题推荐
氯及其化合物应用广泛。氯的单质Cl2可由MnO2与浓盐酸共热得到,Cl2能氧化Br-,可从海水中提取Br2;氯的氧化物ClO2可用于自来水消毒,ClO2是一种黄绿色气体,易溶于水,与碱反应会生成ClO 与ClO
与ClO ;亚氯酸钠(NaClO2)是一种高效漂白剂和氧化剂。亚氯酸钠(NaClO2)实验室制备过程为:①在强酸性介质中用SO2还原NaClO3制备ClO2;②在碱性介质中ClO2与H2O2反应,得到亚氯酸钠溶液;③再经一系列操作可得亚氯酸钠固体。下列说法正确的是
;亚氯酸钠(NaClO2)是一种高效漂白剂和氧化剂。亚氯酸钠(NaClO2)实验室制备过程为:①在强酸性介质中用SO2还原NaClO3制备ClO2;②在碱性介质中ClO2与H2O2反应,得到亚氯酸钠溶液;③再经一系列操作可得亚氯酸钠固体。下列说法正确的是
| A.①中可用盐酸作强酸性介质,②中可用NaOH作碱性介质 |
| B.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为1∶2 |
| C.反应②中的H2O2可用NaClO4代替 |
| D.若通过原电池反应来实现①,正极的电极反应为ClO |
二氧化氯(ClO2)是一种黄绿色、极易爆炸的强氧化性气体,易溶于水,在水中溶解度约为Cl2的5倍,其水溶液在较高温度与光照下会生成ClO 和ClO
和ClO 。实验室制备ClO2的反应为2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。下列有关物质的性质和用途具有对应关系的是
。实验室制备ClO2的反应为2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。下列有关物质的性质和用途具有对应关系的是
| 性质 | 用途 | |
| A | Cl2能溶于水 | 水体杀菌消毒 |
| B | ClO2有强氧化性 | 水体杀菌消毒 |
| C | HClO呈弱酸性 | 棉、麻漂白 |
| D | FeCl3(aq)呈酸性 | 蚀刻电路板上的铜 |
| A.A | B.B | C.C | D.D |
二氧化氯(ClO2)是一种黄绿色气体,易溶于水,在水中的溶解度约为Cl2的5倍,其水溶液在较高温度与光照下会生成ClO 与ClO
与ClO 。ClO2是一种极易爆炸的强氧化性气体,实验室制备ClO2的反应为2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。下列有关物质的性质和用途具有对应关系的是
。ClO2是一种极易爆炸的强氧化性气体,实验室制备ClO2的反应为2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。下列有关物质的性质和用途具有对应关系的是
| A.Cl2能溶于水,可用于工业制盐酸 |
| B.HClO不稳定,可用于棉、麻漂白 |
| C.ClO2有强氧化性,可用于水体杀菌消毒 |
| D.FeCl3溶液呈酸性,可用于蚀刻电路板上的铜 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


