填空题 适中0.65 引用1 组卷267
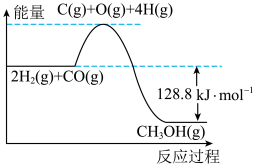
I.在2L的恒容密闭容器中充入1mol CO和2molH2, 一定条件下发生反应:CO(g)+2H2(g)  CH3OH (g),测得CO和CH3OH(g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
CH3OH (g),测得CO和CH3OH(g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
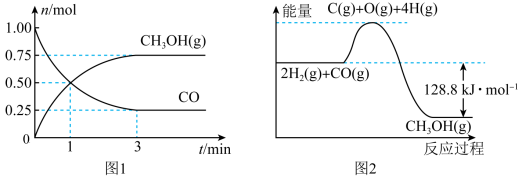
(1)从反应开始至达到平衡,以H2表示的反应的平均反应速率v(H2)=_________ 。外界条件不变时,随着反应的进行,该反应的化学反应速率逐渐减小的原因可能是_________ (填字母)。
A.温度减低 B.压强降低,
C.CO的浓度减小 D.CH3OH 的浓度增大
(2)下列描述中能说明上述反应达到平衡状态的是___________
(3)平衡时H2的转化率为___________ ,平衡时与起始时容器内的压强比为_______ ;
(4)已知断开1mol CO(g)和2mol H2(g)中的化学键需要吸收的能量为1924kJ,则断开lmol CH3OH(g)中的化学键共需要吸收___________ kJ的能量。
Ⅱ.电能是现代社会应用最广泛的能源之一
(5)关于图I所示装置的说法中,正确的是_________ 。
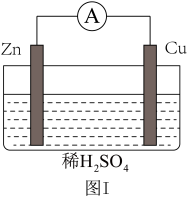
a.负极反应是Zn-2e-=Zn2+
b.电子由Zn片通过导线流向Cu片
c.一段时间后,溶液酸性增强
d.溶液中的H+向Cu片移动
(6)图I所示原电池中,当Cu表面析出4.48L氢气(标准状况)时,导线中通过的电子的物质的量为___________ mol。
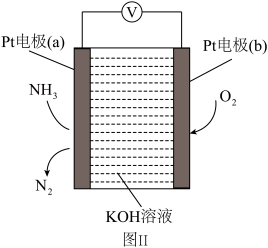
(7)图Ⅱ所示装置为电化学气级传感器,通过电压表示数可测量环境中NH3的含量。电极b是___________ 。(填“正”或“负”)极:电极a上发生的电极反应为___________ 。

(1)从反应开始至达到平衡,以H2表示的反应的平均反应速率v(H2)=
A.温度减低 B.压强降低,
C.CO的浓度减小 D.CH3OH 的浓度增大
(2)下列描述中能说明上述反应达到平衡状态的是___________
| A.CO、H2和CH3OH三种物质的浓度相等 |
| B.混合气体的密度不随时间的变化而变化 |
| C.混合气体的总物质的量不随时间的变化而变化 |
| D.单位时间内消耗2mol H2的同时生成lmol CH3OH |
(4)已知断开1mol CO(g)和2mol H2(g)中的化学键需要吸收的能量为1924kJ,则断开lmol CH3OH(g)中的化学键共需要吸收
Ⅱ.电能是现代社会应用最广泛的能源之一
(5)关于图I所示装置的说法中,正确的是

a.负极反应是Zn-2e-=Zn2+
b.电子由Zn片通过导线流向Cu片
c.一段时间后,溶液酸性增强
d.溶液中的H+向Cu片移动
(6)图I所示原电池中,当Cu表面析出4.48L氢气(标准状况)时,导线中通过的电子的物质的量为
(7)图Ⅱ所示装置为电化学气级传感器,通过电压表示数可测量环境中NH3的含量。电极b是

22-23高一下·广东广州·期中
类题推荐
化学反应与能量,是学习和研究化学原理的重要内容。在2L的恒容密闭容器中充入1molCO和2mol ,一定条件下发生反应:
,一定条件下发生反应: ,测得CO和
,测得CO和 (g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
(g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
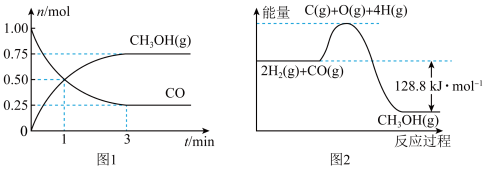
(1)从反应开始至达到平衡,以CO表示的反应的平均反应速率
___________  。下列措施能增大反应速率的是
。下列措施能增大反应速率的是___________ (填字母)。
A.升高温度 B.降低压强 C.减小 的浓度 D.加入合适的催化剂
的浓度 D.加入合适的催化剂
(2)下列描述中能说明上述反应达到平衡状态的是___________。
(3)平衡时CO的体积分数(即物质的量分数)为___________ (保留3位有效数字)。
(4)该反应是___________ 反应(填“吸热”或“放热”),已知断开1molCO(g)和2mol (g)中的化学键需要吸收的能量为1924kJ,则断开1mol
(g)中的化学键需要吸收的能量为1924kJ,则断开1mol (g)中的化学键所需要吸收
(g)中的化学键所需要吸收________ kJ的能量。
(5) 归燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为
归燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为 。则下列说法正确的是
。则下列说法正确的是___________ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4g 转移1.2mol电子
转移1.2mol电子

(1)从反应开始至达到平衡,以CO表示的反应的平均反应速率
A.升高温度 B.降低压强 C.减小
(2)下列描述中能说明上述反应达到平衡状态的是___________。
| A.CO、 |
| B.混合气体的密度不随时间的变化而变化 |
| C.混合气体的总物质的量不随时间的变化而变化 |
| D.单位时间内消耗2mol |
(4)该反应是
(5)
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4g
在2L的恒容密闭容器中充入1molCO和2molH2,一定条件下发生反应:
COg2H2g=CH3OHg,测得和 CH3OH(g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。___________ 。平衡时H2的转化率为___________ 。
(2)下列措施能增大反应速率的是___________ (填字母)。
(3)下列描述中能说明上述反应达到平衡状态的是___________。
(4)已知断开 1molCO(g)和 2molH2(g)中的化学键需要吸收的能量为 1924kJ,则断开 1mol CH3OH(g)中的化学键所需要吸收___________ kJ 的能量。
COg2H2g=CH3OHg,测得和 CH3OH(g)的物质的量变化如图1所示,反应过程中的能量变化如图2所示。

(2)下列措施能增大反应速率的是___________ (填字母)。
| A.升高温度 | B.降低压强 | C.减小 CH3OH 的浓度 | D.加入合适的催化剂 |
(3)下列描述中能说明上述反应达到平衡状态的是___________。
| A.CO、H2和CH3OH 三种物质的浓度相等 |
| B.混合气体的密度不随时间的变化而变化 |
| C.混合气体的总物质的量不随时间的变化而变化 |
| D.单位时间内消耗 2molH2 的同时生成 1molCH3OH |
(4)已知断开 1molCO(g)和 2molH2(g)中的化学键需要吸收的能量为 1924kJ,则断开 1mol CH3OH(g)中的化学键所需要吸收
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网