解答题-实验探究题 较难0.4 引用2 组卷595
实验室以活性炭为催化剂,由 制备三氯化六氨合钴(Ⅲ)
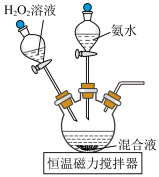
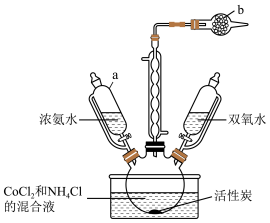
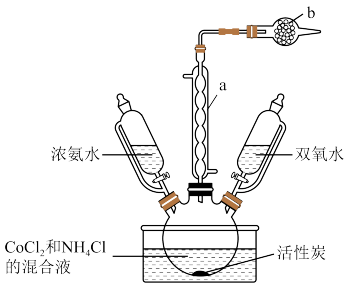
制备三氯化六氨合钴(Ⅲ) 的装置如图所示:
的装置如图所示:

已知: ;
; 具有较强还原性,
具有较强还原性, 不易被氧化。
不易被氧化。
回答下列问题:
(1)仪器c的名称是___________ ;d中无水 的作用是
的作用是___________ 。
(2)向混合液中先加入浓氨水,目的是___________ ,混合液中 的作用是
的作用是___________ ;充分反应后再加入双氧水,水浴加热,控制温度为55℃的原因是___________ 。
(3) 制备
制备 的化学方程式为
的化学方程式为___________ ;将反应后的混合物趁热过滤,待滤液冷却后加入适量浓盐酸,冰水冷却、抽滤、乙醇洗涤、干燥,得到 晶体,抽滤的优点是
晶体,抽滤的优点是___________ 。
(4)为测定产品中钴的含量,进行下列实验:
Ⅰ.称取3.5400g产品,加入足量NaOH溶液蒸出 ,再加入稀硫酸,使
,再加入稀硫酸,使 全部转化为
全部转化为 ,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用
,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用 标准溶液滴定至终点,消耗标准溶液13.30mL。
标准溶液滴定至终点,消耗标准溶液13.30mL。
Ⅱ.另取与步骤Ⅰ中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗 标准溶液1.30mL。
标准溶液1.30mL。
①样品中钴元素的质量分数为___________ 。
②若步骤Ⅱ滴定前滴定管内无气泡,滴定后有气泡,会使测定结果___________ (填“偏大”“偏小”或“不变”)。

已知:
回答下列问题:
(1)仪器c的名称是
(2)向混合液中先加入浓氨水,目的是
(3)
(4)为测定产品中钴的含量,进行下列实验:
Ⅰ.称取3.5400g产品,加入足量NaOH溶液蒸出
Ⅱ.另取与步骤Ⅰ中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗
①样品中钴元素的质量分数为
②若步骤Ⅱ滴定前滴定管内无气泡,滴定后有气泡,会使测定结果
2023·山东临沂·二模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网