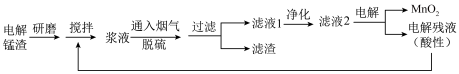
解答题-工业流程题 适中0.65 引用3 组卷557
电解锰渣含有 等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含
等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含 等)中
等)中 的同时,实现电解锰渣的资源化利用。
的同时,实现电解锰渣的资源化利用。
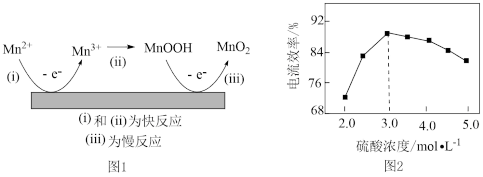
(1)上述流程中为增大反应速率采取的措施有_______ 。
(2)电解锰渣中的 能吸收烟气中的
能吸收烟气中的 ,反应的方程式为
,反应的方程式为_______ 。
(3)电解锰渣与电解残液混合后,浆液中部分离子浓度 及
及 在脱硫过程中的变化如下。
在脱硫过程中的变化如下。
①用方程式表示脱硫过程溶液 降低的原因
降低的原因_______ 。
②分析浆液中 浓度增大的原因:
浓度增大的原因:
i. 被
被 还原;
还原;
ii. 被
被 还原,离子方程式为
还原,离子方程式为_______ ;
iii._______ (用离子方程式表示)。
(4)电解获得 ,装置如下图所示。
,装置如下图所示。
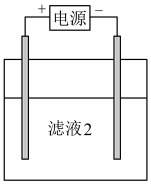
①滤液2在电解池_______ (填“阳”或“阴”)极放电产生 。
。
②净化过程须除去 。研究发现,滤液2中即使含有少量
。研究发现,滤液2中即使含有少量 ,也会导致
,也会导致 产率大幅降低,分析原因:
产率大幅降低,分析原因:_______ 。

(1)上述流程中为增大反应速率采取的措施有
(2)电解锰渣中的
(3)电解锰渣与电解残液混合后,浆液中部分离子浓度
| 7.5 | |||||
| 1.7 |
②分析浆液中
i.
ii.
iii.
(4)电解获得

①滤液2在电解池
②净化过程须除去
2023·北京朝阳·二模
类题推荐
锰酸锂( )是一种锂离子电池正极材料。以软锰矿浆液(含
)是一种锂离子电池正极材料。以软锰矿浆液(含 及少量
及少量 、
、 、
、 、
、 、
、 、
、 等的氧化物)烟气脱硫吸收液为原料,制备锰酸锂的流程如下:
等的氧化物)烟气脱硫吸收液为原料,制备锰酸锂的流程如下:

(1)“浸取”在题图所示的装置中进行,反应生成 ,
, 将
将 转化为
转化为 的离子方程式为
的离子方程式为_______ 。 局部过量会产生
局部过量会产生 ,保持温度、流速、反应时间、反应物和溶剂的量不变,为减少
,保持温度、流速、反应时间、反应物和溶剂的量不变,为减少 的产生可采取的措施是
的产生可采取的措施是_______ 。

(2)“浸取”液除杂后可获得较纯的 溶液(重金属离子质量浓度小于
溶液(重金属离子质量浓度小于 )。重金属离子质量浓度(
)。重金属离子质量浓度( )在除杂中的变化如下表所示。
)在除杂中的变化如下表所示。
已知:① 的价格:3000元/吨;
的价格:3000元/吨; 的价格:57500元/吨。
的价格:57500元/吨。
②大量使用 会造成污染,实验的滤液中按
会造成污染,实验的滤液中按 用量添加
用量添加 溶液沉淀重金属。
溶液沉淀重金属。
③中和氧化液的 在5~6之间。浸取液中
在5~6之间。浸取液中 沉淀完全,需要
沉淀完全,需要 大于9.
大于9.
请设计“除杂”的实验方案:量取浸取液,_______ ,得到较纯的 溶液。[须使用的试剂:
溶液。[须使用的试剂: 、
、 溶液、空气]。
溶液、空气]。
(3)为确定“锂化”需加入的 的质量,需要知道沉锰所得固体[
的质量,需要知道沉锰所得固体[ 、
、 和
和 ]中
]中 元素的质量。若
元素的质量。若 与沉锰所得固体在
与沉锰所得固体在 恰好完全反应,则
恰好完全反应,则 与
与 、
、 和
和 需要满足的关系为
需要满足的关系为_______ 。
(4)固相法制备 的实验过程如下:将高纯
的实验过程如下:将高纯 和
和 按一定的比例混合均匀,控制温度为
按一定的比例混合均匀,控制温度为 使其充分反应,两者恰好完全反应生成
使其充分反应,两者恰好完全反应生成 和气体。
和气体。
①纯净的 分解为
分解为 和
和 的温度为
的温度为 ,而固相法制备
,而固相法制备 的实验中,当温度升高至
的实验中,当温度升高至 时,便产生
时,便产生 气体,其可能的原因是
气体,其可能的原因是_______ 。
②固相法制备 的实验中产生的气体有
的实验中产生的气体有_______ 。
③用沉锰所得固体制备 与固相法制备
与固相法制备 的相比,其优点为
的相比,其优点为_______ 。

(1)“浸取”在题图所示的装置中进行,反应生成

(2)“浸取”液除杂后可获得较纯的
已知:①
②大量使用
③中和氧化液的
| 离子 | ||||||
| 浸出液 | 1058.2 | 1131 | 56.87 | 41.23 | 20.58 | 18.69 |
| 中和氧化液 | 3.51 | 6.23 | 54.26 | 37.67 | 18.32 | 17.89 |
| 硫化后液 | 0.43 | 0.89 | 0.59 | 0.13 | 0.06 | 0.04 |
(3)为确定“锂化”需加入的
(4)固相法制备
①纯净的
②固相法制备
③用沉锰所得固体制备
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网