填空题 适中0.65 引用2 组卷543
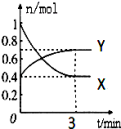
容积均为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2 mol的NO2,发生反应:2NO2(g)  N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是
N2O4(g) ΔH<0,甲中NO2的相关量随时间变化如下图所示。0~3 s内,甲容器中NO2的反应速率增大的原因是___________

2023高三·全国·专题练习
类题推荐
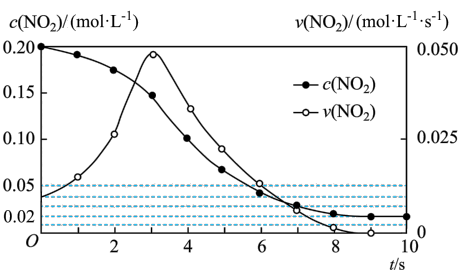
容积均为1L的甲、乙两个刚性容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2molNO2,发生反应2NO2(g) N2O4(g)ΔH<0。甲容器中NO2的相关量随时间变化关系如图所示。下列说法正确的是
N2O4(g)ΔH<0。甲容器中NO2的相关量随时间变化关系如图所示。下列说法正确的是
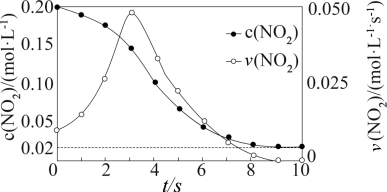

| A.0~3s内,甲容器中NO2反应速率增大的原因是催化剂活性增加 |
| B.3s时甲容器中反应达到化学平衡状态 |
| C.K乙<225L/mol |
| D.欲使甲、乙两容器中NO2的体积分数相等可分离部分乙容器中的N2O4 |
向恒温和绝热的两个体积均为2.0L的恒容密闭容器中分别充入4.0molNO和4.0molO3,发生反应:NO(g)+O3(g) NO2(g)+O2(g),在起始温度相同的条件下,经过一段时间后达到平衡。反应过程中n(NO)随时间变化的情况如表。
NO2(g)+O2(g),在起始温度相同的条件下,经过一段时间后达到平衡。反应过程中n(NO)随时间变化的情况如表。
下列说法错误的是
| 时间/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | |
| 甲 | n(NO)/mol | 4.0 | 3.0 | 2.2 | 1.6 | 1.2 | 0.8 | 0.6 | 0.6 | 0.6 |
| 乙 | 4.0 | 2.9 | 1.7 | 1.0 | 0.9 | 0.8 | 0.8 | 0.8 | 0.8 | |
| A.乙容器为绝热容器 |
| B.该反应的△H<0 |
| C.甲容器中用O2表示0~20s内的平均反应速率为1.4mol·L-1·s-1 |
| D.若在甲容器中充入的是2.0molNO和2.0molO3,则平衡后得到1.7molO2 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网