解答题-原理综合题 较难0.4 引用1 组卷198
烟气中的主要污染物是 、NO,工业上有多种烟气脱硫、脱硝的方法,具体如下:
、NO,工业上有多种烟气脱硫、脱硝的方法,具体如下:
Ⅰ.烟气经 预处理后用
预处理后用 水悬浮液吸收,可减少烟气中
水悬浮液吸收,可减少烟气中 、NO的含量。
、NO的含量。
 氧化烟气中
氧化烟气中 、
、 ,的主要反应的热化学方程式为:
,的主要反应的热化学方程式为:






(1)反应 的
的
___________  。
。
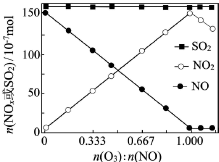
(2)室温下,固定进入反应器的NO、 的物质的量,改变加入
的物质的量,改变加入 的物质的量,反应一段时间后体系中n(NO)、n(
的物质的量,反应一段时间后体系中n(NO)、n( )和n(
)和n( )随反应前n(
)随反应前n( ):n(NO)的变化见图:
):n(NO)的变化见图:
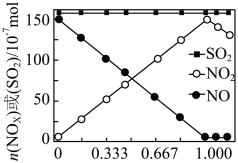
当n( ):n(NO)
):n(NO) 时,反应后
时,反应后 的物质的量减少,其原因是
的物质的量减少,其原因是___________ ;增加n( ),
), 氧化
氧化 的反应几乎不受影响,其可能原因是
的反应几乎不受影响,其可能原因是___________ 。
(3)当用 水悬浮液吸收经
水悬浮液吸收经 预处理的烟气时,清液(pH约为8)中
预处理的烟气时,清液(pH约为8)中 将
将 转化为
转化为 ,其离子方程式为
,其离子方程式为___________ 。
Ⅱ.NaClO溶液在不同温度下也可对烟气中的硫、硝脱除,一定时间内,其脱除率如下图所示。
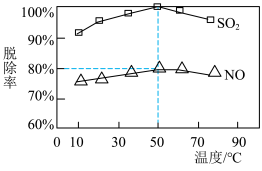
(4)烟气中 和NO体积比为2:1,烟气于50℃时的吸收液转化生成的n(
和NO体积比为2:1,烟气于50℃时的吸收液转化生成的n( ):n(
):n( )
)
___________ 。
Ⅲ.可利用CO为还原剂在催化剂作用下将NO脱除并转化为 和
和 。在一定温度下,向体积为1L的刚性容器中加入1.28 mol CO和1mol NO,发生的反应方程式如下:
。在一定温度下,向体积为1L的刚性容器中加入1.28 mol CO和1mol NO,发生的反应方程式如下:


(5)下述情况能说明反应体系已达到平衡的是___________ 。
a.CO与NO转化率之比不再改变 b.混合气体的密度不再变化
c.混合气体的平均相对分子质量不变 d.v(CO):v( )
)
(6)若达到平衡时NO的转化率为80%, 的选择性为60%,则
的选择性为60%,则
___________ 。( 的选择性
的选择性 )
)
Ⅰ.烟气经
(1)反应
(2)室温下,固定进入反应器的NO、

当n(
(3)当用
Ⅱ.NaClO溶液在不同温度下也可对烟气中的硫、硝脱除,一定时间内,其脱除率如下图所示。

(4)烟气中
Ⅲ.可利用CO为还原剂在催化剂作用下将NO脱除并转化为
(5)下述情况能说明反应体系已达到平衡的是
a.CO与NO转化率之比不再改变 b.混合气体的密度不再变化
c.混合气体的平均相对分子质量不变 d.v(CO):v(
(6)若达到平衡时NO的转化率为80%,
22-23高三下·湖北宜昌·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

 SO3(g)+O2(g) △H3
SO3(g)+O2(g) △H3



