解答题-原理综合题 适中0.65 引用1 组卷125
CO2与生活和生产息息相关,其资源化是我国实现“碳达峰”、“碳中和”的有效途径之一、回答下列问题:
(1) CO2甲醇化:CO2、CO与H2反应制备甲醇,涉及的反应有:
Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ. 。
。
①
_______  。
。
②现利用反应Ⅰ和反应Ⅱ合成CH3OH,已知CO可使反应的催化剂寿命降低。若氢碳比表示为 ,则理论上
,则理论上
_______ 时,原料气的利用率最高,生产中往往采用略高于该值的氢碳比,其目的是_______ 。
(2)CO2碳酸酯化:CO2与环氧丙烷反应合成碳酸丙烯酯,其反应历程如图甲所示(*表示某催化剂的活化中心或活性基团)。
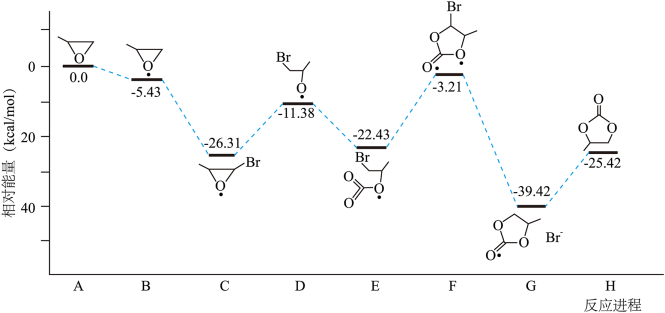
图甲
①H分子中 键与
键与 键的个数之比为
键的个数之比为_______ 。
②决定总反应速率大小的步骤是_______ (填字母),该步骤的能垒(活化能)为_______  。
。
a.A→B b.C→D c.E→F d.F→G
(3)CO2乙烯化:反应原理为2CO2(g)+6H2(g) C2H4(g)+4H2O(g),以n(H2):n(CO2)=3:1的投料比充入体积固定的密闭容器中发生反应,不同温度下平衡时的四种气态物质的物质的量分数如图乙所示,温度为
C2H4(g)+4H2O(g),以n(H2):n(CO2)=3:1的投料比充入体积固定的密闭容器中发生反应,不同温度下平衡时的四种气态物质的物质的量分数如图乙所示,温度为 、反应达到平衡状态时,容器内的压强为
、反应达到平衡状态时,容器内的压强为 。
。
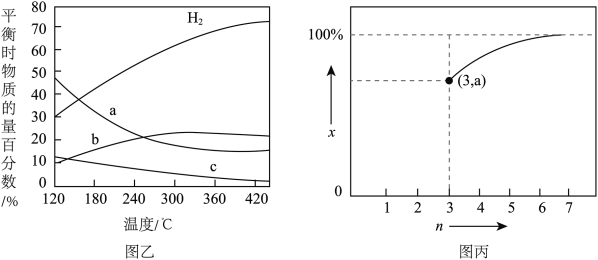
①120℃该反应的平衡常数Kp=_______ (列出算式,以平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
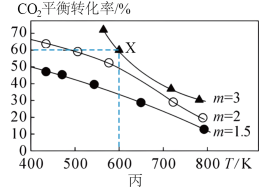
②若以H2和CO2的物质的量之比为n:1( )进行投料,温度控制为120℃,相应平衡体系中CO2的转化率为x,x随
)进行投料,温度控制为120℃,相应平衡体系中CO2的转化率为x,x随 变化的关系如图丙所示,a=
变化的关系如图丙所示,a=_______ %(保留3位有效数字)。
(1) CO2甲醇化:CO2、CO与H2反应制备甲醇,涉及的反应有:
Ⅰ.
Ⅱ.
Ⅲ.
①
②现利用反应Ⅰ和反应Ⅱ合成CH3OH,已知CO可使反应的催化剂寿命降低。若氢碳比表示为
(2)CO2碳酸酯化:CO2与环氧丙烷反应合成碳酸丙烯酯,其反应历程如图甲所示(*表示某催化剂的活化中心或活性基团)。

图甲
①H分子中
②决定总反应速率大小的步骤是
a.A→B b.C→D c.E→F d.F→G
(3)CO2乙烯化:反应原理为2CO2(g)+6H2(g)

①120℃该反应的平衡常数Kp=
②若以H2和CO2的物质的量之比为n:1(
22-23高三下·河北邢台·阶段练习
类题推荐
我国承诺 2030年前做到“碳达峰和碳中和”,这里的碳主要指CO2, CO2与我们生活和生产息息相关。请回答:
(1)工业上常用CO和CO2与氢气反应制备甲醇,涉及的反应有:
主反应:
I . CO(g)+2H2(g) CH3OH(g) △H1= -90.7 kJ·mol-1
CH3OH(g) △H1= -90.7 kJ·mol-1
II. CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2= -49.0 kJ·mol-1
CH3OH(g)+H2O(g) △H2= -49.0 kJ·mol-1
副反应:
III. CO(g)+H2O(g) CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3
IV. 2CH3OH(g) CH3OCH3(g)+H2O(g) △H4= -23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H4= -23.5 kJ·mol-1
请回答:
①△H3=________ kJ·mol-1。
②现利用I和II两个反应合成CH3OH,已知CO可使反应的催化剂寿命降低。若氢碳比表示为x= ,则理论上x=
,则理论上x=_______ 时,原料气的利用率最高。但生产中往往采用略高于该值的氢碳比,理由是___________ 。
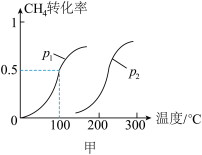
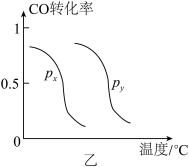
(2)CO2甲烷化技术是碳中和理念的落脚点之一,反应为CO2(g)+ 4H2(g) CH4(g)+2H2O(g) △H= -165kJ·mol-1,其核心是催化剂的选择。其他条件均相同,在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如下图所示。
CH4(g)+2H2O(g) △H= -165kJ·mol-1,其核心是催化剂的选择。其他条件均相同,在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如下图所示。
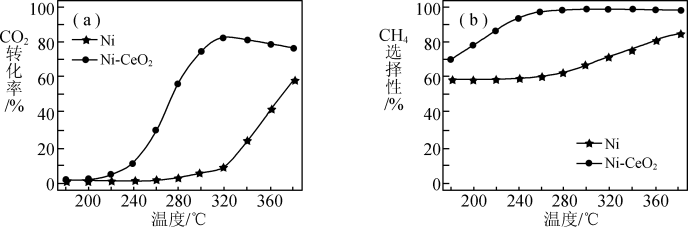
下列说法正确的是 。
(3)CO2可以与环氧丙烷反应合成碳酸丙烯酯:
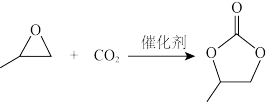 △H= - 110.5kJ·mol-1
△H= - 110.5kJ·mol-1
通过模型假设和理论计算,推测其反应历程如下图所示(*表示某催化剂的活化中心或活性基团):
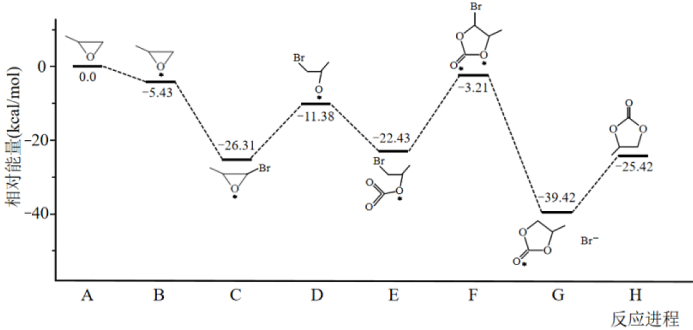
①决定总反应速率大小的步骤是______ (用图中字母表示), 该步骤的能垒(活化能)为_________ 。
②下列说法正确的是__________ 。
A.A →B能量降低,所以该过程必定自发
B.总反应为加成反应,D、F为过渡态,C、E为中间产物
C. D分子中氧原子带负电荷,强烈吸引CO2分子中的碳原子生成E,使体系能量降低
D.反应热的理论值(-25.42)与某次实测值(-110.5)相差太大,说明理论值几乎没有参考价值
(4)用CO2催化加氢可以合成低碳烯烃。反应开始时在0.1MPa 条件下,以n(H2) :n(CO2)=3:1的投料比充入体积固定的密闭容器中,发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g),不同温度下平衡时的四种气态物质的物质的量百分数如下图甲所示:
C2H4(g)+4H2O(g),不同温度下平衡时的四种气态物质的物质的量百分数如下图甲所示:
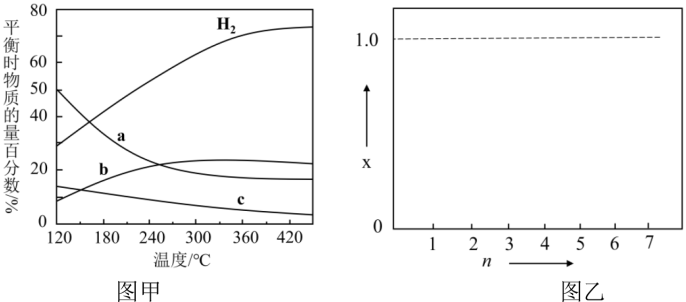
在120°C达到平衡时,CO2的转化率为________ ;若H2和CO2的物质的量之比为 n:1 (n≥3)进行投料,温度控制为120°C,相应平衡体系中CO2的转化率为x,在图乙中绘制x随n (n≥3 )变化的示意图________ (标出曲线的起点坐标)。
(1)工业上常用CO和CO2与氢气反应制备甲醇,涉及的反应有:
主反应:
I . CO(g)+2H2(g)
II. CO2(g)+3H2(g)
副反应:
III. CO(g)+H2O(g)
IV. 2CH3OH(g)
请回答:
①△H3=
②现利用I和II两个反应合成CH3OH,已知CO可使反应的催化剂寿命降低。若氢碳比表示为x=
(2)CO2甲烷化技术是碳中和理念的落脚点之一,反应为CO2(g)+ 4H2(g)

下列说法正确的是 。
| A.高于320°C后,以Ni- CeO2为催化剂,CO2转化率略有下降的原因一定是CO2甲烷化反应已达平衡,升高温度平衡右移 |
| B.高于320°C后,以Ni为催化剂,CO2转化率上升的原因一定是CO2甲烷化反应速率较慢,升高温度反应速率加快,反应相同时间时CO2转化率增加 |
| C.工业上应选择的催化剂是Ni- CeO2 |
| D.工业上应使用的合适温度为360°C |
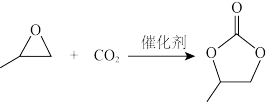 △H= - 110.5kJ·mol-1
△H= - 110.5kJ·mol-1通过模型假设和理论计算,推测其反应历程如下图所示(*表示某催化剂的活化中心或活性基团):

①决定总反应速率大小的步骤是
②下列说法正确的是
A.A →B能量降低,所以该过程必定自发
B.总反应为加成反应,D、F为过渡态,C、E为中间产物
C. D分子中氧原子带负电荷,强烈吸引CO2分子中的碳原子生成E,使体系能量降低
D.反应热的理论值(-25.42)与某次实测值(-110.5)相差太大,说明理论值几乎没有参考价值
(4)用CO2催化加氢可以合成低碳烯烃。反应开始时在0.1MPa 条件下,以n(H2) :n(CO2)=3:1的投料比充入体积固定的密闭容器中,发生反应:2CO2(g)+6H2(g)

在120°C达到平衡时,CO2的转化率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网