解答题-结构与性质 较易0.85 引用1 组卷64
X、Y、Z、W四种元素的部分信息如下表所示。
回答下列问题:
(1)X、Y、Z三种元素电负性由大到小的顺序为___________ (用具体的元素符号填写)。
(2)化合物 、
、 、
、 (气态或液态时)中,中心原子的轨道类型不是
(气态或液态时)中,中心原子的轨道类型不是 杂化的是
杂化的是___________ (填化学式,下同),分子构型是正四面体的是___________ , 属于
属于___________ (极性分子、非极性分子)。
(3)已知 的熔点:306℃,沸点:319℃,则
的熔点:306℃,沸点:319℃,则 的晶体类型为
的晶体类型为___________ 。
(4)在金属材料中添加 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
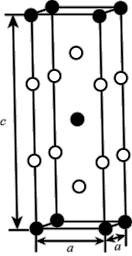
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如图所示。处于顶角位置的是
具有体心四方结构,如图所示。处于顶角位置的是___________ 原子。设Cr和Al原子半径分别为 和
和 ,则金属原子空间占有率为
,则金属原子空间占有率为___________ %(列出计算表达式)。
| 元素 | X | Y | Z | W |
| 相关信息 | 短周期元素,最高化合价为+7价 | 基态原子中,电子占据的最高能层符号为M,最高能级上只有两个自旋方向相同的电子 | Z元素的价电子构型为 | W元素正三价离子的3d轨道为半充满状态 |
回答下列问题:
(1)X、Y、Z三种元素电负性由大到小的顺序为
(2)化合物
(3)已知
(4)在金属材料中添加

22-23高二下·湖南永州·阶段练习
类题推荐
X、Y、Z、W四种元素的部分信息如下表所示。回答下列问题:
(1)W的基态原子电子排布式为_______ ,X、Z两种元素简单氢化物的稳定性顺序为_______ (用化学式填写)。
(2)化合物YX4、ZX3、ZX5(气态或液态时)中,中心原子的轨道类型分子构型是正四面体的是_______ (填化学式,下同),不是sp3杂化的是_______ ,ZX3属于_______ (极性分子、非极性分子)。
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为_______ 。
(4)Z原子的价电子轨道表示式为_______ 。
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为_______ ;若W的原子半径为rcm,阿伏加德罗常数为NA,则其体心立方晶体的晶胞密度可表示为_______ g/cm3(列出计算式)。
| 元素 | X | Y | Z | W |
| 相关信息 | 短周期元素,最高化合价为+7价 | 基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子 | 核外电子共有15种运动状态 | 能与X形成两种常见化合物WX2、WX3,WX2溶液呈浅绿色、WX3溶液呈黄色 |
(1)W的基态原子电子排布式为
(2)化合物YX4、ZX3、ZX5(气态或液态时)中,中心原子的轨道类型分子构型是正四面体的是
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为
(4)Z原子的价电子轨道表示式为
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为

X、Y、Z、W四种元素的部分信息如下表所示。
回答下列问题:
(1)W的基态原子电子排布式为___________ ,
(2)X、Y、Z三种元素电负性由大到小的顺序为___________ (用具体的元素符号填写)。
(3)Y的简单氢化物的空间构型___________ ,含___________ 键。(极性或非极性)
(4)Z原子的价电子轨道表示式为___________ ,在元素周期表中的位置___________ 。
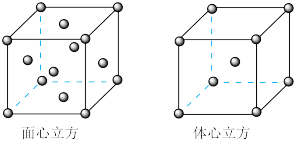
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为___________ ;若W的原子半径为rcm,阿伏加德罗常数为NA,则其体心立方晶体的密度可表示为___________ g•cm-3。
| 元素 | X | Y | Z | W |
| 相关 信息 | 短周期元素,最高化合价为+7价 | 基态原子中,电子占据的最高能层符号为L,能量最高的轨道上只有两个自旋方向相同的电子 | 核外电子共有15种运动状态 | 能与X形成两种常见化合物WX2、WX3,苯酚遇WX3溶液能发生显色反应 |
回答下列问题:
(1)W的基态原子电子排布式为
(2)X、Y、Z三种元素电负性由大到小的顺序为
(3)Y的简单氢化物的空间构型
(4)Z原子的价电子轨道表示式为
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为

有关元素的部分信息如下表所示:
回答下列问题:
(1)D的基态原子电子排布式为 ,A、B、D三种元素电负性由大到小的顺序为 (用具体的元素符号填写)。
(2)化合物BA4、RA3、RA5中,中心原子的轨道类型不是sp3杂化的是 ,分子构型是正四面体的是 ,属于极性分子的是 (用化学式填写)。
(3)已知DA3的沸点:319℃,熔点:306℃,则DA3的晶体类型为 ,B与氢元素能形成BnH2n+2(n为正整数)的一系列物质,这一系列物质沸点的变化规律是 。
(4)R可形成H3RO4、HRO3、H3RO3等多种酸,则这三种酸酸性由强到弱的顺序为 (用化学式填写)。
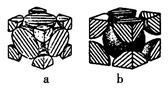
(5)已知D的单质有如图所示的两种常见堆积方式:其中属于面心立方最密堆积的是 (填a或b);若单质D按b方式紧密堆积,原子半径为r cm,NA表示阿伏加德罗常数的值,则单质D的密度 g/cm3(列出算式即可)。
| 元素 | A | B | R | D |
| 相应信息 | 短周期元素、最高正价为+7 | 基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子 | R核外电子共有15种运动状态 | D与A能形成两种常见的化合物DA2,DA3 |
回答下列问题:
(1)D的基态原子电子排布式为 ,A、B、D三种元素电负性由大到小的顺序为 (用具体的元素符号填写)。
(2)化合物BA4、RA3、RA5中,中心原子的轨道类型不是sp3杂化的是 ,分子构型是正四面体的是 ,属于极性分子的是 (用化学式填写)。
(3)已知DA3的沸点:319℃,熔点:306℃,则DA3的晶体类型为 ,B与氢元素能形成BnH2n+2(n为正整数)的一系列物质,这一系列物质沸点的变化规律是 。
(4)R可形成H3RO4、HRO3、H3RO3等多种酸,则这三种酸酸性由强到弱的顺序为 (用化学式填写)。
(5)已知D的单质有如图所示的两种常见堆积方式:其中属于面心立方最密堆积的是 (填a或b);若单质D按b方式紧密堆积,原子半径为r cm,NA表示阿伏加德罗常数的值,则单质D的密度 g/cm3(列出算式即可)。

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


